
���}Ŀ�����ڰl(f��)�F(xi��n)��H2S���^NO��CO֮��ĵ����������wϵ���w��̖���ӣ������Ѕ��c�{��(ji��)����̖���f���揈Ѫ�ܜp�p��Ѫ���Ĺ��ܡ��ش����І��}��
��1���D��ͨ�^�ữ�Wѭ�h(hu��n)���^�͜ض�����ˮ����ֽ��Ƃ���ķ���ϵ�y(t��ng)ԭ����

ͨ�^Ӌ�㣬��֪ϵ�y(t��ng)�����ƚ�ğữ�W����ʽ��_____________��
��2��H2S�cCO2�ڸߜ��°l(f��)��������H2S(g)+CO2(g) ![]() COS(g) +H2O(g)����610 K�r����0.10 mol CO2�c0.40 mol H2S����2.5 L�Ŀ��ƿ�У�����ƽ���ˮ�����|�����֔�(sh��)��0.02����H2S��ƽ���D����
COS(g) +H2O(g)����610 K�r����0.10 mol CO2�c0.40 mol H2S����2.5 L�Ŀ��ƿ�У�����ƽ���ˮ�����|�����֔�(sh��)��0.02����H2S��ƽ���D����![]() =____%������ƽ�ⳣ��(sh��)K=_____��
=____%������ƽ�ⳣ��(sh��)K=_____��
��3��H2S��SO2�����h(hu��n)�������w��������O���Σ�������I(y��)�ϲ�ȡ��N�����p���@Щ�к����w���ŷţ���֪25�棬NH3��H2O��Kb=1.8��105��H2SO3��Ka1=1.3��102��Ka2=6.2��108������ˮ�ĝ�Ȟ�2.0 mol��L1����Һ�е�c(OH)=________ mol��L1����SO2ͨ��ԓ��ˮ�У���c(OH)����1.0��107 mol��L1�r����Һ�е�c(![]() )/c(
)/c(![]() )=___________________��
)=___________________��
���𰸡�H2O(l)=H2(g)+ ![]() O2(g) ��H=+286 kJ/mol 2.5 2.85��10�C3 6.2��10-8 0.62
O2(g) ��H=+286 kJ/mol 2.5 2.85��10�C3 6.2��10-8 0.62
��������
(1)ϵ�y(t��ng)(��)�漰ˮ�ķֽ⣬�����w˹���ɷքe��ϵ�y(t��ng)(��)�ğữ�W����ʽ��ӣ��ɵõ�ˮ�ֽ�ğữ�W����ʽ���tϵ�y(t��ng)(I)�ğữ�W����ʽH2O(l)=H2(g)+![]() O2(g)��H=+286kJ/mol��
O2(g)��H=+286kJ/mol��
(2)���ڷ��� H2S(g)+CO2(g) ![]() COS(g)+H2O(g)
COS(g)+H2O(g)
��ʼ(mol) 0.40 0.10 0 0
�D��(mol) x x x x
ƽ��(mol) 0.40-x 0.10-x x x
����ƽ���ˮ�����|�����֔�(sh��)��0.02���t![]() =0.02��x=0.01��H2S��ƽ���D����a1=
=0.02��x=0.01��H2S��ƽ���D����a1=![]() ��100%=2.5%���w�e��2.5L���tƽ��r�����|�ĝ�Ȟ�c(H2S)=
��100%=2.5%���w�e��2.5L���tƽ��r�����|�ĝ�Ȟ�c(H2S)=![]() mol/L=0.156mol/L��c(CO2)=
mol/L=0.156mol/L��c(CO2)=![]() mol/L=0.036mol/L��c(COS)=c(H2O)=
mol/L=0.036mol/L��c(COS)=c(H2O)=![]() mol/L=0.004mol/L���tK=
mol/L=0.004mol/L���tK=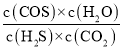 =
=![]() =2.85��10�C3��
=2.85��10�C3��
(3)NH3H2O��Kb=1.8��10-5������ˮ�ĝ�Ȟ�2.0molL-1����Kb=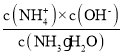 ��֪c(OH-)=
��֪c(OH-)=![]() mol/L=6.0��10-3mol/L����c(OH-)����1.0��10-7molL-1�r��
mol/L=6.0��10-3mol/L����c(OH-)����1.0��10-7molL-1�r��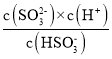 ��֪c(SO32-)/c(HSO3-)=0.62��
��֪c(SO32-)/c(HSO3-)=0.62��



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�������ЙC���������_����
A. 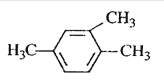 1,3,4-���ױ�
1,3,4-���ױ�
B. 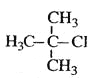 2-��-2-�ȱ���
2-��-2-�ȱ���
C. 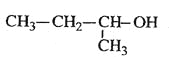 2-��-1-����
2-��-1-����
D. 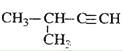 2-��-3-��Ȳ
2-��-3-��Ȳ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����һ���]�����ȣ�����0.8mol����0.6mol�����⣬�l(f��)������H2(g)+I2(g)![]() 2HI(g)�������и����|����S�r�g׃�����_�ĈD���
2HI(g)�������и����|����S�r�g׃�����_�ĈD���
A.  B.
B.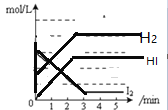
C.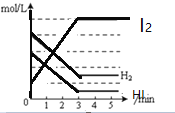 D.
D. 
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���u�Ǹ����c���٣����I(y��)������Ҫ�ɷ֞�FeWO4��MnWO4�ĺ��u�F�V�c���A����ұ���u���������£������f�������_���ǣ� ��
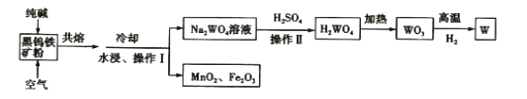
A.�����u�F�V�����Ŀ��������������
B.�����^���п՚������������Fe(II)��Mn(II)
C.����II���^�V��ϴ�졢���H2WO4�y����ˮ�Ҳ���(w��n)��
D.�ڸߜ���WO3��������W
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���h(hu��n)�����}�ѽ����҇����R���ش��}��
��![]() �p�ٶ�����̼���ŷ���һ���Ҫ�n�}���о�������
�p�ٶ�����̼���ŷ���һ���Ҫ�n�}���о�������![]() �����Ӛ�ɺϳɵ�̼����
�����Ӛ�ɺϳɵ�̼����![]() �N���W�I���I�������ʾ
�N���W�I���I�������ʾ
���W�I |
|
|
|
|
|
|
�I�� | 803 | 436 | 332 | 409 | 463 | 326 |
ͨ�^Ӌ��ó�![]() ______ ��
______ ��
![]() ��
��![]() �������]������Ͷ��
�������]������Ͷ��![]() ��
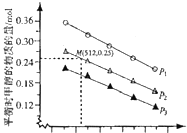
��![]() �l(f��)��ԓ���������y�ò�ͬ�ضȼ������£�ƽ��r���������|������D��ʾ��
�l(f��)��ԓ���������y�ò�ͬ�ضȼ������£�ƽ��r���������|������D��ʾ��
��������![]() ���ضȞ�512K�r����ԓ������Ͷ��
���ضȞ�512K�r����ԓ������Ͷ��![]() ��
��![]()
![]() ��2mol
��2mol![]() ��
��![]()
![]() �r��ƽ���� ______ �����Ƅӣ�
�r��ƽ���� ______ �����Ƅӣ�
![]() ��
��![]() ���՚�
���՚�![]() ����
����![]() ��KOH��Һ��ԭ�ϣ���ʯī��늘O��ֱ�Ә���ȼ��늳أ��tԓ늳ص�ؓ�O����ʽ�� ______ ����ԓ늳�늽�
��KOH��Һ��ԭ�ϣ���ʯī��늘O��ֱ�Ә���ȼ��늳أ��tԓ늳ص�ؓ�O����ʽ�� ______ ����ԓ늳�늽�![]()
![]() ��Һ����ȼ��늳����ʲr��56L�՚�r��Ӌ����Փ�σɘO늽�a�����w�Ŀ����|���� ______ ��
��Һ����ȼ��늳����ʲr��56L�՚�r��Ӌ����Փ�σɘO늽�a�����w�Ŀ����|���� ______ ��
��![]() Ҳ��һ�N�����Ⱦ������ú�ˮ̎����
Ҳ��һ�N�����Ⱦ������ú�ˮ̎����![]() �ďU�⣬��ˮ����Ҫ�x�ӵĺ������£�
�ďU�⣬��ˮ����Ҫ�x�ӵĺ������£�
�ɷ� | ���� | �ɷ� | ���� |
| 18980 |
| 400 |
| 10560 |
| 142 |
| 2560 |
| 1272 |
![]() ��ˮ������̎����߀����
��ˮ������̎����߀����![]() ��
��![]() ��
��![]() ��
��![]() �������м���ʯ�ҝ{ʹ��ˮ�е�
�������м���ʯ�ҝ{ʹ��ˮ�е�![]() �D�Q��
�D�Q��![]() ����
����![]() ���ó�����ȫ�r��
���ó�����ȫ�r��![]()
![]() �� ______
�� ______ ![]()
��֪![]()
![]()
![]() ̎���^�ďU����
̎���^�ďU����![]() �ĺ�������ͨ�^��������y�����õ���ԇ���У�
�ĺ�������ͨ�^��������y�����õ���ԇ���У�![]() �ĵ�˜���Һ��������Һ������̎����ďU����ÿ���
�ĵ�˜���Һ��������Һ������̎����ďU����ÿ���![]() �˛r��
�˛r��![]() ������ͨ�뵽100mL���е��۵ĵ�˜�Һ�У�tmin�_���ζ��K�c���ζ��K�c�ĬF(xi��n)��� ______ Ӌ��ԓ̎�����
������ͨ�뵽100mL���е��۵ĵ�˜�Һ�У�tmin�_���ζ��K�c���ζ��K�c�ĬF(xi��n)��� ______ Ӌ��ԓ̎�����![]() �ĺ��� ______
�ĺ��� ______ ![]() �ú�a��t��ʽ�ӱ�ʾ
�ú�a��t��ʽ�ӱ�ʾ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���״�����Ҫ�Ļ��W���I(y��)���Aԭ�Ϻ�Һ�wȼ�ϡ����I(y��)�Ͽ�����CO��CO2�����aȼ�ϼ״�����֪�״��Ƃ�����P���W�����Լ��ڲ�ͬ�ض��µĻ��W����ƽ�ⳣ��(sh��)���±���ʾ��
���W���� | ƽ�ⳣ��(sh��) | �ضȣ����� | |
500 | 800 | ||
��2H2(g)+CO(g) | K1 | 2��5 | 0��15 |
��H2(g)+CO2(g) | K2 | 1��0 | 2��50 |
��3H2(g)+ CO2(g) | K3 | ||
��1����������______�����������������ş�����������
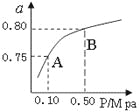
��2��ij�ض��·�������H2��ƽ���D���ʣ�a���c�wϵ������(P)���Pϵ��D��ʾ���tƽ���B(t��i)��A׃��B�r��ƽ�ⳣ��(sh��)K(A) K(B)������������������������������
��3���Д෴���ۡ�H______0�� ��S______0������>����=������<�������������c�����ƌ���K1��K2�cK3֮�g���Pϵ���tK3=__________����K1��K2��ʾ������500����2L�����]�����У��M�з��������y��ij�r��H2��CO2�� CH3OH��H2O�����|�����քe��6mol��2 mol��10 mol��10 mol���˕rv(��)______v(��)������>����=������<����
��4��һ���ض��£���3 L�ݷe��׃�����]�����аl(f��)������������֪c(CO)�c�����r�gt׃����������D��ʾ������t0�r�̷քe��׃һ���l����������׃?y��u)�����������������

��������׃?y��u)��������r����׃�ėl����___________________��
��������׃?y��u)��������r����׃�ėl����__________________��
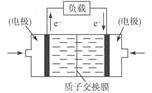
��5���״�ȼ��늳�ͨ�������K늘O���乤��ԭ����D��ʾ��ؓ�O��늘O�����飺______________________��
��6��һ���l���¼״��cһ����̼�������Ժϳ����ᡣͨ����r�£���0��2 mol/L�Ĵ����c0.1 mol/LBa(OH)2��Һ���w�e��ϣ��t�����Һ���x�ӝ���ɴ�С������_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����һ����1���⼰�仯�����ںϳɚ�������ˎ��ȷ�����ЏV����;���ش����І��}��Bodensteins�о������з�����2HI(g)![]() H2(g) + I2(g)����716K�r�����w������е⻯������|�����֔�(sh��)x(HI)�c�����r�gt���Pϵ���±���
H2(g) + I2(g)����716K�r�����w������е⻯������|�����֔�(sh��)x(HI)�c�����r�gt���Pϵ���±���
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
�ٸ����������Y����ԓ������ƽ�ⳣ��(sh��)K��Ӌ��ʽ�飺___________��
�����������У����������ʞ�v��= k����x2(HI)���淴�����ʞ�v��=k����x(H2)��x(I2)������k����k�������ʳ���(sh��)���tk����________(��K��k����ʾ)����k��= 0.0027min-1����t=40min�r��v��=________min-1��
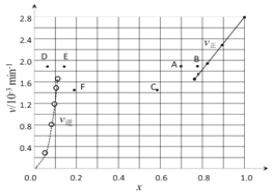
����������(sh��)��Ӌ��õ�v����x(HI)��v����x(H2)���Pϵ�����D��ʾ�������ߵ�ijһ�ضȕr�����������_��ƽ�⣬�������c�քe��_________________������ĸ����
�����������£���0.01 mol��L-1��Ba(OH)2��Һ200mL��0.01 mol��L-1��NaHSO4��Һ100mL��ϣ���������Һ��pHֵ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�������f�����_���ǣ� ��
A.��� SO2 ����Ư���ԣ���������ʹƷ�t��Һ����ˮ��KMnO4(H��)��ʯ����Һ��ɫ
B.�� 50 mL 18.4 mol/L H2SO4 ��Һ�м����������~Ƭ���ӟᣬ��ַ�����߀ԭ�� H2SO4�����|����С�� 0.46 mol
C.SO2��NO2 �� CO2 ���������������Ҫԭ������ˮ�� pH С�� 5.6
D.�� HNO3 �c���}�ᰴ 3��1 ���w�e�Ȼ�����õĻ�������ˮ�����ܽ����K
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���������H2߀ԭWO3�Ƃ����W���b����D��ʾ��Zn����������������s�|�����ԛ]ʳ������Һ���������������⣩�������f�����_����
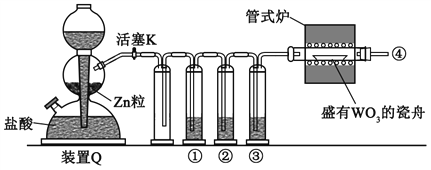
A. �١��ڡ���������ʢ�bKMnO4��Һ����H2SO4�����ԛ]ʳ������Һ
B. ��ʽ�t�ӟ�ǰ����ԇ���ڢ�̎�ռ����w���cȼ��ͨ�^���Д����w����
C. �Y�������r�����P�]����K����ֹͣ�ӟ�
D. �b��Q�����հl(f��)������Ҳ�����ڶ������i�c���}�ᷴ���Ƃ��Ț�
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com