
【題目】根據下表回答下列有關問題.
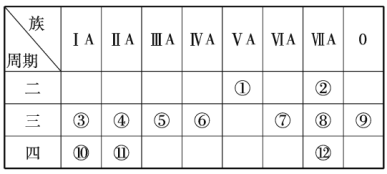
(1)寫出下列元素符號:①______,⑥______,⑦______,______.
(2)這些元素中最活潑的金屬元素是______(填元素符號,下同),最活潑的非金屬元素是______,最不活潑的元素是______.
(3)這些元素的最高價氧化物對應的水化物中酸性最強的是______(填化學式,下同),堿性最強的是______,呈兩性的氫氧化物是______,寫出三者之間兩兩反應的化學方程式:______;______;______.
(4)這些元素(除0族元素外)中原子半徑最小的是______(填元素符號,下同),原子半徑最大的是______.
(5)在③與④中,單質的化學性質較活潑的是______(填元素符號),怎樣用化學實驗證明?______在⑧與中,單質的化學性質較活潑的是____________(填元素符號),怎樣用化學實驗證明?_____________________.
【答案】N Si S Ca K F Ar ![]()
![]()
![]()
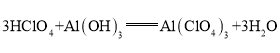
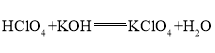
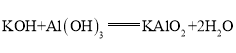 F K Na 將Na、Mg分別與冷水反應,
F K Na 將Na、Mg分別與冷水反應,![]() 跟冷水劇烈反應,放出氫氣,Mg跟冷水不反應 Cl
跟冷水劇烈反應,放出氫氣,Mg跟冷水不反應 Cl ![]() 將氯氣通入溴化鈉溶液中,溶液變為橙紅色,發生的反應為
將氯氣通入溴化鈉溶液中,溶液變為橙紅色,發生的反應為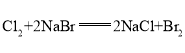
【解析】
根據元素在元素周期表中的位置,可知①~的具體元素,再結合元素周期律可知,最活潑的金屬元素是![]() ,最活潑的非金屬元素是
,最活潑的非金屬元素是![]() ,最不活潑的元素是稀有氣體元素
,最不活潑的元素是稀有氣體元素![]() ,它們的最高價氧化物對應的水化物中酸性最強的是
,它們的最高價氧化物對應的水化物中酸性最強的是![]() ,堿性最強的是
,堿性最強的是![]() ,呈兩性的氫氧化物是
,呈兩性的氫氧化物是![]() .在比較Na與
.在比較Na與![]() 、
、![]() 與
與![]() 的活潑性差異時,可根據元素金屬性、非金屬性強弱比較的依據設計實驗。
的活潑性差異時,可根據元素金屬性、非金屬性強弱比較的依據設計實驗。
(1)據上分析可知,四種元素的符號分別為:①N,⑥Si,⑦S,Ca;
(2)據上分析可知:最活潑的金屬元素是![]() ,最活潑的非金屬元素是
,最活潑的非金屬元素是![]() ,最不活潑的元素是稀有氣體元素
,最不活潑的元素是稀有氣體元素![]() ;
;
答案為:K; F;Ar;
(3)它們的最高價氧化物對應的水化物中酸性最強的是![]() ,堿性最強的是
,堿性最強的是![]() ,呈兩性的氫氧化物是
,呈兩性的氫氧化物是![]() ;氫氧化鋁夠與高氯酸、氫氧化鉀反應,均生成鹽和水,高氯酸與氫氧化鉀反應生成鹽和水,方程式分別為:
;氫氧化鋁夠與高氯酸、氫氧化鉀反應,均生成鹽和水,高氯酸與氫氧化鉀反應生成鹽和水,方程式分別為: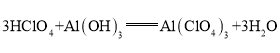 ,
,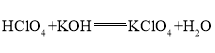 ,
,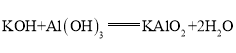 ;
;
答案為:![]() ;
; ![]() ;
;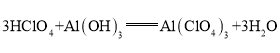 ;
;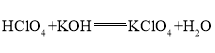 ;
;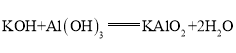 ;
;
(4)同周期從左到右原子半徑遞減,同主族從上到下原子半徑遞增,這些元素(除0族元素外)中原子半徑最小的是F,原子半徑最大的是K;
答案為:F;K;
(5)同周期從左到右金屬性遞減,化學性質Na>Mg,可通過與水反應放出氫氣的劇烈程度來比較,鈉與冷水劇烈反應,而鎂與冷水不反應;
答案為:Na,將Na、Mg分別與水反應,![]() 跟水劇烈反應,放出氫氣,鎂與冷水不反應;
跟水劇烈反應,放出氫氣,鎂與冷水不反應;
同主族從上到下非金屬性遞減,單質的化學性質![]() >
>![]() ,可通過氯氣能置換出溴來證明,氯氣與溴化鈉溶液反應,置換出溴,溶液顯橙色,方程式為:
,可通過氯氣能置換出溴來證明,氯氣與溴化鈉溶液反應,置換出溴,溶液顯橙色,方程式為: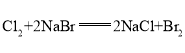 ;
;
答案為:Cl;將氯氣通入溴化鈉溶液中,溶液變為橙色,發生的反應為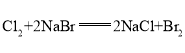 。
。


科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是
A.MgO(s)+C(s)=CO(g)+Mg(g)高溫下能自發進行,則該反應ΔH>0、ΔS>0
B.常溫下等物質的量濃度的CH3COOH溶液和HCl溶液中,水的電離程度相同
C.0.1 mol·L-1 NH4Cl溶液加水稀釋,![]() 的值增大
的值增大
D.對于反應2SO2+O22SO3,使用催化劑能加快反應速率并提高SO2的平衡轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以石油裂解得到的乙烯和 1,3-丁二烯為原料,經過下列反應合成高分子化合物 H,該物質可用于制造以玻璃纖維為填料的增強塑料(俗稱玻璃鋼)。

請按要求填空:
(1)寫出下列反應的反應類型:反應①____________ ,反應⑤ _______________,反應⑧_____________________
(2)反應②的化學方程式是 ____________________
(3) 反應③、④中有一反應是與 HCl 加成,該反應是__________(填反應編號),設計這一步反應的目的是_______________________,物質 C 的結構簡式是____________________ 。
(4)反應⑨的化學方程式是 _______________
(5)寫出與 G 具有相同種類和數目的官能團的同分異構體:_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鍺是重要的半導體材料,應用于航空航天測控、光纖通訊等領域.一種提純二氧化鍺粗品(主要含GeO2、As2O3)的工藝如下:
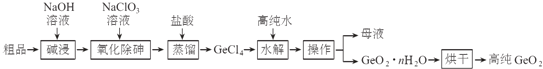
已知:①“堿浸”過程中的反應為:
GeO2+2NaOH=Na2GeO3+H2O
As2O3+2NaOH=2NaAsO2+H2O
②“蒸餾”過程中的反應為:Na2GeO3+6HCl=2NaCl+GeCl4+3H2O
③GeCl4的熔點為-49.5℃,AsCl3與GeCl4的沸點分別為130.2℃、84℃.
(1)鍺的原子序數為32,鍺在元素周期表中的位置為第 ______ 周期 ______ 族.
(2)“氧化除砷”的過程是將NaAsO2氧化為Na3AsO4,其反應方程式為: ______ .
(3)傳統的提純方法是將粗品直接加入鹽酸中蒸餾,其缺點是 ______ .
(4)工業上與蒸餾操作相關的設備有 ______
A.蒸餾釜 B.離心萃取機 C.冷凝塔 D.加壓過濾機
(5)“水解”操作時發生的化學反應方程式為 ______ ,“水解”操作時保持較低溫度有利于提高產率,其最可能的原因是 ______ (答一條即可).
(6)若1噸二氧化鍺粗品(含雜質30%)經提純得0.745噸的高純二氧化鍺產品,則雜質脫除率為 ______.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈷(Co)及其化合物在工業上廣泛應用于磁性材料、電池材料及超硬材料等領域。某學習小組欲從某工業廢料中回收鈷,設計工藝流程如下:(廢料中含有Al、Co2O3 和Fe2O3等物質)。
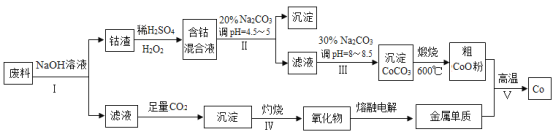
請回答:
(1)廢料用NaOH溶液處理前通常先將廢料粉碎,其目的是____________。
(2)過程Ⅱ用稀H2SO4和H2O2溶液與Co2O3反應而達到浸出鈷的目的,請寫出該反應的離子方程式___________。在實驗室模擬工業生產時,也可用鹽酸浸出鈷,但實際工業生產中不用鹽酸,請分析不用鹽酸浸出鈷的主要原因______________。
(3)碳酸鈉溶液在過程Ⅱ和Ⅲ中所起作用有所不同,請寫出碳酸鈉在過程Ⅱ中發生反應生成沉淀的離子方程式__________________________________。
(4) 若在實驗室中完成過程Ⅳ,則沉淀物需在__________________(填儀器名稱)中灼燒;寫出在過程Ⅴ中發生反應的化學方程式__________________________________。
(5)將1.0×10-3 mol/LCoSO4與1.2×10-3mol/L的Na2CO3等體積混合,此時溶液中的Co2+的濃度為__________ mol/L。(已知:CoCO3的溶度積為:Ksp=1.0×10-13)
(6)CoO與鹽酸反應可得粉紅色的CoCl2溶液。CoCl2晶體因結晶水數目不同而呈現不同顏色,利用藍色的無水CoCl2吸水變色這一性質可制成變色水泥和顯隱墨水。如圖是粉紅色的CoCl2·6H2O晶體在烘箱中受熱分解時,剩余固體質量隨溫度變化的曲線,物質A的化學式是____________________。
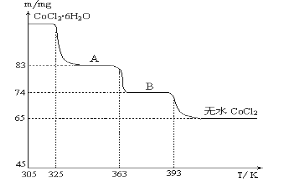
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】核內中子數為N的R2+,質量數為A,則ng它的同價態氧化物中所含電子物質的量為( )
A.![]() (A+N-10)molB.
(A+N-10)molB.![]() (A-N+6)mol
(A-N+6)mol
C.(A-N+2)molD.![]() (A-N+8)mol
(A-N+8)mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,將0.1 mol·L-1 NaOH溶液逐滴滴入10 mL 0.1 mol·L-1 NH4HSO4溶液中,溶液的pH與NaOH溶液體積關系如圖所示:
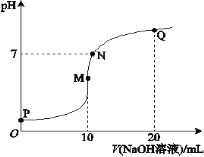
下列關系中,不正確的是
A.M點c(Na+)>c(![]() )
)
B.N點c(![]() )+c(Na+)=2c(
)+c(Na+)=2c(![]() -)
-)
C.Q點c(![]() )+c(NH3·H2O)=c(Na+)
)+c(NH3·H2O)=c(Na+)
D.M、N、Q三點中,水的電離程度M>N>Q
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示為從固體混合物中分離X的兩種方案,請根據方案1和方案2指出下列說法中合理的是( )

A. 可以選用方案1分離碳酸氫鈉中含有的氯化銨
B. 方案1中的殘留物應該具有的性質是受熱易揮發
C. 方案2中加入的試劑一定能夠與除X外的物質發生化學反應
D. 方案2中加入NaOH溶液可以分離出SiO2和Fe2O3混合物中的Fe2O3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉(Na2S2O3·5H2O)俗名“大蘇打”,又稱為“海波”。它易溶于水,難溶于乙醇,加熱、遇酸均易分解。某實驗室模擬工業硫化堿法制取硫代硫酸鈉,其反應裝置及所需試劑如下圖:
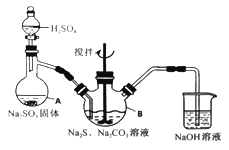
實驗具體操作步驟為:
①開啟分液漏斗,使硫酸慢慢滴下,適當調節分液的滴速,使反應產生的SO2氣體較均勻地通入Na2S和Na2CO3的混合溶液中,同時開啟電動攪拌器攪動,水浴加熱,微沸。
②直至析出的渾濁不再消失,并控制溶液的pH接近7時,停止通入SO2氣體。
……
(1)寫出儀器A的名稱_______。
(2)為了保證硫代硫酸鈉的產量,實驗中不能讓溶液pH <7,請用離子方程式解釋原因_________。
(3)寫出三頸燒瓶B中制取Na2S2O3,反應的總化學反應方程式________。
(4)從上述生成物混合液中獲得較高產率Na2S2O3·5H2O的步驟為

為減少產品的損失,操作①為趁熱過濾,“趁熱”的原因是______;操作②是______;操作①是抽濾、洗滌、干燥。
(5)測定產品純度
取6.00g產品,配制成100mL溶液。取10.00mL溶液,以淀粉溶液為指示劑,用濃度為0.500mol/LI2的標準溶液進行滴定,反應原理為2S2O32-+I2=S4O62-+2I-。相關數據記錄如下表所示。
編號 | 1 | 2 | 3 |
溶液的體積/mL | 10.00 | 10.00 | 10.00 |
消耗I2標準溶液的體積/mL | 19.98 | 22.50 | 20.02 |
滴定時,達到滴定終點的現象是___________。產品的純度為____________。
(6)Na2S2O3常用作脫氧劑,在溶液中易被Cl2氧化成SO42-,該反應的離子方程式為_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com