
【題目】下列有關化學鍵類型的敘述正確的是( )
A.全部由非金屬構成的化合物中肯定不存在離子鍵
B.所有物質中都存在化學鍵
C.已知乙炔的結構式為H—C≡C—H,則乙炔中存在2個σ鍵(C—H)和3個π鍵(C≡C)
D.乙烷分子中只存在σ鍵,不存在π鍵
科目:高中化學 來源: 題型:
【題目】反應Fe(s) +CO2 (g)![]() FeO(s)+CO(g),700℃時平衡常數為1.47,900℃時平衡常數為2.15。下列說法正確的是
FeO(s)+CO(g),700℃時平衡常數為1.47,900℃時平衡常數為2.15。下列說法正確的是
A. 升高溫度該反應的正反應速率增大,逆反應速率減小
B. 該反應的化學平衡常數表達式為K=![]()
C. 絕熱容器中進行該反應,溫度不再變化,則達到化學平衡狀態
D. 該反應的正反應是放熱反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】依據事實,按要求填空:
(1)在25℃、101kPa下,1mol乙醇燃燒生成CO2和液態水時放熱1269.6kJ.則表示乙醇燃燒熱的熱化學方程式為______.
(2)已知拆開1mol H﹣H鍵,1molN﹣H鍵,1molN≡N鍵分別需要的能量是436kJ、391kJ、946kJ,則N2(g)與H2(g)反應生成NH3(g)的熱化學方程式為______.
(3)已知:2SO2(g)+O2(g)═2SO3(g)△H=﹣196.6kJmol﹣1
2NO(g)+O2(g)═2NO2(g)△H=﹣113.0kJmol﹣1
則反應NO2(g)+SO2(g)═SO3(g)+NO(g)的△H=______kJmol﹣1.
(4)由氫氣和氧氣反應生成1mol水蒸氣放熱241.8kJ,寫出該反應的熱化學方程式:______.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示是Zn和Cu形成的原電池,某實驗興趣小組做完實驗后,在讀書卡上的記錄如下,則卡片上的描述合理的是
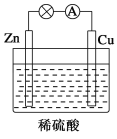

A. ①②③ B. ①②④ C. ②④ D. ③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)已知拆開1 mol H—H鍵、1 mol N—H鍵、1 mol N≡N鍵需要的能量分別是436 kJ、391 kJ、946 kJ,則N2與H2反應生成NH3的熱化學方程式為_________________。
(2)已知化學反應A2(g)+B2(g)===2AB(g)的能量變化如圖所示,回答下列問題:
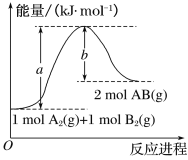
①該反應的ΔH_______0(填 “大于”“小于”或“等于”);
②反應物的總鍵能為______________;
③寫出該反應的熱化學方程式________________________________。
(3)聯氨(又稱肼,N2H4,無色液體)是一種應用廣泛的化工原料,可用作火箭燃料,回答下列問題:
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
寫出聯氨的結構式_______________,上述反應熱效應之間的關系式為ΔH4=__________,聯氨和N2O4可作為火箭推進劑的主要原因為_______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學小組采用類似制乙酸乙酯的裝置(如下圖),用環己醇制備環己烯。
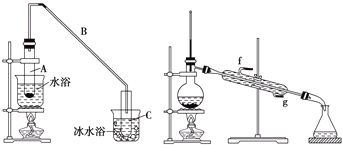
已知: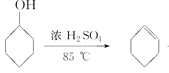 +H2O
+H2O
密度 | 熔點 | 沸點 | 溶解性 | |
環己醇 |
| 25 | 161 | 能溶于水 |
環己烯 |
|
| 83 | 難溶于水 |
(1)制備粗品
將12.5mL環己醇加入試管A中,再加入1mL濃硫酸,搖勻后放入碎瓷片(防止暴沸),緩慢加熱至反應完全,在試管C內得到環己烯粗品。
導管B除了導氣外還具有的作用是______。
②試管C置于冰水浴中的目的是______。
(2)制備精品
①環己烯粗品中含有環己醇和少量酸性雜質等![]() 加入飽和食鹽水,振蕩、靜置、分層,環己烯在______層(填“上”或“下”),分液后用______(填入編號)洗滌。
加入飽和食鹽水,振蕩、靜置、分層,環己烯在______層(填“上”或“下”),分液后用______(填入編號)洗滌。
A.KMnO4溶液![]() 稀H2SO4 C.Na2CO3溶液
稀H2SO4 C.Na2CO3溶液
②再將環己烯按上圖裝置蒸餾,冷卻水從______口進入![]() 填“g”或“f”),蒸餾時要加入生石灰,其目的是______。
填“g”或“f”),蒸餾時要加入生石灰,其目的是______。
③收集產品時,控制的溫應在______左右,實驗制得的環己烯精品質量低于理論產量,可能的原因是_____。
A.蒸餾時從![]() 開始收集產品
開始收集產品
B.環己醇實際用量多了
C.制備粗品時環己醇隨產品一起蒸出
(3)以下區分環己烯精品和粗品的方法,合理的是______。
A.分別加入酸性高錳酸鉀溶液
B.分別加入用金屬鈉
C.分別測定沸點
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應:2SO2+O2![]() 2SO3達到平衡狀態時,保持恒溫恒容向容器中加入一定量的O2。下列說法正確的是(K為平衡常數,Qc為濃度商)( )
2SO3達到平衡狀態時,保持恒溫恒容向容器中加入一定量的O2。下列說法正確的是(K為平衡常數,Qc為濃度商)( )
A. Qc不變,K變大,O2轉化率增大 B. Qc不變,K變大,SO2轉化率減小
C. Qc變小,K不變,O2轉化率減小 D. Qc增大,K不變,SO2轉化率增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有濃度為0.1mol·L-1的鹽酸、硫酸、醋酸三種溶液,試回答:
(1)三種溶液中c(H+)依次為a mol·L-1、b mol·L-1、cmol·L-1,大小順序為 ______。
(2)等體積的以上三種酸分別與過量的NaOH溶液反應,生成的鹽的物質的量依次為n1mol、n2mol、n3mol,它們的大小關系為 ______。
(3)中和等量NaOH溶液都生成正鹽時,分別需上述三種酸的體積依次是V1L、V2L、V3 L,其大小關系為 ______。
(4)與等量鋅反應時產生氫氣![]() 的速率分別為v1、v2、v3,其大小關系為 ______。
的速率分別為v1、v2、v3,其大小關系為 ______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com