
【題目】風靡全球的飲料果醋中含有蘋果酸(MLA),其分子式為C4H6O5。0.1mol蘋果酸與足量的NaHCO3溶液反應能產生4.48LCO2(標準狀況),蘋果酸脫水能生成使溴水褪色的產物。蘋果酸經聚合生成聚蘋果酸酯(PMLA)。
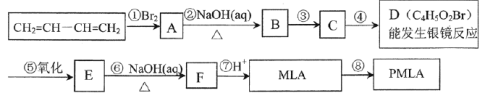
(1)寫出物質的結構簡式:A___,D___。
(2)指出合成路線中①、②的反應類型:①___;②___。
(3)寫出所有與MLA具有相同官能團的同分異構體的結構簡式:___。
(4)寫出E→F轉化的化學方程式___。
(5)上述轉化關系中步驟③和④的順序能否顛倒?___(填“能”或“不能”)。說明理由:___。
(6)請寫出以丙烯為原料制備乳酸(2-羥基丙酸)的合成路線流程圖(無機試劑任取)___。
【答案】CH2BrCH=CHCH2Br OHCCH2CHBrCHO 加成反應 取代(水解)反應 ![]() 、
、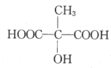 HOOCCH2CHBrCOOH+3NaOH→NaOOCCH2CH(OH)COONa+NaBr+2H2O 不能 若先氧化則B中碳碳雙鍵也被氧化
HOOCCH2CHBrCOOH+3NaOH→NaOOCCH2CH(OH)COONa+NaBr+2H2O 不能 若先氧化則B中碳碳雙鍵也被氧化 ![]()
【解析】
蘋果酸分子式為![]() ,
,![]() mol蘋果酸與足量
mol蘋果酸與足量![]() 溶液反應能產生
溶液反應能產生![]()
![]() 標準狀況
標準狀況![]() ,二氧化碳的物質的量為
,二氧化碳的物質的量為![]() ,則1mol蘋果酸含
,則1mol蘋果酸含![]() 蘋果酸脫水能生成使溴水褪色的產物,應含有1個
蘋果酸脫水能生成使溴水褪色的產物,應含有1個![]() ,結合蘋果酸的分子式知,蘋果酸的結構簡式為:
,結合蘋果酸的分子式知,蘋果酸的結構簡式為:![]() 。蘋果酸酯化反應進行的聚合生成聚蘋果酸
。蘋果酸酯化反應進行的聚合生成聚蘋果酸![]() ,其結構為
,其結構為![]() 。D被氧化生成E,則E中含有溴原子,E和氫氧化鈉的水溶液發生反應生成F,F酸化生成MLA,所以F的結構簡式為:
。D被氧化生成E,則E中含有溴原子,E和氫氧化鈉的水溶液發生反應生成F,F酸化生成MLA,所以F的結構簡式為:![]() ,E的結構簡式為:
,E的結構簡式為:![]() ,D能發生銀鏡反應則D中含有醛基,所以D的結構簡式為:
,D能發生銀鏡反應則D中含有醛基,所以D的結構簡式為:![]() ,根據1,
,根據1,![]() 丁二烯及D的結構簡式知,1,
丁二烯及D的結構簡式知,1,![]() 丁二烯和溴發生1,4加成生成A為
丁二烯和溴發生1,4加成生成A為![]() ,A和氫氧化鈉的水溶液發生取代反應生成B為
,A和氫氧化鈉的水溶液發生取代反應生成B為![]() ,B與HBr發生加成反應生成C,C的結構簡式為:
,B與HBr發生加成反應生成C,C的結構簡式為:![]() ,C再被氧化生成D,蘋果酸經聚合生成聚蘋果酸
,C再被氧化生成D,蘋果酸經聚合生成聚蘋果酸![]() ,據此解答。
,據此解答。
![]() 由上述分析可知,A為
由上述分析可知,A為![]() ,D為
,D為![]() ,故答案為:
,故答案為:![]() ;
;![]() ;
; ![]() 反應
反應![]() 是1,
是1,![]() 丁二烯和溴發生1,4加成生成
丁二烯和溴發生1,4加成生成![]() ,反應
,反應![]() 是
是![]() 和氫氧化鈉的水溶液發生取代反應生成
和氫氧化鈉的水溶液發生取代反應生成![]() ,故答案為:加成反應;取代反應;
,故答案為:加成反應;取代反應; ![]() 所有與MLA具有相同官能團的同分異構體的結構簡式有:
所有與MLA具有相同官能團的同分異構體的結構簡式有: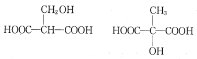 , 故答案為:
, 故答案為: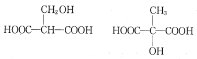 ;
; ![]() 轉化的化學方程式為:
轉化的化學方程式為:![]() ,故答案為:
,故答案為:![]() ;
; ![]() 順序不能顛倒,若先氧化則B中碳碳雙鍵也被氧化,故答案為:不能,若先氧化則B中碳碳雙鍵也被氧化;
順序不能顛倒,若先氧化則B中碳碳雙鍵也被氧化,故答案為:不能,若先氧化則B中碳碳雙鍵也被氧化;
(6) 丙烯和HOBr發生加成反應生成CH3CHBrCH2OH,CH3CHBrCH2OH發生氧化反應生成CH3CHBrCOOH,CH3CHBrCOOH和氫氧化鈉的水溶液加熱酸化得到CH3CHOHCOOH,故答案為:![]() 。
。


 星級口算天天練系列答案
星級口算天天練系列答案 芒果教輔達標測試卷系列答案
芒果教輔達標測試卷系列答案科目:高中化學 來源: 題型:
【題目】已知反應①:CO(g)+CuO(s) ![]() CO2(g)+Cu(s)和反應②:H2(g)+CuO(s)
CO2(g)+Cu(s)和反應②:H2(g)+CuO(s) ![]() Cu(s)+H2O(g)在相同的某溫度下的平衡常數分別為K1和K2,該溫度下反應③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某溫度下的平衡常數分別為K1和K2,該溫度下反應③:CO(g)+H2O(g) ![]() CO2(g)+H2(g)的平衡常數為K。則下列說法正確的是( )
CO2(g)+H2(g)的平衡常數為K。則下列說法正確的是( )
A.反應①的平衡常數K1=![]()
B.反應③的平衡常數K=![]()
C.對于反應③,恒容時,溫度升高,H2濃度減小,則該反應為吸熱反應
D.對于反應③,恒溫恒容下,增大壓強,H2濃度一定增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】500℃時,在四個體積為2L的恒容密閉容器中發生反應:NO2(g) + SO2(g)![]() SO3(g)+ NO(g)。有關物質起始時的物質的量數據如下表所示:
SO3(g)+ NO(g)。有關物質起始時的物質的量數據如下表所示:
容器 | 起始時物質的量/mol | |||
NO2 | SO2 | SO3 | NO | |
甲 | 0.1 | 0.1 | 0 | 0 |
乙 | 0.15 | 0.05 | 0.05 | 0.05 |
丙 | 0 | 0 | 0.2 | 0.2 |
丁 | 0.1 | 0.2 | 0 | 0 |
已知甲容器達到平衡時容器中c(SO3)=0.01mol·L-1。下列說法正確的是
A.升溫至700℃,上述反應的平衡常數為![]() ,則正反應為吸熱反應
,則正反應為吸熱反應
B.達平衡時,容器丙中c(SO2)是容器甲的2倍
C.達平衡時,容器丁中c(NO)與乙容器中相同
D.保持溫度不變容器甲達到平衡時再充入SO2(g)和SO3(g)各0.02mol,此時v(正)>v(逆)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用H2O2和H2SO4的混合溶液可腐蝕印刷電路板上的銅,其熱化學方程式為Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) ΔH
已知①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH1=64kJ·mol-1
②2H2O2(l)=2H2O(l)+O2(g) ΔH2=-196kJ·mol-1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=-286kJ·mol-1
O2(g)=H2O(l) ΔH3=-286kJ·mol-1
下列說法不正確的是( )
A.反應①可通過銅作電極電解稀的H2SO4方法實現
B.反應②在任何條件下都能自發進行
C.若H2(g)+![]() O2(g)=H2O(g) ΔH4,則ΔH4<ΔH3
O2(g)=H2O(g) ΔH4,則ΔH4<ΔH3
D.ΔH=-320kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮元素的化合物在工農業以及國防科技中用途廣泛,但也會對環境造成污染,如地下水中硝酸鹽造成的氮污染已成為一個世界性的環境問題。
(1)神舟載人飛船的火箭推進器中常用肼(N2H4)作燃料。NH3與NaClO反應可得到肼(N2H4),該反應中被氧化與被還原的元素的原子個數之比為___。如果反應中有5mol電子發生轉移,可得到___ g肼。
(2)常溫下向25mL0.01mol/L稀鹽酸中緩緩通入5.6mLNH3(標準狀況,溶液體積變化忽略不計),反應后溶液中離子濃度由大到小的順序是___。在通入NH3的過程中溶液的導電能力___(填寫“變大”、“變小”或“幾乎不變”)。
(3)向上述溶液中繼續通入NH3,該過程中離子濃度大小關系可能正確的是___(選填編號)。
a.[Cl-]=[NH4+]>[H+]=[OH-] b.[Cl-]>[NH4+]=[H+]>[OH-
c.[NH4+]>[OH-]>[Cl-]>[H+] d.[OH-]>[NH4+]>[H+]>[Cl-]
(4)常溫下向25mL含HCl0.01mol的溶液中滴加氨水至過量,該過程中水的電離平衡(填寫電離平衡移動情況)___。當滴加氨水到25mL時,測得溶液中水的電離度最大,則氨水的濃度為___mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗不能達到預期目的是( )
實驗操作 | 實驗目的 | |
A | 充滿NO2的密閉玻璃球分別浸泡在冷、熱水中 | 研究溫度對化學平衡移動的影響 |
B | 向盛有1mL硝酸銀溶液的試管中滴加NaCl溶液,至不再有沉淀,再向其中滴加Na2S溶液 | 說明一種沉淀能轉化為另一種溶解度更小的沉淀 |
C | 苯酚和水的濁液中,加少量濃碳酸鈉溶液 | 比較苯酚與碳酸氫鈉的酸性 |
D | 取少量溶液滴加Ca(OH)2溶液,觀察是否出現白色渾濁 | 確定NaHCO3溶液中是否混有Na2CO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 均是短周期元素,它們在元素周期表中的相對位置如圖所示,其中
均是短周期元素,它們在元素周期表中的相對位置如圖所示,其中![]() 與
與![]() 形成的一種化合物能使品紅溶液褪色,下列說法正確的是( )
形成的一種化合物能使品紅溶液褪色,下列說法正確的是( )

A.![]() 與
與![]() 形成的兩種常見化合物中含有的化學鍵類型全部相同
形成的兩種常見化合物中含有的化學鍵類型全部相同
B.可用![]() 溶液除去
溶液除去![]() 單質中混有的
單質中混有的![]() 單質
單質
C.簡單氫化物的熱穩定性:![]()
D.化合物![]() 和
和![]() 中,陽離子半徑均大于陰離子半徑
中,陽離子半徑均大于陰離子半徑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有兩種氣態單質![]() 和
和![]() ,已知
,已知![]() 和
和![]() 所含的原子個數相等,分子數之比為
所含的原子個數相等,分子數之比為![]() 。
。![]() 和
和![]() 的原子核內質子數都等于中子數,
的原子核內質子數都等于中子數,![]() 原子
原子![]() 層電子數是
層電子數是![]() 層的3倍。
層的3倍。
(1)![]() 、
、![]() 的元素符號分別為_______。
的元素符號分別為_______。
(2)![]() 中的
中的![]() 值為_______。
值為_______。
(3)![]() 的能層數目為_______。
的能層數目為_______。
(4)![]() 、
、![]() 形成的一種氣態化合物與水反應能生成由
形成的一種氣態化合物與水反應能生成由![]() 、
、![]() 形成的另一種氣態化合物,寫出該反應的化學方程式:_______。
形成的另一種氣態化合物,寫出該反應的化學方程式:_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是一個化學過程的示意圖,回答下列問題:
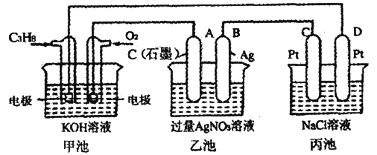
(1)甲池是___________裝置,電極B的名稱是___________。
(2)甲裝置中通入C3H8的電極反應____________,丙裝置中D極的產物是___________(寫化學式)。
(3)一段時間,當乙池中產生112 mL(標準狀況下)氣體時,均勻攪拌丙池,所得溶液在25℃時的pH=__________。(已知:NaCl溶液足量,電解后溶液體積為200 mL)。
(4)若要使乙池恢復電解前的狀態,應向乙池中加入__________(寫物質化學式)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com