
【題目】短周期元素X、Y、Z、W的原子序數依次增大,X原子在元素周期表中原子半徑最小,Y的次外層電子數是最外層的![]() ,ZX2是一種儲氫材料,W與Y屬于同一主族。下列敘述正確的是:
,ZX2是一種儲氫材料,W與Y屬于同一主族。下列敘述正確的是:
A. 原子半徑:rW>rZ>rY
B. 化合物X2Y、ZY、ZX2中化學鍵的類型相同
C. 由X、Y、Z、W組成的化合物的水溶液可能顯酸性
D. 由Y元素形成的離子與W元素形成的離子的電子數不可能相同
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】下列醛、酮的反應屬于還原反應的是( )
A.醛的銀鏡反應
B.醛在空氣中久置變質
C.由2-丁酮制備2-丁醇
D.乙醛與新制的氫氧化銅懸濁液加熱有磚紅色沉淀產生
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2014年5月7日,天津某工程檢測公司在進行探傷作業期間,一枚黃豆粒大小的放射源銥﹣192丟失,造成了嚴重的安全事故,圖示是銥在元素周期表中的信息,下列說法正確的是( ) 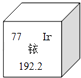
A.銥的相對原子質量為192.2克
B.銥原子核內的中子數為77
C.K2IrO3中Ir的化合價為+4
D.生活中常用的銥金筆為純凈的銥單質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏伽德羅常數的值,下列敘述正確的是( )
A. 11gT2O含有的電子數為5NA
B. 常溫下,0.2L 0.5molL﹣1NH4NO3溶液的氮原子數小于0.2NA
C. 含4molHCl的濃鹽酸與足量二氧化錳反應轉移的電子總數為NA
D. 標準狀況下,2.24L H2S全部溶于水所得溶液中HS﹣和S2﹣離子數之和為0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用A+、B﹣、C2﹣、D、E、F分別表示含有18個電子的幾種微粒(離子或分子),請回答下列問題:
(1)A元素是、B元素是、C元素是(用元素符號表示).
(2)D是由兩種元素組成的雙原子分子,用電子式表示其形成過程 .
(3)E是所有含18個電子的微粒中氧化能力最強的分子,其分子式是 , 其與水反應的化學方程式為 .
(4)F分子中含有4個原子,其電子式是或 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于電解池的敘述不正確的是( )
A.與電源正極相連的是電解池的陰極
B.與電源負極相連的是電解池的陰極
C.在電解池的陽極發生的是氧化反應
D.若用鐵做陰極,則鐵不會被氧化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】水中溶氧量(DO)是衡量水體自凈能力的一個指標,通常用每升水中溶解氧分子的質量表示,單位mg·L-1,我國《地表水環境質量標準》規定,生活飲用水源DO不能低于5mg/L。某化學小組同學設計了下列裝置(夾持裝置略),測定某河水DO。

Ⅰ.測定原理:
堿性條件下,O2將 Mn2+氧化為 MnO(OH)2;①2Mn2++O2+4OH-=2MnO(OH)2↓,酸性條件下,MnO(OH)2將I-氧化為I2;②MnO(OH)2+I-+H+→Mn2++I2+H2O(未配平),用Na2S2O3標準溶液滴定生成的I2,③2S2O32-+I2=S4O62-+2I-。
Ⅱ.測定步驟
a.安裝裝置,檢驗氣密性,充N2排盡空氣后,停止充N2.。
b.向燒瓶中加入200mL水樣。
c.向燒瓶中依次迅速加入1mL MnSO4無氧溶液(過量)2mL堿性KI無氧溶液(過量),開啟攪拌器,至反應①完全。
d.攪拌并向燒瓶中加入2mLH2SO4無氧溶液,至反應②完全,溶液為中性或弱酸性。
e.從燒瓶中取出40.00mL溶液,以淀粉作指示劑,用0.01000ml·L-1Na2SO3溶液進行滴定,記錄數據。
f.……
g.處理數據(忽略氧氣從水樣中的溢出量和加入試劑后水樣體積的變化)。
回答下列問題
(1)配制以上無氧溶液吋,除去所用溶劑水中氧的簡單操作為_____________。
(2)在橡膠塞處加入水樣及有關試劑應選擇的儀器為___________________。
①滴定管 ②注射器 ③量筒
(3)步驟f為_________________。
(4)步驟e中達到滴定終點的標志為__________________。若某次滴定消耗Na2S2O3溶液4.50mL,水樣的DO=________mg·L-1(保留一位小數)。若滴定開始時仰視滴定管刻度,滴定結束時俯視滴定管刻度,則所測的值_________(填:偏高、偏低、無影響)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com