
【題目】反應N2+O2![]() 2NO在恒容密閉容器中進行,達到平衡后,充入N2,下列說法正確的是
2NO在恒容密閉容器中進行,達到平衡后,充入N2,下列說法正確的是
A. 平衡向逆反應方向移動,N2和O2的轉化率都減小
B. 平衡向正反應方向移動,N2和O2的轉化率都增大
C. 壓強增大平衡不移動,N2的轉化率不變
D. 平衡向正反應方向移動,N2的轉化率減小,O2的轉化率增大
 寒假天地重慶出版社系列答案
寒假天地重慶出版社系列答案科目:高中化學 來源: 題型:
【題目】高鐵酸鈉(Na2FeO4)具有很強的氧化性,是一種新型的綠色凈水消毒劑。工業上可以通過次氯酸鈉氧化法制備高鐵酸鈉,生產過程如下:
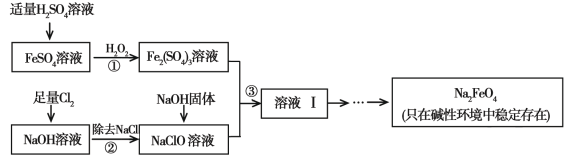
(1)高鐵酸鈉中鐵元素的化合價為 ,次氯酸鈉的電子式是________。
(2)步驟①反應的離子方程式是 。
(3)從溶液I中分離出Na2FeO4后,還有副產品Na2SO4 、NaCl,則步驟③中反應的離子方程式為 。
(4)工業上還可用電解濃NaOH溶液的方法制Na2FeO4,其工作原理如圖所示:
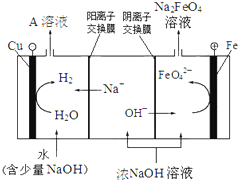
陽極的電極反應式為 。可循環使用的物質是 。
(5)計算Na2FeO4的消毒效率(以單位質量得到的電子數表示)約是氯氣的________倍,
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)已知:下列兩個熱化學方程式: Fe(s) + 1/2O2(g) ![]() FeO(s)
FeO(s) ![]() =-272.0KJ/mol,2Al(s) + 3/2O2(g)
=-272.0KJ/mol,2Al(s) + 3/2O2(g) ![]() Al2O3(s)
Al2O3(s) ![]() =-1675.7KJ/mol 則 Al(s)的單質和FeO(s)反應的熱化學方程式是____________________________。
=-1675.7KJ/mol 則 Al(s)的單質和FeO(s)反應的熱化學方程式是____________________________。
(2)對于下列反應:2SO2 + O2 ![]() 2SO3 , 如果2min內SO2的濃度由6 mol/L下降為2 mol/L,那么,用O2濃度變化來表示的反應速率為_____________。如果開始時SO2濃度為4mol/L,2min后反應達平衡,若這段時間內v(O2)為0.5mol/(L· min),那么2min時SO2的濃度為 。
2SO3 , 如果2min內SO2的濃度由6 mol/L下降為2 mol/L,那么,用O2濃度變化來表示的反應速率為_____________。如果開始時SO2濃度為4mol/L,2min后反應達平衡,若這段時間內v(O2)為0.5mol/(L· min),那么2min時SO2的濃度為 。
(3)如圖表示在密閉容器中反應:2SO2+O2![]() 2SO3+Q達到平衡時,由于條件改變而引起反應速度和化學平衡的變化情況,ab過程中改變的條件可能是 ;bc過程中改變的條件可能是 ;
2SO3+Q達到平衡時,由于條件改變而引起反應速度和化學平衡的變化情況,ab過程中改變的條件可能是 ;bc過程中改變的條件可能是 ;
(4)若增大壓強時,將反應速度變化情況畫在c—d處

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】右圖是溫度和壓強對反應:X+Y ![]() 2Z 影響的示意圖。圖中橫坐標表示溫度,縱坐標表示平衡混合氣體中Z的體積分數。下列敘述正確的是
2Z 影響的示意圖。圖中橫坐標表示溫度,縱坐標表示平衡混合氣體中Z的體積分數。下列敘述正確的是
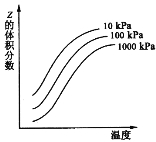
A.上述可逆反應的正反應為放熱反應
B.X、Y、Z均為氣態
C.X和Y只有一種為氣態,Z為氣態
D.上述反應的逆反應的△H>0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2017 年世界地球日我國的主題為“節約集約利用資源,倡導綠色簡約生活”。下列做法應提倡的是
A.夏天設定空調溫度盡可能的低
B.推廣使用一次性塑料袋和紙巾
C.少開私家車多乘公共交通工具
D.對商品進行豪華包裝促進銷售
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列陳述均正確且Ⅰ、Ⅱ兩者間有因果關系的是( )
選項 | 陳述Ⅰ | 陳述Ⅱ |
A | 工業合成氨的反應在高溫下進行 | N2+3H2 |
B | 明礬水溶液水解生成膠體 | 明礬可用于凈水 |
C | SiO2是酸性氧化物 | HF溶液不能用玻璃試劑瓶盛放 |
D | 氯的非金屬性比碘強 | 酸性:氫碘酸強于鹽酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關物質的分類正確的是
堿 | 酸 | 鹽 | 堿性氧化物 | 酸性氧化物 | |
A | NaOH | H2SO4 | BaCO3 | Al2O3 | CO2 |
B | KOH | HCl | NaCl | Na2O | CO |
C | NaOH | H2SO3 | CaCl2 | CuO | SO2 |
D | Na2CO3 | HNO3 | CaCO3 | MgO | SO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是( )
A.阿伏加德羅常數個硫酸分子里含有4molO B.CH4的摩爾質量為16g
C.lmolFe的質量為56g/mol D.lmolNH3為18克
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com