
【題目】某校化學學習小組利用如圖裝置來制取乙酸乙酯。
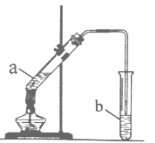
I.實驗過程:向試管a中加入碎瓷片,3mL乙醇,然后邊振蕩試管邊慢慢加入2mL濃硫酸,最后加入2mL乙酸,按圖連接好裝置,用酒精燈緩慢加熱,將產生的蒸汽經導管通到b試管中的液面上。
II. 已知化學方程式:CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
III.查閱資料得知:乙酸乙酯不溶于水,密度比水小,且有香味
請回答下列問題:
(1)試管a中加入碎瓷片,其作用是_____(填字母代號)。
A.加快化學反應速率 B.防止溶液暴沸
(2)試管b中的溶液是_____(填字母代號)。
A飽和碳酸鈉溶液 B.飽和氫氧化鈉溶液
(3)實驗完畢后,將b試管中的液體充分振蕩,靜置后,溶液分為兩層。
①乙酸乙酯在________(填“上層”或“下層”)。
②常用________操作將兩層液體分離(填“過濾”或“分液”)。
(4)實驗中加入乙酸的質量為2.1g,其中60%的乙酸發生酯化反應,則得到乙酸乙酯的質量為______g(計算結果保留兩位小數)。
【答案】B A 上層 分液 1.85
【解析】
根據實驗室制備乙酸乙酯的實驗原理及裝置分析解答;根據關系式計算產物的質量。
(1)液體乙酸乙醇沸點低,加熱要加碎瓷片,防止暴沸,故答案為:B;
(2)試管b中的溶液是飽和Na2CO3溶液,用于中和乙酸,溶解乙醇,降低乙酸乙酯在水中的溶解度,故答案為:A;
(3)實驗完畢后,將b試管中的液體充分振蕩,靜置后,溶液分為兩層,乙酸乙酯密度比水小,在上層,常用分液操作將兩層液體分離,故答案為:上層;分液;
(4)設得到的乙酸乙酯的物質的量為x,
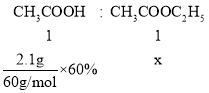
x=0.021mol,m(CH3COOC2H5)=0.021mol×88g/mol≈1.85g,即得到乙酸乙酯的質量為1.85g,故答案為:1.85。


 尖子生新課堂課時作業系列答案
尖子生新課堂課時作業系列答案科目:高中化學 來源: 題型:
【題目】在T℃條件下,向lL固定體積的密閉容器M中加入2molX和lmolY,發生如下反應:2X(g)+Y(g)![]() aZ(g)+W(g) ΔH=-QkJ·mol-1(Q>0)。當反應達到平衡后,放出的熱量為Q1kJ。若平衡后再升高溫度,混合氣體的平均相對分子質量減小。維持溫度T℃不變,若起始時向容器M中加入物質的物質的量如下,則反應達到平衡后放出的熱量仍為Q1kJ的是( )
aZ(g)+W(g) ΔH=-QkJ·mol-1(Q>0)。當反應達到平衡后,放出的熱量為Q1kJ。若平衡后再升高溫度,混合氣體的平均相對分子質量減小。維持溫度T℃不變,若起始時向容器M中加入物質的物質的量如下,則反應達到平衡后放出的熱量仍為Q1kJ的是( )
A.2molX、1molY、1molAr
B.amolZ、1molW
C.1molX、0.5molY、0.5amolZ、0.5molW
D.2molX、1molY、1molZ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組對人教版教材實驗“在200mL燒杯中放入20g蔗糖(C12H22O11),加入適量水,攪拌均勻,然后再加入15mL質量分數為98%濃硫酸,迅速攪拌”進行如下探究;
(1)觀察現象:蔗糖先變黃,再逐漸變黑,體積膨脹,形成疏松多孔的海綿狀黑色物質,同時聞到刺激性氣味,按壓此黑色物質時,感覺較硬,放在水中呈漂浮狀態,同學們由上述現象推測出下列結論:
①濃硫酸具有強氧化性 ②濃硫酸具有吸水性 ③濃硫酸具有脫水性④濃硫酸具有酸性 ⑤黑色物質具有強吸附性
其中依據不充分的是_________(填序號);
(2)為了驗證蔗糖與濃硫酸反應生成的氣態產物,同學們設計了如下裝置:

試回答下列問題:
①圖1的A中最好選用下列裝置_________(填編號);
②圖1的 B裝置所裝試劑是_________;D裝置中試劑的作用是_________;E裝置中發生的現象是_________;
③圖1的A裝置中使蔗糖先變黑的化學反應方程式為_________,后體積膨脹的化學方程式為:_________;
④某學生按圖2進行實驗時,發現D瓶品紅不褪色,E裝置中有氣體逸出,F裝置中酸性高錳酸鉀溶液顏色變淺,推測F裝置中酸性高錳酸鉀溶液顏色變淺的原因_________,其反應的離子方程式是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】標準狀況下15 g CO與CO2的混合氣體,體積為11.2 L。則:
(1)混合氣體的密度是_________。
(2)混合氣體的平均摩爾質量是_________。
(3)CO2和CO的體積之比是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下列圖示所得結論正確的是
A.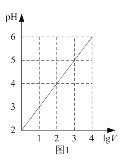 圖1表示1 LpH=2的某一元酸加水稀釋至V L,pH隨lgV的變化,說明該酸是弱酸
圖1表示1 LpH=2的某一元酸加水稀釋至V L,pH隨lgV的變化,說明該酸是弱酸
B.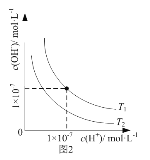 圖2表示不同溫度下水溶液中H+和OH-濃度的變化的曲線,說明圖中溫度T2>T1
圖2表示不同溫度下水溶液中H+和OH-濃度的變化的曲線,說明圖中溫度T2>T1
C.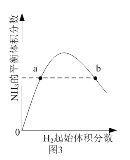 圖3表示一定條件下的合成氨反應中,NH3的平衡體積分數隨H2起始體積分數(N2的起始量恒定)的變化,說明圖中a點N2的轉化率小于b點
圖3表示一定條件下的合成氨反應中,NH3的平衡體積分數隨H2起始體積分數(N2的起始量恒定)的變化,說明圖中a點N2的轉化率小于b點
D.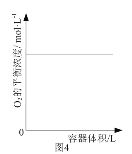 圖4表示同一溫度下,在不同容積的容器中進行反應2BaO2(s)
圖4表示同一溫度下,在不同容積的容器中進行反應2BaO2(s)![]() 2BaO(s)+O2(g), O2的平衡濃度與容器容積的關系,說明改變壓強平衡不發生移動
2BaO(s)+O2(g), O2的平衡濃度與容器容積的關系,說明改變壓強平衡不發生移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用如圖裝置(夾持裝置略)制備高效水處理劑高鐵酸鉀(K2FeO4)并探究其性質。
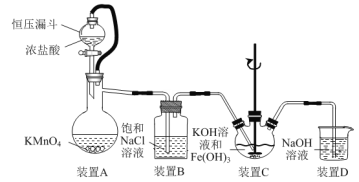
已知K2FeO4具有下列性質:①可溶于水,微溶于濃KOH溶液;②在0℃~5℃、強堿性溶液中比較穩定,在Fe(OH)3或Fe3+催化下發生分解;③在弱堿性至酸性條件下,能與水反應生成O2和Fe(OH)3(或Fe3+)。
(1)裝置A用于制取氯氣,其中使用恒壓漏斗的原因是____。
(2)為防止裝置C中K2FeO4分解,可以采取的措施是____和____。
(3)裝置C中生成K2FeO4反應的離子方程式為____。
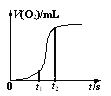
(4)用一定量的K2FeO4處理飲用水,測得產生O2的體積隨時間的變化曲線如圖所示。t1 s~t2 s內,O2的體積迅速增大的主要原因是____。
(5)驗證酸性條件下氧化性FeO42->Cl2的實驗方案為:取少量K2FeO4固體于試管中,____。(實驗中須使用的的試劑和用品有:濃鹽酸,NaOH溶液、淀粉KI試紙、棉花)
(6)根據K2FeO4的制備實驗得出:氧化性Cl2>FeO42-,而第(5)小題實驗表明,Cl2和FeO42-的氧化性強弱關系相反,原因是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】丙烷的分子結構可簡寫成鍵線式結構![]() ,有機物A的鍵線式結構為
,有機物A的鍵線式結構為![]() ,有機物B與等物質的量的H2發生加成反應可得到有機物A。下列有關說法錯誤的是( )
,有機物B與等物質的量的H2發生加成反應可得到有機物A。下列有關說法錯誤的是( )
A. 用系統命名法命名有機物A,名稱為2,2,3﹣三甲基戊烷
B. 有機物A的一氯取代物只有4種
C. 有機物A的分子式為C8H18
D. B的結構可能有3種,其中一種名稱為3,4,4﹣三甲基﹣2﹣戊烯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求回答下列問題。
(1)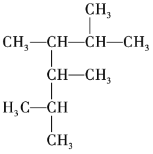 的名稱為______。
的名稱為______。
(2) 的名稱為______。
的名稱為______。
(3)3-甲基-2-戊烯的結構簡式為______。
(4)1,3,5-三甲基苯的結構簡式為______。
(5)某烷烴的相對分子質量為72,其一氯代物只有一種,該烷烴的結構簡式為______。
(6)2,3-二甲基-2-丁烯的鍵線式為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲硅烷廣泛用于電子工業、汽車領域,三氯氫硅(![]() )是制備甲硅烷的重要原料。回答下列問題:
)是制備甲硅烷的重要原料。回答下列問題:
(1)工業上以硅粉和氯化氫氣體為原料生產![]() 時伴隨發生的反應有:
時伴隨發生的反應有:
①![]()
②![]()
以硅粉和氯化氫氣體生產![]() 的熱化學方程式是_______________________。
的熱化學方程式是_______________________。
(2)工業上可用四氯化硅和氫化鋁鋰(![]() )制甲硅烷,反應后得甲硅烷及兩種鹽。該反應的化學方程式為_________________________________________________。
)制甲硅烷,反應后得甲硅烷及兩種鹽。該反應的化學方程式為_________________________________________________。
(3)三氯氫硅歧化也可制得甲硅烷。反應![]() 為歧化制甲硅烷過程的關鍵步驟,此反應采用一定量的
為歧化制甲硅烷過程的關鍵步驟,此反應采用一定量的![]() 催化劑,在不同反應溫度下測得
催化劑,在不同反應溫度下測得![]() 的轉化率隨時間的變化關系如圖所示。
的轉化率隨時間的變化關系如圖所示。
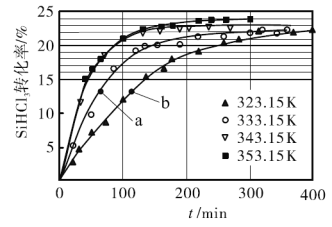
①![]() 時,平衡轉化率為_________。該反應是__________反應(填“放熱”或“吸熱”)。
時,平衡轉化率為_________。該反應是__________反應(填“放熱”或“吸熱”)。
②![]() 時,要縮短反應達到平衡的時間,可采取的措施有________________________。(答一種即可)
時,要縮短反應達到平衡的時間,可采取的措施有________________________。(答一種即可)
③比較a、b處反應速率的大小:![]() _______________
_______________![]() (填“>”“<”或“=”)。已知反應速率
(填“>”“<”或“=”)。已知反應速率![]() 分別是正、逆反應的速率常數,與反應溫度有關,x為物質的量分數,則在
分別是正、逆反應的速率常數,與反應溫度有關,x為物質的量分數,則在![]() 時
時![]() ___________(保留3位小數)。
___________(保留3位小數)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com