
下列溶液中微粒濃度關系一定正確的是
A.氨水和氯化銨的pH=7的混合溶液中:c(Cl-)=c(NH4+)
B.pH=1的一元酸和pH=13的一元堿等體積混合:c(OH-)=c(H+)
C.0.1mol·L-1的硫酸銨溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-)
D.0.1mol·L-1的硫化鈉溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案科目:高中化學 來源:2016-2017學年黑龍江大慶一中高二上11月月考化學卷(解析版) 題型:選擇題
常溫下,下列各組離子在指定溶液中一定能大量共存的是
A.0.1mol/L FeCl3溶液:K+、NH4+、SCN-、NO3-
B.0.1mol/LCu(NO3)2溶液:Na+、Mg2+、Cl-、SO42-
C.0.5mol/L AlCl3溶液:K+、Na+、S2-、SO42-
D.由水電離產生的c(H+)=10-13 mol·L-1的溶液:K +、Na+、HCO3-、Cl-
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高一上月考二化學卷(解析版) 題型:選擇題
下列關于電解質的理解中錯誤的是
A.電解質、非電解質都對化合物而言,單質不屬于此范疇
B.一種物質是不是電解質與其所處的狀態無關
C.在水溶液里或熔融狀態下,因其自身電離而導電的化合物叫做電解質
D.電解質在任何條件下都能導電
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高一上月考二化學卷(解析版) 題型:選擇題
已知下列分子或離子在酸性條件下都能氧化KI,自身發生如下變化:H2O2→H2O,IO3-→I2,MnO4-→Mn2+,HNO3→NO。如果分別用等物質的量的這些物質氧化足量的KI,得到I2最多的是
A.H2O2 B.IO3- C.MnO4- D.HNO3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高二上11月月考化學卷(解析版) 題型:填空題
已知:I2+2S2O32-=S4O62-+2I-。相關物質的溶度積常數見下表:
物質 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×10-29 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,為得到純凈的CuCl2﹒2H2O晶體,加入 調至pH=4,使溶液中的Fe3+轉化為Fe(OH)3沉淀,此時溶液中的c(Fe3+)= ;過濾后,將所得濾液低溫蒸發、濃縮結晶,可得到CuCl2﹒2H2O晶體。
(2)在空氣中直接加熱CuCl2﹒2H2O晶體得不到純的無水CuCl2,原因是 。(用化學方程式表示)。由CuCl2﹒2H2O晶體得到純的無水CuCl2的合理方法是 。
(3)某學習小組用“間接碘量法”測定含有CuCl2﹒2H2O晶體的試樣(不含能與I―發生反應的氧化性質雜質)的純度,過程如下:取0.36 g試樣溶于水,加入過量KI固體,充分反應,生成白色沉淀。用0.1000 mol·L-1Na2S2O3標準溶液滴定,到達滴定終點時,消耗Na2S2O3標準溶液20.00 mL。
①可選用 作滴定指示荊,滴定終點的現象是 。
②CuCl2溶液與KI反應的離子方程式為 。
③該試樣中CuCl2﹒2H2O的質量百分數為 。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高二上11月月考化學卷(解析版) 題型:選擇題
下列固體物質溶液水,再將其溶液加熱,蒸發結晶、再灼燒,能得到化學組成與原固體物質相同的是①膽礬 ②氯化鋁 ③硫酸鋁 ④NaHCO3 ⑤氯化銅
A.③④ B.①③④ C.①②③④ D.全部
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高二上11月月考化學卷(解析版) 題型:選擇題
常溫下,向0.1 mol·L-1的硫酸溶液中逐漸加入物質的量濃度相同的的氫氧化鋇溶液,生成沉淀的量與加入氫氧化鋇溶液的體積關系如圖所示,a、b、c、d分別表示實驗時不同階段的溶液,下列有關說法中不正確的是

A.溶液的pH:a<b<c<d B.溶液的導電能力:a>b>d>c
C.a、b溶液呈酸性 D.c、d溶液呈堿性
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上期中理化學卷(解析版) 題型:填空題
在25℃時,對于0.1mol·L-1的氨水,請回答以下問題。
(1)若向氨水中加入少量硫酸銨固體,此時溶液中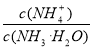 將_________(填“增大”、“減小”或“不變”);
將_________(填“增大”、“減小”或“不變”);
(2)若向氨水中加入pH=1的硫酸,且氨水與硫酸的體積比為1:1,此時溶液的pH_________7(填“>”、“<”或“=”),用離子方程式表示其原因______________,此時溶液中各離子濃度由大到小的順序為_______________。
(3)若向氨水中加入0.05mol•L-1稀硫酸至溶液正好呈中性,所用氨水的體積V1與稀硫酸的體積V2的關系為V1_________V2(填“大于”、“小于”或“等于”),寫出溶液中各離子濃度之間滿足的電荷守恒表達式______________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年新疆兵團二師華山中學高一期中化學卷(解析版) 題型:實驗題
用Na2CO3·10H2O晶體,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1) 應稱取Na2CO3·10H2O晶體的質量: 。
(2) 根據下列操 作對所配溶液的濃度產生的影響,完成下列要求:
作對所配溶液的濃度產生的影響,完成下列要求:
① Na2CO3·10H2O晶體失去了部分結晶水
② 用“左碼右物”的稱量方法稱量晶體(使用游碼)
③ 碳酸鈉晶體不純,其中混有氯化鈉
④ 稱量碳酸鈉晶體時所用砝碼生銹
⑤ 容量瓶未經干燥使用
⑥ 定容時俯視容量瓶刻度線
其中引起所配溶液濃度偏高的有 (填序號,下同),偏低的有 ,無影響的有 。
(3)下列操作中,容量瓶所不具備的功能有 。
A.配制一定體積準確濃度的標準溶液
B.貯存溶液
C.測量容量瓶規格以下的任意體積的液體
D.準確稀釋某一濃度的溶液
E.用來加熱溶解固體溶質
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com