
【題目】現有以下幾種有機物:
①![]() ②
②![]() ③
③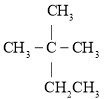 ④
④![]() ⑤
⑤![]()
⑥![]() ⑦
⑦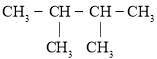 ⑧
⑧![]() ⑨
⑨ ![]()
請利用上述給出的物質按要求回答下列問題:
(1)③的系統命名是________。
(2)用“>”表示①③④⑧熔沸點高低順序:________(填序號)。
(3)與③互為同系物的是________(填序號)。
(4)⑨的一氯代物同分異構體數目有________種。
(5)在120℃,![]() 條件下,某種氣態烴與足量的
條件下,某種氣態烴與足量的![]() 完全反應后,測得反應前后氣體的體積沒有發生改變,則該烴是________(填序號)。
完全反應后,測得反應前后氣體的體積沒有發生改變,則該烴是________(填序號)。
(6)寫出⑥在鐵作催化劑的條件下與液溴發生取代反應的化學方程式________。
(7)②在加熱條件下和CuO反應的化學方程式________。
(8)②和⑤發生反應的化學方程式為________。
【答案】2,2-二甲基丁烷 ③>⑧>④>① ①④⑧ 4 ① ![]()
![]()
![]()
![]()
![]()
![]()
【解析】
(1)③先找主鏈,再從上邊開始編號。
(2)都為烷烴,碳原子數越多,熔沸點越高。
(3) ③為烷烴,①④⑧都為烷烴,分子式不相同。
(4)⑨(![]() )具有對稱性,有四種位置的氫。
)具有對稱性,有四種位置的氫。
(5)在120℃,![]() 條件下,某種氣態烴與足量的
條件下,某種氣態烴與足量的![]() 完全反應后,測得反應前后氣體的體積沒有發生改變,則氫原子數為4。
完全反應后,測得反應前后氣體的體積沒有發生改變,則氫原子數為4。
(6)苯在鐵作催化劑的條件下與液溴發生取代反應。
(7)乙醇在加熱條件下和CuO反應生成乙醛。
(8)乙醇和乙酸發生酯化反應。
(1)③先找主鏈,再從上邊開始編號,其系統命名是2,2-二甲基丁烷;故答案為:2,2-二甲基丁烷。
(2)都為烷烴,碳原子數越多,熔沸點越高,因此①③④⑧熔沸點高低順序:③>⑧>④>①;故答案為:③>⑧>④>①。
(3) ③為烷烴,①④⑥都為烷烴,分子式不相同,因此與③互為同系物的是①④⑥;故答案為:①④⑥。
(4)⑨(![]() )具有對稱性,有四種位置的氫,因此一氯代物同分異構體數目有4種;故答案為:4。
)具有對稱性,有四種位置的氫,因此一氯代物同分異構體數目有4種;故答案為:4。
(5)在120℃,![]() 條件下,某種氣態烴與足量的
條件下,某種氣態烴與足量的![]() 完全反應后,測得反應前后氣體的體積沒有發生改變,根據烴反應特點,當氫原子數為4的時候,燃燒后體積沒有改變,因此該烴是①;故答案為:①。
完全反應后,測得反應前后氣體的體積沒有發生改變,根據烴反應特點,當氫原子數為4的時候,燃燒后體積沒有改變,因此該烴是①;故答案為:①。
(6)苯在鐵作催化劑的條件下與液溴發生取代反應的化學方程式![]() ;故答案為:
;故答案為:![]() 。
。
(7)乙醇在加熱條件下和CuO反應的化學方程式![]() ;故答案為:
;故答案為:![]() 。
。
(8)乙醇和乙酸發生酯化反應的化學方程式為![]() ;故答案為:
;故答案為:![]() 。
。


 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案 名題訓練系列答案
名題訓練系列答案 期末集結號系列答案
期末集結號系列答案科目:高中化學 來源: 題型:
【題目】由碳、氫、氧3種元素組成的有機物A,相對分子質量為152,其分子中C、H原子個數比為1∶1,氧元素的質量分數為31.58%。A遇FeCl3溶液顯紫色,A能與NaHCO3溶液反應,其苯環上的一氯取代物有兩種,請回答下列問題:
(1)A的分子式是_______________________________。
(2)A的結構簡式為________________________________________。
(3)A可以發生如圖所示轉化關系,D的分子式為C10H12O3,A與C反應的化學方程式________。

(4)甲、乙兩裝置均可用作實驗室由C制取B的裝置,乙圖采用甘油浴加熱(甘油沸點290 ℃,熔點18.17 ℃),當甘油溫度達到反應溫度時,將盛有C和濃硫酸混合液的燒瓶放入甘油中,很快達到反應溫度。甲、乙兩裝置相比較,乙裝置有哪些優點________________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸是重要的化工生產原料,工業上常用硫鐵礦焙燒生成SO2,SO2氧化到SO3,再用98.3%左右的濃硫酸吸收SO3得到“發煙”硫酸(H2SO4·SO3)。最后用制得的“發煙”硫酸配制各種不同濃度的硫酸用于工業生產。
完成下列計算:
(1)1kg98%的濃硫酸吸收SO3后,可生產___kg“發煙”硫酸。
(2)“發煙”硫酸(H2SO4·SO3)溶于水,其中SO3都轉化為硫酸。若將890g“發煙”硫酸溶于水配成4.00L硫酸,該硫酸的物質的量濃度為___mol/L。
(3)硫鐵礦氧化焙燒的化學反應如下:3FeS2+8O2→Fe3O4+6SO24FeS2+11O2→2Fe2O3+8SO2
①1噸含FeS280%的硫鐵礦,理論上可生產多少噸98%的濃硫酸__?
②若24molFeS2完全反應耗用氧氣1467.2L(標準狀況),計算反應產物中Fe3O4與Fe2O3物質的量之比___。
(4)用硫化氫制取硫酸,既能充分利用資源又能保護環境,是一種很有發展前途的制備硫酸的方法。硫化氫與水蒸氣的混合氣體在空氣中完全燃燒,再經過催化氧化冷卻制得了98%的濃硫酸(整個過程中SO2損失2%,不補充水不損失水)求硫化氫在混合氣中的體積分數___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以環戊烷為原料制備環戊二烯的合成路線如圖,則下列說法正確的是( )
![]()
A. A的結構簡式是![]()
B. ①②的反應類型分別是取代、消去
C. 反應②③的條件分別是濃硫酸加熱、光照
D. 加入酸性KMnO4溶液,若溶液褪色則可證明![]() 已完全轉化為
已完全轉化為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碘在不同狀態下(固態或氣態)與氫氣反應的熱化學方程式如下所示:
①H2(g) + I2(?)![]() 2HI(g)+9.48kJ
2HI(g)+9.48kJ
②H2(g) + I2(?)![]() 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判斷正確的是
A.①中的I2為固態,②中的I2為氣態
B.②的反應物總能量比①的反應物總能量低
C.①的產物比反應②的產物熱穩定性更好
D.1mol 固態碘升華時將吸熱17kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A~F都是有機化合物,它們的轉化關系如下:
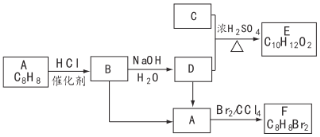
請回答下列問題:
(1)化合物C中含有官能團的名稱為________,A為一取代芳香烴,共面的碳原子最多有________個。
(2)D中含有一個甲基,由B生成D的化學方程式為________。
(3)由A生成B的反應類型為________。
(4)由B生成A的反應條件是________。
(5)E存在于梔子香油中,其結構簡式為________。
(5)在F的同分異構體中,苯環上一硝化產物只有一種,核磁共振有兩組峰且峰面積比為![]() 的是________(填結構簡式)。
的是________(填結構簡式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分子式為C5H10O2的有機物R在酸性條件下可水解為酸和醇,下列說法不正確的是
A.這些醇和酸重新組合可形成的酯共有40種
B.分子式與R相同的酸與足量堿石灰共熱,最多可得到2種烷烴
C.R水解得到的酸至少有5對共用電子對數目
D.R水解得到的醇發生消去反應,可得到4種烯烴
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸是一種重要的化工原料。接觸法生產的硫酸產品有98%的硫酸、20%的發煙硫酸(H2SO4和SO3的混合物,其中SO3的質量分數為0.2)。
完成下列計算:
(1)若不計生產過程的損耗,__________m3 SO2(折合成標準狀況)經充分轉化、吸收,可產出1噸 98%的硫酸(密度為1.84g/mL)。若98%的硫酸可表示為SO3![]() H2O,20%的發煙硫酸可表示為SO3aH2O,則a的值為 ___________(用分數表示)。
H2O,20%的發煙硫酸可表示為SO3aH2O,則a的值為 ___________(用分數表示)。
(2)鋁和鋁的化合物在社會生產和人類生活中也有著重要的作用。現有甲、乙兩瓶無色溶液,已知它們可能是Na[Al(OH)4]溶液和H2SO4溶液。現經實驗獲得如下數據:
(已知:2Na[Al(OH)4]+H2SO4→2Al(OH)3↓+Na2SO4+2H2O)
組別 | 甲(mL) | 乙(mL) | 沉淀的物質的量(mol) |
① | 140 | 10 | 0.02 |
② | 10 | 140 | 0.02 |
③ | 20 | 560 | 0.04 |
請通過必要的計算推斷過程回答:乙溶液中的溶質是什么________?其物質的量濃度為多少________?
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某稀硫酸和稀硝酸混合溶液100mL,逐漸加入鐵粉,產生氣體的量隨鐵粉加入量的變化如圖所示.下列說法錯誤的是( )

A.H2SO4濃度為4mol/L
B.溶液中最終溶質為FeSO4
C.原混合酸中NO3﹣濃度為0.2mol/L
D.AB段反應為:Fe+2Fe3+→3Fe2+
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com