

 NaClO+H2↑.電解結束后一段時間,有同學發現鐵電極表面變成紅褐色,則反應方程式為3NaClO+2Fe+3H2O=2Fe(OH)3↓+3NaCl.
NaClO+H2↑.電解結束后一段時間,有同學發現鐵電極表面變成紅褐色,則反應方程式為3NaClO+2Fe+3H2O=2Fe(OH)3↓+3NaCl. 分析 (1)N、P元素的大量排放,會導致水體的富營養化;
(2)氧氣的氧化性強于I2,故O2能將I-氧化為I2,氧氣被還原為OH-;
(3)根據溶液一定要呈電中性來分析;
(4)除去海水中Ca2+、SO42-分別用過量的Na2CO3溶液和BaCl2溶液,試劑的加入順序要滿足:盡量不引入新的雜質離子,如果雜質離子引入了,則一定要容易除去;
(5)①溶液A所在的極上有H2生成,則為陰極,根據電極反應來分析;左側電極為陽極,Cl-失電子發生氧化反應,據此分析;
②由圖二可知,是用惰性電極來電解NaCl溶液來制備NaClO溶液,即Cl-在陽極放電,H+在陰極放電,據此寫出電解方程式;鐵電極表面變成紅褐色,即有2Fe(OH)3沉淀生成,是鐵與呈弱堿性的NaClO溶液發生了氧化還原反應導致.
解答 解:(1)含磷洗滌劑的大量使用,會導致N、P元素的大量排放,造成水體的富營養化,引起藻類的瘋長,引發赤潮,故答案為:N,P;
(2)氧氣的氧化性強于I2,故O2能將I-氧化為I2,氧氣被還原為OH-,離子方程式為:4I-+O2+2H2O=2I2+4OH-,故答案為:4I-+O2+2H2O=2I2+4OH-;
(3)根據溶液一定要呈電中性,可知:c(Na+)+c(K+)+2c(Mg2+)=c(Cl-)+2c(SO42-),由于Na+、K+、Mg2+、Cl-均為0.02mol/L,故有:0.02mol/L+0.02mol/L+0.04mol/L=0.02mol/L+2c(SO42-),解得:c(SO42-)=0.03mol/L,故答案為:0.03;
(4)除去海水中Ca2+、SO42-分別用過量的Na2CO3溶液和BaCl2溶液(或Ba(OH)2),為了能除去過量的Ba2+,則Na2CO3溶液一定要在BaCl2或Ba(OH)2溶液之后加入;加入BaCl2或Ba(OH)2溶液后,會生成BaSO4沉淀,但此時不用先過濾,因為溶液中還有Ca2+和過量的Ba2+,加入Na2CO3溶液后,會又生成CaCO3和BaCO3沉淀,此時一并過濾除去即可,可節省實驗用品和時間,
故答案為:BaCl2溶液(或Ba(OH)2),加入稍過量的Na2CO3溶液不會使生成的BaSO4沉淀溶解,且一次性過濾可節省實驗用品和時間;
(5)①溶液A所在的極上有H2生成,則為陰極,電極上是來自于水的H+放電:2H2O+2e-=H2↑+2OH-,而中間為陽離子交換膜,Na+會從左側移動到右側,故溶液A為NaOH溶液;左側電極為陽極,Cl-失電子發生氧化反應,根據電解質溶液為中性溶液,則電極反應為:3H2O+Cl--6e-=ClO3-+6H+;故答案為:NaOH溶液,3H2O+Cl--6e-=ClO3-+6H+;
②由圖二可知,是用惰性電極來電解NaCl溶液來制備NaClO溶液,即Cl-在陽極放電:Cl--2e-+H2O=ClO-+2H+;H+在陰極放電:2H++2e-=H2↑,將陰陽極上放電的物質分別找到其來源后相加,即可得電解的化學方程式:NaCl+H2O NaClO+H2↑;鐵電極表面變成紅褐色,即有2Fe(OH)3沉淀生成,是鐵與呈弱堿性的NaClO溶液發生了氧化還原反應,鐵被氧化為氫氧化鐵,NaClO被還原為NaCl,反應為:3NaClO+2Fe+3H2O=2Fe(OH)3↓+3NaCl.
NaClO+H2↑;鐵電極表面變成紅褐色,即有2Fe(OH)3沉淀生成,是鐵與呈弱堿性的NaClO溶液發生了氧化還原反應,鐵被氧化為氫氧化鐵,NaClO被還原為NaCl,反應為:3NaClO+2Fe+3H2O=2Fe(OH)3↓+3NaCl.
故答案為:NaCl+H2O NaClO+H2↑;3NaClO+2Fe+3H2O=2Fe(OH)3↓+3NaCl.
NaClO+H2↑;3NaClO+2Fe+3H2O=2Fe(OH)3↓+3NaCl.
點評 本題考查了氧化還原反應的書寫、海水的除雜以及除雜試劑的加入順序和電極反應的書寫,綜合性較強,注意根據陰陽極反應來書寫電解總反應的方法.


科目:高中化學 來源: 題型:解答題
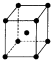 前四周期原子序數依次增大的六種元素A,B,D,X,Y,Z,基態時核外電子排布具有以下特征:A的電子層數和最外層電子數相等,非金屬元素B的已成對電子數是未成對電子數的2倍,且A和B位于不同周期;D和X的價電子層中未成對電子均只有1個,并且D-和X+的電子相差為8;Y、Z與X位于同一周期,它們價電子層中的未成對電子數分別為4和2,且原子序數相差為2.回答下列問題:
前四周期原子序數依次增大的六種元素A,B,D,X,Y,Z,基態時核外電子排布具有以下特征:A的電子層數和最外層電子數相等,非金屬元素B的已成對電子數是未成對電子數的2倍,且A和B位于不同周期;D和X的價電子層中未成對電子均只有1個,并且D-和X+的電子相差為8;Y、Z與X位于同一周期,它們價電子層中的未成對電子數分別為4和2,且原子序數相差為2.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 阿司匹林的分子式是:C9H8O4 | |
| B. | 阿司匹林可以通過鄰羥基苯甲酸與乙酸酯化反應制備,乙酸的用量應過量,可以提高鄰羥基苯甲酸的轉化率,同時也起到了溶劑的作用 | |
| C. | 原子經濟性反應指原料分子中的原子全部轉化成所需要的產物,不產生副產物,實現零排放,則阿司匹林制備符合原子經濟性 | |
| D. | 阿司匹林分子中所有碳原子可以共平面 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 油脂和蛋白質都是天然高分子化合物,都能水解 | |
| B. | 天然氣和液化石油氣的主要成分都是烴,都能燃燒 | |
| C. | 苯和乙烯都含有碳碳雙鍵,都能和H2發生加成反應 | |
| D. | 裂化汽油和四氯化碳都不溶于水,都可用于萃取溴 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
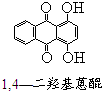 芳香族化合物A(C8H6O4)能與NaHCO3溶液反應生成CO2.由A與對二氯苯(
芳香族化合物A(C8H6O4)能與NaHCO3溶液反應生成CO2.由A與對二氯苯( )為原料經多步反應可合成1,4-二羥基蒽醌(結構如圖所示).
)為原料經多步反應可合成1,4-二羥基蒽醌(結構如圖所示). .
.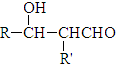 $\stackrel{△}{→}$
$\stackrel{△}{→}$
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 灼熱銅絲發生的現象變化為紫紅色與黑色交替出現,甲醇發生還原反應 | |
| B. | C中有機產物易溶于水,與水分子間只形成1種氫鍵 | |
| C. | 檢驗C中產物的試劑可用1 mol•L-1的CuS04溶液2 mL和O.4 mol•L-1的NaOH溶液4 mL混合得到 | |
| D. | 可用酸性高錳酸鉀溶液檢驗產物生成 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 甲 | 乙、丙、丁 |
| ① | 常見干燥劑 | 濃硫酸、石灰石、堿石灰 |
| ② | 常見合金 | 不銹鋼、青銅、生鐵 |
| ③ | 基本營養物質 | 蛋白質、維生素、糖類 |
| ④ | 腐蝕品 | 濃硫酸、燒堿、硝酸 |
| ⑤ | 堿性氧化物 | 過氧化鈉、氧化鎂、氧化鐵 |
| ⑥ | 弱電解質 | 醋酸、一水合氨、水 |
| A. | ①②③ | B. | ④⑤⑥ | C. | ②④⑥ | D. | ①⑤⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
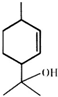
| A. | 松油醇的分子式為C10H16O | |
| B. | 1 mol松油醇與足量金屬鈉反應可生成標準狀況下的H2 22.4L | |
| C. | 可以用酸性高錳酸鉀溶液鑒別苯乙烯和松油醇 | |
| D. | 松油醇能發生加成反應、氧化反應、酯化等反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 防止“地溝油”重上餐桌的方法之一是將其制成生物柴油,在汽油中添加20%的生物柴油可減少50%的CO2、70%的SO2的排放,空氣毒性可降低90% | |
| B. | 北京市600個居住小區率先進行垃圾分類試點,以促進垃圾的綜合利用 | |
| C. | 減少CO2的方法有可將CO2制成干冰用于人工降雨、用石灰水吸收CO2、將CO2制成甲醇、種植樹木吸收CO2等 | |
| D. | 限制化學發展,關停化工企業,消除污染源頭 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com