
【題目】下列說法正確的是( )
A.明礬水解形成的Al(OH)3膠體能殺菌消毒,可用于水的凈化
B.對2HI(g)![]() H2(g)+I2(g)平衡體系增加壓強使顏色變深,能用勒夏特勒原理解釋
H2(g)+I2(g)平衡體系增加壓強使顏色變深,能用勒夏特勒原理解釋
C.pH=6的某溶液一定呈酸性
D.二次電池充電時,電池上標有“+”的電極應與外接電源的正極相連
【答案】D
【解析】
A. 明礬為KAl(SO4)212H2O,溶于水后Al3+水解生成Al(OH)3膠體;
B. 2HI(g)![]() H2(g)+I2(g)為等體積反應,改變壓強,平衡不移動;
H2(g)+I2(g)為等體積反應,改變壓強,平衡不移動;
C. 未標明溶液所處的溫度,不能確定溶液的酸堿性;
D. 二次電池充電時,電能轉化為化學能。
A. 明礬溶于水后Al3+水解生成Al(OH)3膠體,膠體具有吸附性,可用于水的凈化,A項錯誤;
B. 2HI(g)![]() H2(g)+I2(g)為等體積反應,改變壓強,平衡不移動,不能用勒夏特勒原理解釋,B項錯誤;
H2(g)+I2(g)為等體積反應,改變壓強,平衡不移動,不能用勒夏特勒原理解釋,B項錯誤;
C. 未標明溶液所處的溫度,pH=6的某溶液可能是酸性溶液,也可能是中性溶液或堿性溶液,C項錯誤;
D. 二次電池充電時,電能轉化為化學能,與電池上標有“+”的電極應與外接電源的正極相連,D項正確;
答案選D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】聚乙烯醇具有親水性和成膜性,在適宜的濃度下,能起類似人工淚液的作用,作為潤滑劑預防或治療眼部刺激癥狀。聚乙烯醇生產過程中會產生大量副產物乙酸甲酯,其催化醇解反應可用于制備甲醇和乙酸己酯,該反應的化學方程式為:CH3COOCH3(l)+C6H13OH(l)![]() CH3COOC6H13(l)+CH3OH(l),已知v正=k正x(CH3COOCH3)x(C6H13OH),v逆=k逆x(CH3COOC6H13)x(CH3OH),其中v正、v逆為正、逆反應速率,k正、k逆為速率常數,x為各組分的物質的量分數。
CH3COOC6H13(l)+CH3OH(l),已知v正=k正x(CH3COOCH3)x(C6H13OH),v逆=k逆x(CH3COOC6H13)x(CH3OH),其中v正、v逆為正、逆反應速率,k正、k逆為速率常數,x為各組分的物質的量分數。
(1)“洗衣凝珠”是由一層薄膜包裹洗衣液制成的新型洗滌產品,該薄膜的主要化學成分是可溶于水的聚乙烯醇(簡稱PVA)塑料,聚乙烯醇的化學式為(C2H4O)n,試回答:聚乙烯醇屬于_____(填“金屬材料”、“有機合成材料”、“硅酸鹽材料”、“復合材料”之一),從物質結構的角度解釋聚乙烯醇具有親水性的原因___________________________。
(2)343K時,乙酸甲酯和己醇按物質的量之比1:1、1:2和2:1進行初始投料。則達到平衡后,初始投料比____時,乙酸甲酯轉化率最大;與按1:2投料相比,按2:1投料時化學平衡常數Kx___(填增大、減小或不變)。
(3)反應開始時,已醇和乙酸甲酯按物質的量之比1:1投料,測得348K、343K、338K三個溫度下乙酸甲酯轉化率(α)隨時間(t)的變化關系如圖所示。

該醇解反應的ΔH____0(填>或<)。348K時,以物質的量分數表示的化學平衡常數Kx=____(保留2位有效數字)。A、B、C、D四點中,v逆最大的是___,v正最大的是____。
(4)該醇解反應使用離子交換樹脂作催化劑,下列關于該催化劑的說法正確的是____。
a.參與了醇解反應,但并不改變反應歷程 b.提高乙酸甲酯的平衡轉化率
c.提高了醇解反應的活化能 d.使k正和k逆增大相同倍數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2L甲醛氣體與xL的氧氣混合點燃,反應后甲醛和氧氣均無剩余,生成的混合氣體的體積為aL(氣體體積均在120°C,101kPa時測定),并將此aL混合氣體通過足量的堿石灰后,測得剩余氣體的體積為bL。若a-b=3.5,則x的值為
A. 2B. 4C. 1.75D. 3.5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鹵族元素的單質和化合物很多,我們可以利用所學物質結構與性質的相關知識去認識和理解它們。
(1)鹵族元素位于元素周期表的__________________區;溴的價電子排布式為______________________。
(2)在一定濃度的溶液中,氫氟酸是以二分子締合(HF)2 形式存在的。使氫氟酸分子締合的作用力是____________________。
(3)請根據下表提供的第一電離能數據判斷,最有可能生成較穩定的單核陽離子的鹵素原子是____________________(寫出 名稱)。
氟 | 氯 | 溴 | 碘 | |
第一電離能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的結構分別如圖 a、b 所示:
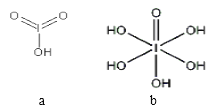
請比較二者酸性強弱:HIO3______________________H5IO6(填“>”、 “<”或“=”)。
(5)已知 ClO2-為 V 形,中心氯原子周圍有四對價層電子。 ClO2-中心氯原子的雜化軌道類型為___________________,寫 出一個 ClO2-的等電子體______________________。
(6)如圖為碘晶體晶胞結構。有關說法中正確的是______________________。
A.碘分子的排列有 2 種不同的取向,2 種取向不同的碘分子 以 4 配位數交替配位形成層結構
B.用均攤法可知平均每個晶胞中有 4 個碘原子
C.碘晶體中微粒(碘分子)的堆積為最密堆積
D.碘晶體中存在的相互作用有非極性鍵和范德華力
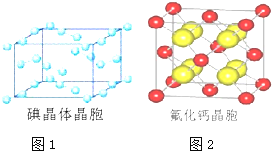
(7)已知 CaF2 晶體(見圖)的密度為ρg/cm3,NA 為阿伏加德羅常數,棱上相鄰的兩個 Ca2+ 的核間距為 a cm, 則 CaF2 的相對分子質量可以表示為__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿式碳酸銅可用于有機催化劑、殺蟲劑及飼料中銅的添加劑,還可用于煙火和顏料制造。CuSO4 溶液與Na2CO3 溶液反應能否得到堿式碳酸銅?某班同學進行相關探究。
(沉淀制備)稱取 12.5 g 膽礬溶于 87.4 mL 蒸餾水中,滴 4 滴稀硫酸,充分攪拌后得到 CuSO4 溶液。向其中加入適 量 Na2CO3 溶液,將所得藍綠色懸濁液過濾,用蒸餾水洗滌,再用無水乙醇洗滌。
(1)滴加稀硫酸的作用是______________________。所得硫酸銅溶液的溶質質量分數約 為______________________。
(2)用無水乙醇洗滌的目的是______________________。
(實驗探究)同學們設計了如下裝置,用制得的藍綠色固體進行實驗:
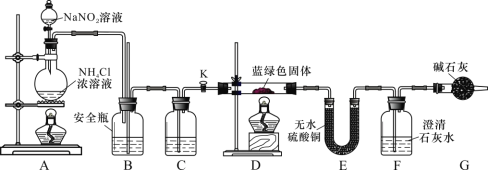
(3)D 裝置加熱前,需要首先打開活塞 K,用 A 裝置制取適量 N2,然后關閉 K,點燃 D 處酒精燈。A 中產生N2 的作用是______________________,C 中盛裝的試劑應是______________________。
(4)裝置 A 中發生反應的離子方程式為______________________。
(5)若藍綠色固體的組成為 xCuCO3·yCu(OH)2,實驗能觀察到的現象是_______________________________________。
(6)同學們查閱文獻知:Ksp[CaCO3]=2.8×10-9,Ksp[BaCO3]=5.1×10-9,經討論認為需要用 Ba(OH)2 代替 Ca(OH)2來定量測定藍綠色固體的化學式,其原因是 ______________。
a.Ba(OH)2 的堿性比 Ca(OH)2 強
b.Ba(OH)2 溶解度大于 Ca(OH)2,能充分吸收 CO2;
c.相同條件下,CaCO3 的溶解度明顯大于 BaCO3
d.吸收等量 CO2 生成的 BaCO3 的質量大于 CaCO3,測量誤差小
待 D 中反應完全后,打開活塞 K,再次滴加 NaNO2 溶液產生 N2,其目的是 ________________________________________。若定量分析所取藍綠色固體質量為 27.1 g,裝置 F 中使用 Ba(OH)2 溶液,實驗結束后, 裝置 E 的質量增加 2.7 g,F 中產生沉淀 19.7 g。則該藍綠色固體的化學式為 ____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組在家中進行化學實驗,按照圖A連接好線路發現燈泡不亮,按照圖B連接好線路發現燈泡亮.
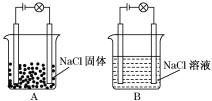
依據上述現象判斷或回答下列問題:
(1)NaCl屬于________(“酸”、“堿”或“鹽”),因為__________________________.
(2)NaCl固體________(填“能”或“不能”)導電,原因是_____________________.
(3)NaCl溶液________(填“能”或“不能”)導電,原因是__________________.
(4)在NaCl固體、NaCl溶液中屬于電解質的是_________________________________,
原因是____________________________________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用固體表面催化工藝進行NO分解的過程如下圖所示。
![]()
下列說法不正確的是
A.NO屬于共價化合物
B.O2含有非極性共價鍵
C.過程②吸收能量,過程③釋放能量
D.標準狀況下,NO分解生成11.2LN2轉移電子數為6.02×1023
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫時,向20mL 0.1 mol/L的CH3COOH溶液中逐滴滴加0.1 mol/L的NaOH溶液,滴入NaOH溶液的體積與溶液pH的變化如圖所示。下列說法正確的是
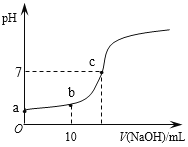
A. a點的pH=1
B. b點時,c (CH3COO—)=0.05mol/L
C. c點時,V(NaOH)=20mL
D. 反應過程中![]() 的值不斷增大
的值不斷增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】α1和α2,c1和c2分別為兩個恒容容器中平衡體系N2O4(g)![]() 2NO2(g)和3O2(g)
2NO2(g)和3O2(g)![]() 2O3(g)的反應物轉化率及反應物的平衡濃度,在溫度不變的情況下,均增加反應物的物質的量,下列判斷正確的是
2O3(g)的反應物轉化率及反應物的平衡濃度,在溫度不變的情況下,均增加反應物的物質的量,下列判斷正確的是
A. α1、α2均減小,c1、c2均增大
B. α1、α2均增大,c1、c2均減小
C. α1減小,α2增大,c1、c2均增大
D. α1減小,α2增大,c1增大,c2減小
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com