
【題目】如何除去雜質(zhì)、提純下列各物質(zhì)?請在表中填空。
混合物成分 | 提純所用試劑的化學式 | 離子方程式 |
(1)FeCl2中含少量FeCl3雜質(zhì) | _______ | __________________ |
(2)FeCl3中含少量FeCl2雜質(zhì) | _______ | __________________ |
(3)FeSO4中含少量CuSO4雜質(zhì) | _______ | __________________ |
【答案】Fe Fe+2Fe3+![]() 3Fe2+ Cl2 2Fe2++Cl2
3Fe2+ Cl2 2Fe2++Cl2![]() 2Fe3++2Cl- Fe Fe+Cu2+
2Fe3++2Cl- Fe Fe+Cu2+![]() Cu+Fe2+
Cu+Fe2+
【解析】
(1)FeCl2中含少量FeCl3雜質(zhì),利用Fe3+的氧化性,不能引入新的雜質(zhì),所以選用的還原劑是Fe,發(fā)生的反應為:Fe+2Fe3+![]() 3Fe2+,答案為:Fe;Fe+2Fe3+
3Fe2+,答案為:Fe;Fe+2Fe3+![]() 3Fe2+;
3Fe2+;
(2)FeCl3中含少量FeCl2雜質(zhì),利用Fe2+的還原性將FeCl2除去,不能引入新的雜質(zhì),選用的氧化劑為Cl2,發(fā)生的反應為:2Fe2++Cl2![]() 2Fe3++2Cl-,答案為:Cl2;2Fe2++Cl2
2Fe3++2Cl-,答案為:Cl2;2Fe2++Cl2![]() 2Fe3++2Cl-;
2Fe3++2Cl-;
(3)FeSO4中含少量CuSO4雜質(zhì),利用Cu2+氧化性,加入鐵粉,發(fā)生的反應為:Fe+Cu2+![]() Cu+Fe2+,再過濾,即可除去,答案為: Fe;Fe+Cu2+
Cu+Fe2+,再過濾,即可除去,答案為: Fe;Fe+Cu2+![]() Cu+Fe2+。
Cu+Fe2+。


 怎樣學好牛津英語系列答案
怎樣學好牛津英語系列答案科目:高中化學 來源: 題型:
【題目】甲酸(HCOOH)是還原性弱酸,常用于橡膠、醫(yī)藥等工業(yè)生產(chǎn),也可用于制備重要的化工原料[Cu(HCOO)2·4H2O]。
I.堿式碳酸銅的制備
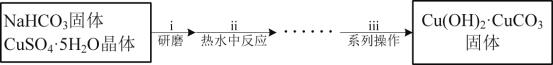
(1)“操作i”中研磨的目的是__。
(2)“操作ii”發(fā)生的反應是:2CuSO4+4NaHCO3═Cu(OH)2·CuCO3↓+3CO2↑+2Na2SO4+H2O。原料中NaHCO3必須過量的原因是__。反應溫度低于80℃的原因是__。
(3)“操作iii”中系列操作包括過濾、__、干燥。
II.甲酸的制備
(4)一定條件下,CO能與NaOH固體發(fā)生反應:CO+NaOH![]() HCOONa,再將HCOONa酸化,即可得HCOOH。
HCOONa,再將HCOONa酸化,即可得HCOOH。
①為了證明“CO與NaOH固體發(fā)生了反應”,甲同學設計下列驗證方案:取少許固體產(chǎn)物,配成溶液,在常溫下測其pH,若pH>7,則得證。該方案是否可行__(填“是”或“否”),請簡述你的理由:__。
②乙同學設計了另一個定性驗證方案:取固體產(chǎn)物,配成溶液,__(請補充完整)。
III.甲酸銅的合成及純度測定
(5)實驗室按Cu(OH)2·CuCO3+4HCOOH+5H2O═2Cu(HCOO)2·4H2O+CO2↑反應制得甲酸銅晶體,按以下步驟測定其純度。
步驟一:準確稱取mg甲酸銅晶體樣品,配成250mL溶液;
步驟二:移取25.00mL溶液于錐形瓶中,往溶液中加入足量KI搖勻,用cmol/LNa2S2O3溶液滴定至溶液變淺黃色時,加入10mL10%KSCN試劑,并加幾滴淀粉溶液,繼續(xù)用cmol/LNa2S2O3溶液滴定至終點,共消耗Na2S2O3溶液V1mL。
步驟三:用25.00mL蒸餾水代替甲酸銅溶液,重復步驟二,消耗Na2S2O3溶液V2mL;
已知:CuI難溶于水,能吸附I2;2Cu2++4I-=2CuI↓+I2;I2+2![]() =
=![]() +2I-;CuI(s)+SCN-(aq)
+2I-;CuI(s)+SCN-(aq)![]() CuSCN(s)+I-(aq)
CuSCN(s)+I-(aq)
①配制溶液時用到的玻璃儀器有:燒杯、量筒、玻璃棒和__;
②實驗中加入10mL10%KSCN試劑的目的是__。
③甲酸銅晶體的純度__(列表達式即可,Cu(HCOO)2·4H2O的摩爾質(zhì)量為226g/mol)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】a、b、c、d、e、f、g為七種由短周期元素構(gòu)成的粒子,它們都有10個電子,其結(jié)構(gòu)特點如下所示:(單位:電荷)
粒子代號 | a | b | c | d | e | f | g |
電荷數(shù) | 0 | +1 | -1 | 0 | +2 | +1 | 0 |
其中b的離子半徑大于e的離子半徑;c與f可形成兩個共價型g分子。試寫出:
(1)a粒子的原子結(jié)構(gòu)示意圖是______________。
(2)b與e相應元素的最高價氧化物對應水化物的堿性強弱比較為________(用化學式表示)。
(3)若d極易溶于水,在水溶液中變化的方程式為________,實驗室制備d氣體的化學方程式為________;若d為正四面體形分子,其重要應用之一為________。
(4)c粒子是________,f粒子是________(用化學式表示),由c、f生成g的離子方程式是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關(guān)于物質(zhì)性質(zhì)的敘述正確的是( )
A.SiO2與濃鹽酸在高溫下能反應生成SiCl4
B.木炭與濃硫酸共熱可生成CO2
C.明礬溶液中加入過量NaOH溶液可制備Al(OH)3膠體
D.向飽和食鹽水中通入足量CO2可制得NaHCO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是( )
A.室溫下,pH=3的CH3COOH溶液與pH=11的NaOH溶液等體積混合,所得溶液pH>7
B.室溫下,Na2CO3溶液中加入少量Ca(OH)2固體,溶液中![]() 的值增大
的值增大
C.在外加電流的陰極保護法中,須將被保護的鋼鐵設備與直流電源的負極相連
D.反應NH3(g)+HCl(g)=NH4Cl(s)在室溫下能自發(fā)進行,該反應的ΔH>0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有甲乙兩位同學均想利用原電池反應檢測金屬的活動性順序,兩人均使用鎂片和鋁片作電極,但甲同學將電極放入 6mol/L 的硫酸溶液,乙同學將電極放入 6mol/L 的氫氧化鈉溶液中,如圖所示:
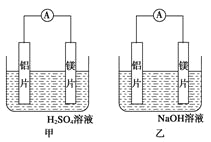
(1)寫出甲電池中正極的電極反應式___________________ ;
(2)寫出乙池中負極的電極反應式: 負極:_____ 總反應的離子方程式:_________
(3)如果甲與乙同學均認為“構(gòu)成原電池的電極材料如果都是金 屬,則構(gòu)成負極材料的金屬活潑
,則甲會判斷出_____活動性更強,而乙會判斷出_____活動性更強(填名稱)
(4)由此實驗,可得到如下哪些正確結(jié)論(_____)
a. 利用原電池反應判斷金屬活動性順序時應注意選擇合適的介質(zhì)
b. 鎂的金屬性不一定比鋁的強
c. 該實驗說明金屬活動性順序表已過時,已沒有利用價值
d. 該實驗說明化學研究對象復雜,反應受條件影響較大,因此應具體問題具體分析
(5)上述實驗也反過來證明了“直接利用金屬活動性順序表判斷原電池中的正負極”這種做法__填 “可靠”或“不可靠”)。如不可靠,請你提出另一個判斷原電池正負極的可行實驗方案_______________ (如 可靠,可不填)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】支撐海港碼頭基礎(chǔ)的鋼管樁,常用外加電流的陰極保護法進行防腐,工作原理如圖所示,下列有關(guān)表述錯誤的是( )
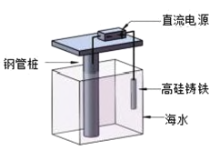
A.利用了電解原理B.電子由電源負極流向鋼管樁
C.鋼管樁是負極D.高硅鑄鐵作陽極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)在反應A(g)+3B(g)=2C(g)中,若以物質(zhì)A表示的該反應的化學反應速率為0.2 mol·L1·min1,則以物質(zhì)B表示此反應的化學反應速率為________mol·L1·min1。
(2)在2 L的密閉容器中,充入2 mol N2和3 mol H2,在一定條件下發(fā)生反應,3 s后測得N2為1.9 mol,則以H2的濃度變化表示的反應速率為____________________________。
(3)將10 mol A和5 mol B放入容積為10 L的密閉容器中,某溫度下發(fā)生反應:3A(g)+B(g) ![]() 2C(g),在最初2 s內(nèi),消耗A的平均速率為0.06 mol·L1·s1,則在2 s時,容器中有______ mol A,此時C的物質(zhì)的量濃度為________。
2C(g),在最初2 s內(nèi),消耗A的平均速率為0.06 mol·L1·s1,則在2 s時,容器中有______ mol A,此時C的物質(zhì)的量濃度為________。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com