
【題目】關于一定條件下的化學平衡H2(g)+I2(g)![]() 2HI(g) ΔH<0,下列說法正確的是( )
2HI(g) ΔH<0,下列說法正確的是( )
A.恒溫恒容,充入H2,v(正)增大,平衡右移
B.恒溫恒容,充入He,v(正)增大,平衡右移
C.加壓,v(正),v(逆)不變,平衡不移動
D.升溫,v(正)減小,v(逆)增大,平衡左移
 千里馬走向假期期末仿真試卷寒假系列答案
千里馬走向假期期末仿真試卷寒假系列答案科目:高中化學 來源: 題型:
【題目】某研究小組利用麥芽酚 A 制備某藥物中間體 X, 其合成路線如下
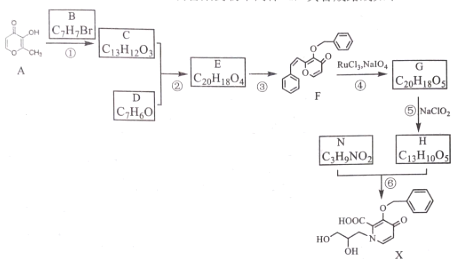
已知:

請回答 :
(l)化合物F的含氧官能團名稱為__________,化合物E 的結構簡式為____________。
(2)寫出反應① 的化學方程式:_________________ 。
(3)下列說法不正確的是__________ ( 填字母序號)。
A.化合物 E 可發生取代、加成、消去、氧化、還原等反應
B.化合物 N 的同分異構體可能是某氨基酸
C.反應③屬于消去反應
D.化合物X在一定條件下反應生成的物質中可能含有3個六元環
(4) 寫出化合物H同時符合下列條件的同分異構體的結構簡式______________。
a.IR 譜檢測表明:分子中含有2個獨立的苯 環,不含其他的環 ;
b.1H - NMR 譜表明:分子中共有3種化學環境不同的氫原子;
(5)由乙烯和苯為原料合成 D, 利用已知信息,設計合成路線(用流程圖表示,無機試劑任選)__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究碳、氮、硫等元素化合物的性質或轉化對建設生態文明、美麗中國具有重要意義。
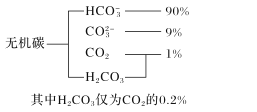
(1)海水中無機碳的存在形式及分布如圖所示,用離子方程式表示海水呈弱堿性的主要原因______________________。已知春季海水pH=8.1,預測冬季海水堿性將會_______(填“增強”或“減弱”),理由是_________________。
(2)工業上以CO和H2為原料合成甲醇的反應:CO(g)+2H2(g)===CH3OH(g) ΔH<0,在容積為1L的恒容容器中,分別在T1、T2、T3三種溫度下合成甲醇。如圖是上述三種溫度下不同H2和CO的起始組成比(起始時CO的物質的量均為1mol)與CO平衡轉化率的關系。下列說法正確的是________(填字母)。
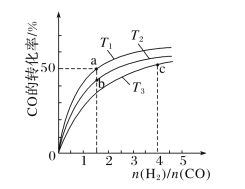
A.a、b、c三點H2轉化率:c>a>b
B.上述三種溫度之間關系為T1>T2>T3
C.c點狀態下再通入1molCO和4molH2,新平衡中H2的體積分數增大
D.a點狀態下再通入0.5molCO和0.5molCH3OH,平衡不移動
(3)NO加速臭氧層被破壞,其反應過程如下圖所示:
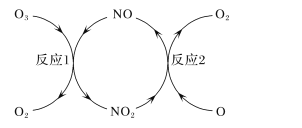
①NO的作用是_________________。
②已知:O3(g)+O(g)===2O2(g) ΔH=-143kJ·mol-1
反應1:O3(g)+NO(g)===NO2(g)+O2(g) ΔH1=-200.2kJ·mol-1 。
反應2:熱化學方程式為____________________________。
(4)若將CO和NO按不同比例投入一密閉容器中發生反應:2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-759.8kJ·mol -1,反應達到平衡時,N的體積分數隨n(CO)n(NO)的變化曲線如下圖。
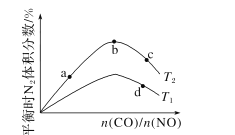
①b點時,平衡體系中C、N原子個數之比接近________。
②a、b、c三點CO的轉化率從小到大的順序為________;b、c、d三點的平衡常數從大到小的順序為__________。
③若n(CO)n(NO)=0.8,反應達平衡時,N的體積分數為20%,則NO的轉化率為_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.亞硫酸鈉的氧化反應:2Na2SO3 (aq) +O2(aq)=2Na2SO4(aq) H=x kJ/mol。其反應速率受溶解氧濃度影響,分為富氧區和貧氧區兩個階段。
(1)已知O2(g) ![]() O2(aq) H=y kJ/mol,Na2SO3 溶液與O2(g)反應的熱化學方程式為___________________。
O2(aq) H=y kJ/mol,Na2SO3 溶液與O2(g)反應的熱化學方程式為___________________。
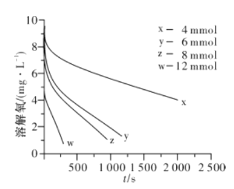
(2)291.5 K時,1.0 L溶液中Na2SO3初始量分別為4、6、8、12 mmol,溶解氧濃度初始值為9.60 mg/L,每5 s記錄溶解氧濃度,實驗結果如圖所示。當Na2SO3初始量為12 mmol,經過20 s溶解氧濃度降為6.40 mg/L,則0~20s內Na2SO3的平均反應速率為_______mol/(L·s)。
(3)為確定貧氧區速率方程v=k·ca(SO32-)·cb(O2)中的a、b的值(取整數),分析實驗數據。
c(Na2SO3)×103 | 3.65 | 5.65 | 7.65 | 11.65 |
v×106 | 10.2 | 24.4 | 44.7 | 103.6 |
①當溶解氧濃度為4.0 mg/L時,c(SO32-)與速率數值關系如表(甲)所示,則a=____。
②當溶解氧濃度小于4.0mg/L時,圖中曲線皆為直線,Na2SO3氧化速率與溶解氧濃度無關,則b=_______。
(4)兩個階段不同溫度的速率常數之比如表(乙)所示。已知![]() ,R為常數。Ea(富氧區)_____ (填“>”或“<”)Ea(貧氧區)。
,R為常數。Ea(富氧區)_____ (填“>”或“<”)Ea(貧氧區)。
反應階段 | 速率方程 |
|
富氧區 | v=k·c (SO32-)·c (O2) | 1.47 |
貧氧區 | v=k·ca (SO32-)·cb(O2) | 2.59 |
II. (5)在容積固定的密閉容器中,起始充入0.2 mol SO2和0.1 mol O2,反應體系起始總壓強0.1MPa。反應在一定溫度下達到平衡時SO2的轉化率為90%。該反應的壓強平衡常數Kp=________ ( 分壓=總壓×物質的量分數)(寫單位)。
(6)利用原電池原理,也可用SO2和O2來制備硫酸,該電池用多孔材料作電極。請寫出該電池負極反應式_________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列指定反應的離子方程式正確的是
A.用石墨電極電解MgCl2溶液:Mg2++2Cl-+2H2O![]() Mg(OH)2↓+Cl2↑+H2↑
Mg(OH)2↓+Cl2↑+H2↑
B.泡沫滅火器工作時化學反應:2Al3++3CO32-+6H2O=Al(OH)3↓+3CO2↑
C.向Ca(HCO3)2溶液中滴加少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
D.硫化鈉的水解反應;S2-+H3O+=HS-+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關化學實驗操作,現象和結論均為正確的是
選項 | 操作 | 現象 | 結論 |
A | Mg2+和Cu2+共存的溶液中滴入適量NaOH溶液 | 產生白色沉淀 | 相同溫度下,溶度積常數 Ksp[Mg(OH)2]<Ksp[Cu(OH)2] |
B | 加熱盛有(NH4)2CO3固體的試管,并在試管口放置濕潤的紅色石蕊試紙 | 試紙變藍 | (NH4)2CO3顯堿性 |
C | 常溫下,向等濃度、等體積的Na2CO3和NaHCO3溶液中滴加等量的酚酞溶液 | 碳酸鈉溶液中紅色更深 | 陰離子水解常數Kh: CO32->HCO3- |
D | 向飽和硼酸溶液中滴加少量Na2CO3粉末 | 無氣泡冒出 | 不能證明酸性:碳酸>硼酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甘氨酸亞鐵[(NH2CH2COO)2Fe]是一種補鐵強化劑。某學習小組利用FeCO3與甘氨酸(NH2CH2COOH)制備甘氨酸亞鐵,實驗裝置如下圖所示(夾持和加熱儀器已省略)。
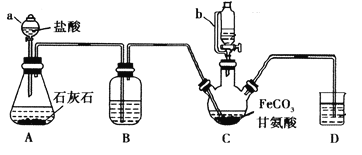
有關物質性質如下表:
甘氨酸 | 檸檬酸 | 甘氨酸亞鐵 |
易溶于水,微溶于乙醇 | 易溶于水和乙醇 | 易溶于水,難溶于乙醇 |
兩性化合物 | 強酸性、強還原性 |
實驗過程:
I.合成:裝置C中盛有0.1mol FeCO3和200mL1.0mol·L-1甘氨酸溶液和適量檸檬酸。實驗時,先打開儀器a的活塞,待裝置c中空氣排凈后,加熱并不斷攪拌,并通過儀器b向C中加入適量氫氧化鈉溶液調節pH到6左右,使反應物充分反應。
Ⅱ.分離:反應結束后,過濾,將濾液進行蒸發濃縮;加入無水乙醇,過濾、洗滌并干燥。
回答下列問題:
(1)儀器a的名稱是________;與a相比,儀器b的優點是_____________________________。
(2)裝置B中盛有的試劑是____________;實驗過程中裝置D的導管一直沒入液面下的必要性是___________________________________________。
(3)合成過程加入檸檬酸的作用是促進FeCO3溶解和________________________ 。
(4)加入氫氧化鈉溶液調節pH若大于6,甘氨酸亞鐵產量下降。原因可用離子方程式表示為________。
(5)過程II中加入無水乙醇的目的是_______________________。
(6)檢驗產品中是否含有Fe3+的試劑名稱是_________ 。
(7)本實驗制得15.3g甘氨酸亞鐵(M=204g/mol),則其產率是_____%。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A.乙烯分子中的 σ鍵和π鍵比例為 5:1
B.某元素氣態基態原子的逐級電離能(kJmol﹣1)分別為 738、1451、7733、10540、13630、17995、21703, 當它與氯氣反應時可能生成的陽離子是 X2+
C.Na、P、Cl 的電負性依次增大
D.向配合物[TiCl(H2O)5]Cl2H2O 溶液中加入足量的 AgNO3 溶液,所有 Cl-均被完全沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,下列各溶液中有關微粒的物質的量濃度關系正確的是( )
A.向0.1mol/LNH4HSO4溶液中滴加NaOH溶液至恰好呈中性:c(Na+)c(NH4+)c(SO42-)c(OH-)c(H+)
B.0.1mol/LNaHC2O4溶液呈酸性:c(Na+)c(HC2O4-)c(H2C2O4)c(C2O42-)
C.20mL0.1mol/LCH3COONa溶液與10mL0.1mol/LHCl溶液混合后的酸性溶液:cCH3COOH2cH+c(CH3COO-)cOH-
D.濃度均為0.1mol/L的小蘇打溶液與燒堿溶液等體積混合:c(Na+)c(H+)2c(CO32-)c(OH-)c(HCO3-)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com