
(I) 電子工業常用30%的FeCl3溶液腐蝕敷在絕緣板上的銅箔,制造印刷電路板。用FeCl3溶液做腐蝕液與Cu反應生成CuCl2和FeCl2。
(1) 寫出該反應的化學方程式 。
(2) 檢驗溶液中Fe3+存在的試劑是 ,證明Fe3+存在的現象是 。
(Ⅱ) 印刷電路的廢腐蝕液含有大量CuCl2、FeCl2、FeCl3,任意排放會造成環境污染及資源的浪費。通過下列流程可從該廢液中回收銅,并將鐵的化合物全部轉化為FeCl3溶液,作為腐蝕液原料循環使用。
⑴ 步驟①中發生反應的離子方程式 。
(2) 步驟②需加入的試劑A是 (填化學式)。
(3) 步驟③通入的氣體B是 (填化學式),寫出該反應的化學方程式 。
(4) 為測定濾渣中銅的質量分數,取50g的濾渣與足量的試劑A反應,得到5.6L氣體(標準狀況下),試計算濾渣中銅的質量分數。
(16分)
(I) (1)2FeCl3+Cu==2FeCl2+CuCl2 (2分) [化學式錯不給分]
(2)KSCN溶液(1分), 溶液變成血紅色(1分)
(II) (1)2Fe3++Fe=3Fe2+ (2分) Fe+Cu2+=Fe2++Cu (2分) [化學式錯不給分]
(2) HCl (1分)
(3) C12 (1分) 2FeCl2+C12=2FeCl3 (2分) [化學式錯不給分]
(4) 72% (4分)(按解題步驟給分)
方程式占1分
算出鐵的質量(或物質的量占1分)占2分
算出銅的質量分數占1分
解析試題分析:(I) (1)根據題中提供的反應物和生成物,故反應的化學方程式為2FeCl3+Cu==2FeCl2+CuCl2。
(2)檢驗Fe3+利用其特征反應,故試劑是KSCN溶液,現象是溶液變成血紅色。
(Ⅱ) ⑴Fe粉會和CuCl2、FeCl3反應,故離子方程式為2Fe3++Fe=3Fe2+ Fe+Cu2+=Fe2++Cu。
(2)過量的Fe粉在濾渣中,加入HCl使其反應,故加入的試劑A是HCl。
(3)濾液1、濾液2中都是Fe2+離子,加入氯氣使其反應生成Fe3+,故通入的氣體B是C12;反應的化學方程式為2FeCl2+C12=2FeCl3。
(4)依據反應方程式Fe+Cu2+=Fe2++Cu Fe+2HCl= FeCl2+H2↑計算。
考點:鐵、鐵的化合物、銅之間的反應
點評:本題是有關實驗方案的設計和無機反應的考查,要求學生熟悉所實驗的內容及原理,能夠考查同學們進行分析問題、解決問題的能力。


 高中必刷題系列答案
高中必刷題系列答案科目:高中化學 來源:2011-2012學年云南景洪第一中學高一上期末考試化學試卷(帶解析) 題型:實驗題
(I)電子工業常用30%的FeCl3。溶液腐蝕敷在絕緣板上的銅箔,制造印刷電路板。用FeCl3溶液做腐蝕液與Cu反應生成CuCl2和FeCl2。
(1)寫出該反應的化學方程式 。
(2)檢驗溶液中Fe3+存在的試劑是
(Ⅱ)印刷電路的廢腐蝕液含有大量CuCl2、FeCl2、FeCl3,任意排放會造成環境污染及資源的浪費。通過下列流程可從該廢液中回收銅,并將鐵的化合物全部轉化為FeCl3溶液,作為腐蝕液原料循環使用。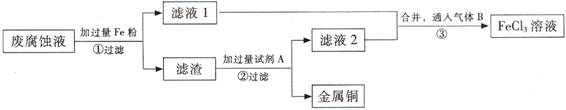 (3) 步驟①中發生反應的離子方程式
(3) 步驟①中發生反應的離子方程式
(4)濾渣的主要成分是 , (填化學式)。
(5)為了除去濾渣中的雜質得到銅,需加入的試劑A是 (填化學式)。
查看答案和解析>>
科目:高中化學 來源:2015屆廣東陸豐碣石中學高一下學期第一次月考化學試卷(解析版) 題型:實驗題
(I) 電子工業常用30%的FeCl3溶液腐蝕敷在絕緣板上的銅箔,制造印刷電路板。用FeCl3溶液做腐蝕液與Cu反應生成CuCl2和FeCl2。
(1) 寫出該反應的化學方程式 。
(2) 檢驗溶液中Fe3+存在的試劑是 ,證明Fe3+存在的現象是 。
(Ⅱ) 印刷電路的廢腐蝕液含有大量CuCl2、FeCl2、FeCl3,任意排放會造成環境污染及資源的浪費。通過下列流程可從該廢液中回收銅,并將鐵的化合物全部轉化為FeCl3溶液,作為腐蝕液原料循環使用。

⑴ 步驟①中發生反應的離子方程式 。
(2) 步驟②需加入的試劑A是 (填化學式)。
(3) 步驟③通入的氣體B是 (填化學式),寫出該反應的化學方程式 。
(4) 為測定濾渣中銅的質量分數,取50g的濾渣與足量的試劑A反應,得到5.6L氣體(標準狀況下),試計算濾渣中銅的質量分數。
查看答案和解析>>
科目:高中化學 來源:2014屆云南景洪第一中學高一上期末考試化學試卷(解析版) 題型:實驗題
(I)電子工業常用30%的FeCl3。溶液腐蝕敷在絕緣板上的銅箔,制造印刷電路板。用FeCl3溶液做腐蝕液與Cu反應生成CuCl2和FeCl2。
(1)寫出該反應的化學方程式 。
(2)檢驗溶液中Fe3+存在的試劑是
(Ⅱ)印刷電路的廢腐蝕液含有大量CuCl2、FeCl2、FeCl3,任意排放會造成環境污染及資源的浪費。通過下列流程可從該廢液中回收銅,并將鐵的化合物全部轉化為FeCl3溶液,作為腐蝕液原料循環使用。
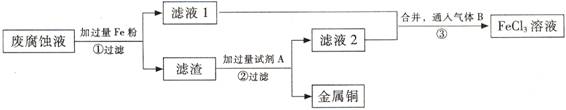 (3) 步驟①中發生反應的離子方程式
(3) 步驟①中發生反應的離子方程式
(4)濾渣的主要成分是 , (填化學式)。
(5)為了除去濾渣中的雜質得到銅,需加入的試劑A是 (填化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
(I)電子工業常用30%的FeCl3。溶液腐蝕敷在絕緣板上的銅箔,制造印刷電路板。用FeCl3溶液做腐蝕液與Cu反應生成CuCl2和FeCl2。
(1)寫出該反應的化學方程式 。
(2)檢驗溶液中Fe3+存在的試劑是
證明Fe2+存在的現象是 。
(Ⅱ)印刷電路的廢腐蝕液含有大量CuCl2、FeCl2、FeCl3,任意排放會造成環境污染及資源的浪費。通過下列流程可從該廢液中回收銅,并將鐵的化合物全部轉化為FeCl3 溶液,作為腐蝕液原料循環使用。

(3) 步驟①中發生反應的離子方
(4)濾渣的主要成分是 (填化學式)。
(5)為了除去濾渣中的雜質得到銅,需加入的試劑A是 (填化學式)。
(6)步驟③通人的氣體B (填化學式),
寫出該反應的化學方程式 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com