
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| H2O | CO | CO | H2 | |||
| i | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| ii | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| iii | 900 | a | b | c | d | t |
分析 (1)①反應速率v(CO2)=$\frac{△c(CO2)}{△t}$;平衡常數K=$\frac{[CO2]•[H2]}{[CO]•[H2O]}$;對于吸熱反應,溫度升高,平衡常數變大;對于放熱反應,溫度升高,平衡常數變小.②平衡轉化率等于物質消耗的量與物質的起始量之比.
(2)①原電池負極發生氧化反應,失去電子.②電解池中陽極發生氧化反應,失去電子;電解池陰極發生還原反應,得到電子.可根據電子守恒來計算原電池及電解池相關的計算題.
解答 解:(1)①實驗組i中,由H2O(g)+CO(g)?CO2(g)+H2(g)可知,在2L的恒容容器中,平衡時各物質的濃度分別為:[H2O]=0.2mol•L-1,[CO]=1.2mol•L-1,[CO2]=0.8mol•L-1,[H2]=0.8mol•L-1;所以反應速率v(CO2)=$\frac{[CO2]}{△t}$=$\frac{0.8mol•L-}{5min}$=0.16mol•L-1•min-1.在650℃下,平衡常數K1=$\frac{[CO2]•[H2]}{[CO]•[H2O]}$=$\frac{0.8mol•L-1×0.8mol•L-1}{0.2mol•L-1×1.2mol•L-1}$≈2.67;900℃時,平衡時各物質的濃度分別為:[H2O]=0.3mol•L-1,[CO]=0.8mol•L-1,[CO2]=0.2mol•L-1,[H2]=0.2mol•L-1,平衡常數K2=$\frac{0.2mol•L-1×0.2mol•L-1}{0.3mol•L-1×0.8mol•L-1}$≈0.17,溫度升高,K2小于K1.
故答案為:0.16mol•L-1•min-1;減小.
②在實驗組iii中,由H2O(g)+CO(g)?CO2(g)+H2(g)可知,在2L的恒容容器中,平衡時各物質的濃度分別為:[H2O]=$\frac{2-d}{2}$mol•L-1,[CO]=$\frac{1-d}{2}$mol•L-1,[CO2]=$\fracp9vv5xb5{2}$mol•L-1,[H2]=$\fracp9vv5xb5{2}$mol•L-1;在900℃時,K2=$\frac{(2-d)•(1-d)}{p9vv5xb5^{2}}$=0.17,解得d=0.4,由等量關系可得c=1-0.4=0.6;達平衡時實驗組ii中H2O(g)的轉化率αii (H2O)=$\frac{0.4mol}{1mol}$×100%=40%,實驗組iii中CO的轉化率αiii (CO)=$\frac{0.4mol}{1mol}$×100%=40%,所以αii (H2O)=αiii (CO).
故答案為:0.6;=.
(2)①負極CO發生氧化反應與O2-結合生成CO32-,負極電極反應式為:CO+2O2--2e-=CO32-;
故答案為:CO+2O2--2e-=CO32-.
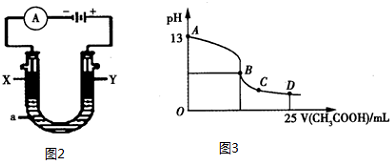
②電解池中陽極反應:2Cl--2e-=Cl2↑,陰極反應:2H2O+2e-=H2↑+2OH-,因此總電解方程式為:2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$Cl2↑+H2↑+2OH-;根據圖知,KOH溶液的pH=13,常溫下,KOH的濃度是0.1mol/L,則n(KOH)=0.1mol/L×2L=0.2mol,根據2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$2OH-+H2↑+Cl2↑知,生成0.2mol氫氧根離子轉移電子的物質的量=$\frac{0.2mol}{2}$×2=0.2mol,燃料電池的負極反應方程式是CO+2O2--2e-=CO32-,消耗1molCO轉移電子數=2mol,因此當轉移0.2mol電子時消耗CO的物質的量為0.1mol,則CO的質量=0.1mol×28g/mol=2.8g;
故答案為:2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$Cl2↑+H2↑+2OH-;2.8g.
點評 本題難度較大,綜合性強,綜合了化學反應速率、平衡,以及原電池電解池等知識,非常好的一道題.


 新課標同步訓練系列答案
新課標同步訓練系列答案 一線名師口算應用題天天練一本全系列答案
一線名師口算應用題天天練一本全系列答案科目:高中化學 來源: 題型:選擇題
| 實驗步驟 | 實驗現象 |
| ①a和b相混合 | 氣體變為紅棕色 |
| ②c和d相混合 | 產生白煙 |
| ③c、e分別通入少量溴水中 | 都變成無色透明的溶液 |
| ④b、e分別通入氫硫酸中 | 都產生淡黃色的渾濁 |
| A. | O2、NO、HCl、NH3、CO2 | B. | O2、NO、NH3、HCl、SO2 | ||
| C. | NO、O2、NH3、HCl、SO2 | D. | HBr、Cl2、NH3、H2S、C2H4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬與鹽溶液的反應都是置換反應 | |
| B. | 陰離子都只有還原性 | |
| C. | 離子化合物中肯定存在離子鍵,可能不存在共價鍵 | |
| D. | 與強酸、強堿都反應的物質只有兩性氧化物或兩性氫氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2CO3的摩爾質量為106 g | |
| B. | 金剛石與石墨互為同位素 | |
| C. | 常溫下,4.6gNa中含有的質子數為2.2NA | |
| D. | 標準狀況下,11.2LCO2完全參與反應,轉移的電子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 三種實驗方案中都能制得純凈的銅 | |
| B. | 甲方案中的反應涉及置換、分解、復分解三種反應類型 | |
| C. | 乙方案中加過量鐵粉只能還原其中的二種陽離子 | |
| D. | 丙方案不會產生環境污染 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2SO2(g)+O2(g)$?_{500℃}^{V_{2}O_{5}}$2SO3(g)△H=-196.6kJ/mol,若2molSO2完全反應則放出熱量等于196.6kJ | |
| B. | “冰,水為之,而寒于水”說明相同質量的水和冰比較,冰的能量高 | |
| C. | 已知C(石墨)=C(金剛石)△H=+1.9kJ/mol,則從能量角度看金剛石比石墨穩定 | |
| D. | 氫氣的燃燒熱為285.8kJ/mol,則氫氣燃燒的熱化學方程式為2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在相同條件下,甲酸的導電性比強酸溶液的導電性弱 | |
| B. | 甲酸能與水以任意比互溶 | |
| C. | 10mL 1mol/L甲酸恰好跟10 mL 1mol/L NaOH溶液完全反應 | |
| D. | 1mol/L甲酸溶液中c(H+)約為1×10-2mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
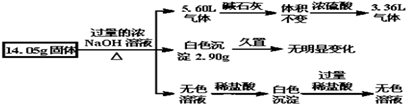
| A. | 一定含有Al,其物質的量為$\frac{5}{3}$mol | |
| B. | 一定不含FeCl2,可能含有MgCl2和AlCl3 | |
| C. | 一定含有(NH4)2SO4和FeCl2 | |
| D. | 一定含有(NH4)2SO4和MgCl2,且物質的量相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 1:4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com