
【題目】原子核外電子總數為42的烷烴有 ( )
A. 2種B. 3種C. 4種D. 5種
 快樂小博士鞏固與提高系列答案
快樂小博士鞏固與提高系列答案科目:高中化學 來源: 題型:
【題目】元素在周期表中的位置反映了元素的原子結構和性質。請回答下列有關硼(B)元素的問題:
(1)![]() 原子核內的中子數為________。
原子核內的中子數為________。
(2)硼元素在元素周期表中的位置為___________。
(3)![]() 的原子半徑__________
的原子半徑__________![]() 的原子半徑(填“大于”或“小于”)。
的原子半徑(填“大于”或“小于”)。
(4)硼元素的最高價氧化物對應的水化物酸性比氮元素的最高價氧化物對應的水化物酸性_______(填“強”或“弱”)。
(5)四氫硼鋰(LiBH4)是一種重要的化學試劑,低溫下可與HCl氣體發生如下反應:2 LiBH4 + 2 HCl = 2 LiCl + B2H6 + 2H2該反應中,LiBH4和B2H6中的氫元素均顯-1價。請回答下列問題。LiBH4中硼元素的化合價為__________;該反應的還原劑為____________;4 mol LiBH4完全反應后共失去_____mol電子。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素A、B、C、D 原子序數依次增大且最外層電子數之和為17。B、D 同主族,短周期中C原子半徑最大,B最外層電子數是次外層的3倍。下列推斷不正確的是
A. 元素B、C、D 形成的化合物的水溶液呈中性
B. 元素B、C 形成的化合物中可能既含有離子鍵又含共價鍵
C. 離子半徑從大到小的順序為D>B>C
D. 元素B 的簡單氣態氫化物的熱穩定性比D 的強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO2的利用是國際社會普遍關注的問題。
(1)CO2的電子式是__________
(2)CO2在催化劑作用下可以直接轉化為乙二醇和甲醇,但若反應溫度過高,乙二醇會深度加氫生成乙醇。
![]()
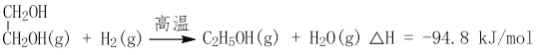
獲取乙二醇的反應歷程可分為如下2步:
I. 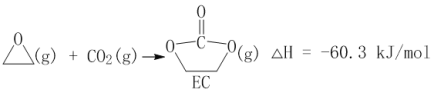
II.EC加氫能生成乙二醇與甲醇。
①步驟II的熱化學方程式是__________;
②研究反應溫度對EC加氫的影響(反應時間均為4小時),實驗數據見下表:
反應溫度/℃ | EC轉化率/ % | 產率/% | |
乙二醇 | 甲醇 | ||
160 | 23.8 | 23.2 | 12.9 |
180 | 62.1 | 60.9 | 31.5 |
200 | 99.9 | 94.7 | 62.3 |
220 | 99.9 | 92.4 | 46.1 |
由上表可知,溫度越高,EC的轉化率越高,原因是__________。溫度升高到220℃時,乙二醇的產率反而降低,原因是__________
(3)用稀硫酸作電解質溶液,電解CO2可制取甲醇,裝置如下圖所示,電極 a 接電源的__________極(填“正”或“負”),生成甲醇的電極反應式是__________
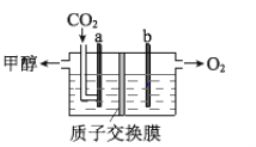
(4)CO2較穩定、能量低。為實現CO2的高效使用,下列研究方向合理的是__________(填序號)。
a.降低CO2參與反應的速率和比例
b.利用電能、光能或熱能預先活化CO2分子
c.選擇高效的催化劑降低反應條件
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗發現,298 K時,在FeCl3酸性溶液中加少量鋅粒后,Fe3+立即被還原成Fe2+。某夏令營興趣小組根據該實驗事實設計了如圖所示原電池裝置。下列有關說法正確的是( )
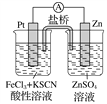
A. 該原電池的正極反應是Zn-2e-===Zn2+
B. 左燒杯中溶液的血紅色逐漸褪去
C. 該電池鉑電極上有氣泡出現
D. 該電池總反應為3Zn+2Fe3+===2Fe+3Zn2+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求回答下列問題:
(1)0.3molNH3中所含質子數與______gH2O分子中所含質子數相等。
(2)與3.2gSO2所含的氧原子數相等的NO2氣體在標準狀況下的體積為_______L。
(3)將30ml 0.5mol/L的NaOH溶液加水稀釋到500ml,稀釋后溶液物質的量濃度為_______。
(4)同溫同壓下,SO2與O2的密度比為____,若質量相同,兩種氣體體積比為___ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在溶液中能大量共存的一組離子是( )
A. K+、H+、SO32-、S2- B. NH4+、K+、OH-、Cl-
C. H+、K+、MnO4-、SO42- D. Fe3+、Na+、S2-、NO3-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將SO2氣體通入BaCl2溶液至飽和,未見有沉淀生成,繼續通入或加入另一種物質仍無沉淀產生,則通入或加入的物質不可能是( )
A. 氨水 B. CO2 C. 過氧化氫溶液 D. SO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】請將符合題意的下列變化的序號填在對應的橫線上:①碘的升華;②氧氣溶于水;③氯化鈉溶于水;④燒堿熔化;⑤氯化氫溶于水;⑥氯化銨受熱分解。
(1)化學鍵沒有被破壞的是__________;僅發生離子鍵破壞的是__________;
(2)即發生離子鍵破壞、又發生共價鍵破壞的是____________________;
(3)N2的電子式為__________;Na2O2的電子式為___________;CO2的電子式為_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com