
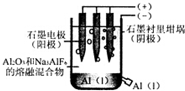
| A. | 電解過程中每轉移12 mol電子,會產生2 molO2 | |
| B. | 加入助熔劑冰晶石(Na3AIF6)可降低電解的溫度 | |
| C. | 電解過程中陽極反應式4A13++12e-→4Al | |
| D. | 若用該裝置電解氯化鋁溶液也能得到金屬鋁 |
分析 A、根據陽極電極反應式計算;
B、助熔劑冰晶石(Na3AIF6)可以使氧化鋁在較低溫度下熔融;
C、電解池中,陽極是氧離子發生失電子的氧化反應;
D、電解氯化鋁溶液,陰極為氫離子得電子生成氫氣,不會析出鋁單質.
解答 解:A、電解池的陽極是氧離子發生失電子的氧化反應,電極反應式為:2O2-→O2↑+4e-,所以轉移12 mol電子,會產生3 molO2,故A錯誤;
B、助熔劑冰晶石(Na3AIF6)可以使氧化鋁在較低溫度下熔融,所以可以降低電解的溫度,故B正確;
C、電解池中,陽極是氧離子發生失電子的氧化反應,電極反應式為:2O2-→O2↑+4e-,故C錯誤;
D、工業制鋁是電解熔融的氧化鋁:2Al2O3$\frac{\underline{\;電解\;}}{\;}$4Al+3O2↑,電解氯化鋁溶液,陰極為氫離子得電子生成氫氣,不會析出鋁單質,故D錯誤;
故選B.
點評 本題主要考查了鋁金屬的冶煉,掌握工業制鋁是利用電解原理電解熔融的氧化鋁:2Al2O3$\frac{\underline{\;電解\;}}{\;}$4Al+3O2↑,難度不大,注意對知識的積累.


科目:高中化學 來源: 題型:選擇題
| A. | 氣象環境報告中的“PM2.5”是一種新分子的描述 | |
| B. | 采取“靜電除塵”、“燃煤固硫”、“汽車尾氣催化凈化”等方法,可提高空氣質量、 | |
| C. | “玉兔號”月球車太陽能電池帆板的材料是二氧化硅 | |
| D. | 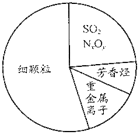 如圖為霧霾的主要成分示意圖,SO2和NxOy都屬于酸性氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向AgI濁液中滴入NaCl溶液,產生大量白色沉淀:AgI(s)+Cl-(aq)=AgCl(s)+I-(aq) | |
| B. | 用氨水除去鋁片表面的氧化膜:Al2O3+2NH3•H2O=2AlO2-+2NH4++H2O | |
| C. | 用鐵氰化鉀溶液檢驗Fe2+:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓ | |
| D. | 向酸性KMnO4溶液中滴入過氧化氫產生無色氣泡:2MnO4-+9H2O2+6H+=2Mn2++7O2↑+12H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 主族元素X、Y、Z、M、N的原子序數依次增大,X、Z、M分屬于3個不同的周期,X、M元素可以形成負一價離子,Y原子的各能層電子數相同,Z原子最外層電子數是次外層的3倍,N元素原子的4p軌道上有3個未成對電子.
主族元素X、Y、Z、M、N的原子序數依次增大,X、Z、M分屬于3個不同的周期,X、M元素可以形成負一價離子,Y原子的各能層電子數相同,Z原子最外層電子數是次外層的3倍,N元素原子的4p軌道上有3個未成對電子.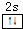 ,該元素的名稱是鈹.氣態分子YM2的立體構型直線型,YM2可形成多聚體(YM2)n的原因是BeCl2分子中Be與另外兩個BeCl2分子的Cl原子形成配位鍵.
,該元素的名稱是鈹.氣態分子YM2的立體構型直線型,YM2可形成多聚體(YM2)n的原因是BeCl2分子中Be與另外兩個BeCl2分子的Cl原子形成配位鍵.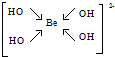 ,1mol該離子中含有的共價鍵數目為8NA.
,1mol該離子中含有的共價鍵數目為8NA.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 元素Y的最高正化合價為+6 | B. | 簡單離子半徑的大小順序:X>Y>Z | ||
| C. | 簡單氣態氫化物的穩定性:X>Y | D. | 元素X和Y能形成離子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 鐵片鍍鋅時,鐵片與外電源的正極相連 | |
| B. | 反應SO2(g)+2H2S(g)=3S(s)+2H2O(l)在常溫下能自發進行,則該反應的△H<0 | |
| C. | 0.1mol•L-1的CH3COOH溶液加水稀釋,溶液的pH和其中水的電離程度均增大 | |
| D. | 在N2(g)+3H2(g)?2NH3(g)平衡體系中加入催化劑,N2的反應速率和轉化率均增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下NaF溶液的pH大于7 | |
| B. | HF能與Na2CO3溶液反應,產生CO2氣體 | |
| C. | 1mol/L的HF水溶液能使紫色石蕊試液變紅 | |
| D. | 用HF溶液做導電性實驗,燈泡很暗 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | b-m-n | B. | b+m-n | C. | b-m+n | D. | b+m+n |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com