
下列離子方程式正確的是
A.過量氯氣通入溴化亞鐵溶液中2Fe2++2Br-+2Cl2====Fe3++Br2+4Cl-
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O
C.碳酸氫鈣和過量的氫氧化鈉溶液反應:Ca2++ OH—+HCO3—=CaCO3↓+ H2O
D.用FeCl3溶液腐蝕印刷電路板:Cu+Fe3+=Fe2++Cu2+
 考前必練系列答案
考前必練系列答案科目:高中化學 來源:2016屆河南省濮陽市心高三上第一次市統摸底化學試卷(解析版) 題型:填空題
(7分)某消毒液的主要成分為 NaClO(混有少量 NaCl),請用相應的化學用語來解釋下列事實。
(1)該消毒液可用NaOH溶液吸收 Cl2 制備,化學方程式為__________。
(2)該消毒液的 pH 約為 12,離子方程式為________________。
(3)向 FeSO4 溶液中滴入少量該溶液,溶液顏色變成棕黃色,反應的離子方程式為_______________。
(4)該消毒液不能與潔廁靈(主要成分為濃鹽酸)混用,否則會產生中毒危險。若將二者混合,每產生 1 mol Cl2,轉移電子個數約為_____________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省白城市高一上第一次月考化學試卷(解析版) 題型:選擇題
A、B、C、D可能是Na2CO3、HCl、AgNO3、BaCl2四種無色溶液中的某一種,把它們兩兩混合后產生的現象如下表,則A、B、C、D四種物質按順序排列正確的是
反應物 | A+B | A+C | B+C | C+D | B+D |
現象 | 白↓ | 白↓ | 白↓ | 白↓ | 無色↑ |
A.BaCl2、 Na2CO3、 AgNO3、 HCl
B.Na2CO3、 HCl、 AgNO3、 BaCl2
C.HCl、 AgNO3、 Na2CO3、 BaCl2
D.AgNO3、 Na2CO3、 BaCl2、 HCl
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北大名縣第一中學高二上學期第一次月考試化學試卷(解析版) 題型:選擇題
在體積一定的密閉容器中給定物質A、B、C的量,在一定條件下發生反應建立的化學平衡:aA(g) + bB(g) 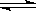 xC(g),符合下圖所示的關系(c%表示平衡混合氣中產物C的百分含量,T表示溫度,p表示壓強)。在圖中,Y軸是指
xC(g),符合下圖所示的關系(c%表示平衡混合氣中產物C的百分含量,T表示溫度,p表示壓強)。在圖中,Y軸是指
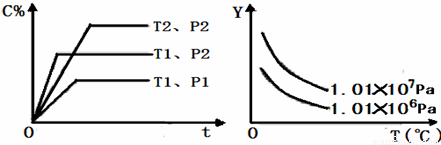
A.反應物A的百分含量 B.平衡混合氣中物質B的百分含量
C.平衡混合氣的密度 D.平衡混合氣的平均摩爾質量
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北大名縣第一中學高二上學期第一次月考試化學試卷(解析版) 題型:選擇題
在容積為2升的密閉容器中,有反應:mA(g)+nB(g) 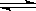 pC(g)+qD(g),經過5分鐘達到平衡,此時,各物質的變化為:A減少了amol·L-1,B的平均反應速度VB=
pC(g)+qD(g),經過5分鐘達到平衡,此時,各物質的變化為:A減少了amol·L-1,B的平均反應速度VB=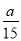 mol·L-1·min-1,C增加了
mol·L-1·min-1,C增加了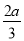 mol·L-1,這時,若增加系統壓強,發現A與C的百分含量不變,則m︰n︰p︰q為
mol·L-1,這時,若增加系統壓強,發現A與C的百分含量不變,則m︰n︰p︰q為
A.1︰1︰1︰1 B.1︰3︰2︰2
C.1︰3︰2︰1 D.3︰1︰2︰2
查看答案和解析>>
科目:高中化學 來源:2016屆浙江省高三上學期第一次模擬考試化學試卷(解析版) 題型:選擇題
某廢水中含有的NH4+在一定條件下可被O2氧化,反應過程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) △H=-273kJ·mol-1
②NO2-(aq)+1/2O2(g)=NO3-(aq) △H=-73kJ·mol-1
下列說法正確的是( )
A.1mol的NH3和1mol的NH4+都有10×6.02 ×1023個質子
B.室溫下,NH4NO2溶液呈酸性,則說明Ka(HNO2)< Kb(NH3·H2O)
C.NH4+(aq)+2O2(g) NO3—(aq)+2H+(aq)+H2O(l);△H= - 346kJ/mol
D.在上述兩次轉化過程中,廢水的酸性先增大然后逐漸減弱
查看答案和解析>>
科目:高中化學 來源:2016屆云南省高三上學期第一次月考化學試卷(解析版) 題型:選擇題
將15.6 g Na2O2和5.4 g Al同時放入一定量的水中,充分反應后得到200 mL溶液,再向該溶液中緩慢通入標準狀況下的HCl氣體6.72 L,若反應過程中溶液的體積保持不變,則下列說法正確的是
A.標準狀況下,反應過程中得到6.72 L氣體
B.最終得到的溶液中c(Na+)=c(Cl-)+c(OH-)
C.最終得到7.8 g沉淀
D.最終得到的溶液中c(Na+)=1.5 mol·L-1
查看答案和解析>>
科目:高中化學 來源:2016屆全國推薦高三聯考(二)化學試卷(解析版) 題型:填空題
(12分) 軟錳礦(主要成分MnO2,含Fe,Al2O3 ,MgO雜質)的水懸濁液與煙氣中的SO2反應可制備MnSO4·H2O,MnO2與SO2反應的化學方程式為MnO2 +SO2=MnSO4。已知下列信息:
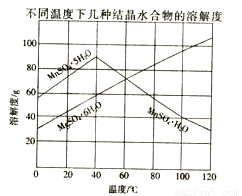
室溫下幾種氫氧化物的溶度積

回答下列問題:
(1)質量為17.40 g純凈MnO2最多能氧化 L(標準狀況) SO2。
(2)懸濁液吸收煙氣后,Fe首先轉化為Fe2+進入溶液,然后被 氧化為Fe3+;要證明溶液中存在Fe3+,可選擇的試劑是 (填標號)。
a.KMnO4溶液 b.KCl溶液 c.KSCN溶液 d.KNO3溶液
(3)室溫下,將吸收液過濾,在濾液中加入CaCO3,可除去MnSO4溶液中的Fe3+、Al3+,原因是 。
(4)從MnSO4和MgSO4混合溶液中結晶MnSO4·H2O晶體,需控制結晶溫度范圍為 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西陽泉十五中高三第一次階段考試化學試卷(解析版) 題型:選擇題
下列各組中的兩種物質相互反應時,無論哪種過量,都可以用同一個離子方程式表示的是
①碳酸鈉溶液與鹽酸 ②偏鋁酸鈉溶液與鹽酸 ③苯酚鈉溶液和CO2
④硝酸銀溶液和氨水 ⑤氯化鋁溶液和氨水 ⑥碳酸氫鈉溶液與澄清石灰水
A.③⑤ B.①③⑥ C.僅有⑤ D.②④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com