
反應2SO2(g)+O2 (g)![]() 2SO3(g) ,經一段時間后SO3的濃度增加了0.4mol·L-1 ,在這段時間內用O2表示的反應速率為0.4mol·L-1·s-1 ,則這段時間為 ( )
2SO3(g) ,經一段時間后SO3的濃度增加了0.4mol·L-1 ,在這段時間內用O2表示的反應速率為0.4mol·L-1·s-1 ,則這段時間為 ( )
A.0.1s B.2.5s C.0.5s D.10s
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
在一定條件下,向一帶活塞的密閉容器中充入2molSO2和1molO2,發生下列反應:
2SO2(g)+O2(g) 2SO3(g) △H<0,達到平衡狀態后,在t1時刻改變條件,化學反應速率隨時間變化關系如圖。下列對t1時刻改變條件的推斷中正確的是
A.保持壓強不變,升高反應溫度
B.保持溫度不變,增大容器體積
C.保持溫度和容器體積不變,充入1molSO3(g)
D.保持溫度和壓強不變,充入1molSO3(g)
查看答案和解析>>
科目:高中化學 來源: 題型:
(9分)利用催化氧化反應將SO2轉化為SO3是工業上生產硫酸的關鍵步驟。T℃時反應2SO2(g)+O2(g)2SO3(g)過程中的能量變化如圖所示,回答下列問題。
(1)T℃時將3molSO2和1molO2通入體積為2L的恒溫恒容密閉容器中,發生反應。2min時反應達到平衡,此時測得反應物O2還剩余0.1mol , 則達到平衡時SO2的轉化率為 。(1分)
(2)下列敘述能證明該反應已達化學平衡狀態的是 (填序號)(2分)
①SO2的體積分數不再發生變化 ②容器內壓強不再發生變化 ③容器內氣體分子總數不再發生變化 ④相同時間內消耗2n molSO2的同時生成n molO2 ⑤相同時間內消耗2n molSO2的同時生成2n molSO3
(3) 反應 (填“放出”或“吸收”) 熱量(用E1、E2或E3表示)(2分)。
(4)若以下圖所示裝置,用電化學原理生產硫酸,將SO2、O2以一定壓強噴到活性電極上反應。
寫出兩電極的電極反應式:
; 。(2分) [來網]為穩定持續生產,硫酸溶液的濃度應維持不變,則通入SO2和水的質量比為 (2分)
查看答案和解析>>
科目:高中化學 來源:2011-2012學年江蘇省揚州市邗江區高二下學期期中考試化學試卷(帶解析) 題型:實驗題
(14分)在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+ O2 (g)  2SO3(g) △H< 0。查閱資料知SO3熔點16.83℃,沸點44.8℃。
2SO3(g) △H< 0。查閱資料知SO3熔點16.83℃,沸點44.8℃。
(1)600℃時,在一密閉容器中,將二氧化硫和氧氣混合,反應過程中SO2,O2,SO3物質的量變化如圖。
①該反應的化學平衡常數表達式 K=
②該反應能自發進行的原因是 。
③據圖判斷,該反應處于平衡狀態的時間是 。
④據圖判斷,反應進行至20 min時,曲線發生變化的原因是 (用文字表達)。
(2)某化學研究學習小組用下圖的裝置組裝設計了一個實驗,以測定SO2轉化為SO3的轉化率,儀器的連接順序是a→h→i→b→c→f→g→d→e。
①為提高SO2的轉化率,實驗時Ⅰ處滴入濃硫酸與Ⅱ處加熱催化劑的先后順序是 。
②在Ⅰ處用大火加熱燒瓶時SO2的轉化率會 。(填“填大”“不變”或“減小”)
③用n mol Na2SO3粉末與足量濃硫酸進行此實驗,當反應結束時,繼續通入O2一段時間后,稱得Ⅲ處增重 m g,則本實驗中SO2的轉化率為 。
查看答案和解析>>
科目:高中化學 來源:2014屆天津市高二上學期期中考試化學試卷(解析版) 題型:選擇題
在一定溫度下、一定體積條件下,能說明下列反應達到平衡狀態的是( )
A.反應2SO2(g)+O2(g)
 2SO3(g) 容器內的密度不隨時間變化
2SO3(g) 容器內的密度不隨時間變化
B.反應A2(g)+B2(g)
 2AB(g)容器內的總壓強不隨時間變化
2AB(g)容器內的總壓強不隨時間變化
C.反應N2+3H2 2NH3容器內氣體平均相對分子質量不隨時間變化
2NH3容器內氣體平均相對分子質量不隨時間變化
D.反應4A(s)+3B(g)
 2C(g)+D(g)容器內氣體平均相對分子質量不隨時間變化
2C(g)+D(g)容器內氣體平均相對分子質量不隨時間變化
查看答案和解析>>
科目:高中化學 來源:09-10學年長春外國語學校高一下學期第二次月考理科化學卷 題型:選擇題
對于反應2SO2(g)+O2(g) 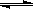 2SO3(g)能增大正反應速率的措施是
2SO3(g)能增大正反應速率的措施是
A.通入大量O2 B.增大容器容積
C.移去部分SO3 D.降低體系溫度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com