
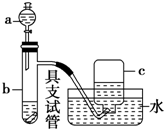
 如圖是用濃硝酸、銅片、水等試劑探究濃、稀硝酸的強氧化性并觀察還原產物的實驗裝置.
如圖是用濃硝酸、銅片、水等試劑探究濃、稀硝酸的強氧化性并觀察還原產物的實驗裝置.分析 Ⅰ.(1)銅與濃硝酸發生氧化還原反應生成硝酸銅和二氧化氮和水;
(2)實驗中銅溶解同時有紅棕色氣體產生,則可說明濃硝酸具有強氧化性,氧化銅單質生成銅離子,據此答題;
Ⅱ.(3)上述反應完成后,向試管中加水將濃硝酸稀釋成稀硝酸,如果能繼續溶解銅,則可進一步證明稀硝酸也具有強氧化性,據此判斷解答;
(4)依據一氧化氮為無色,二氧化氮為紅棕色,一氧化氮容易被氧化氧化生成二氧化氮,據此判斷解答.
解答 解:Ⅰ.(1)銅與濃硝酸發生氧化還原反應生成硝酸銅和二氧化氮和水,化學方程式:Cu+4HNO3(濃)═Cu(NO3)2+2NO2↑+2H2O;
故答案為:Cu+4HNO3(濃)═Cu(NO3)2+2NO2↑+2H2O;
(2)實驗中銅片溶解,試管中溶液變藍,且有紅棕色氣體產生,則可說明濃硝酸具有強氧化性,氧化銅單質生成銅離子,
故答案為:銅片溶解,試管中溶液變藍,且有紅棕色氣體產生;
Ⅱ.(3)上述反應完成后,向試管中加水將濃硝酸稀釋成稀硝酸,如果能繼續溶解銅,則可進一步證明稀硝酸也具有強氧化性,
故答案為:向試管中加水將濃硝酸稀釋;
(4)若b生成的氣體為紅棕色,說明氣體為二氧化氮,若b生成的氣體為無色,接觸空氣后變為紅棕色,說明生成氣體為一氧化氮,故選C;
故答案為:C.
點評 本題考查了硝酸的性質,明確硝酸氧化性與濃度之間的關系是解題關鍵,注意解有關硝酸反應的計算題時,對氮原子守恒的應用,題目難度不大.


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 預期現象和結論 |
| 步驟1:取少量吸收液于試管中,加稀硫酸酸化,然后再滴入幾滴品紅溶液; | 現象:品紅不褪色 結論:假設1不成立; |
| 步驟2:另取少量吸收液于試管中, 滴入幾滴KSCN溶液. | 現象:溶液變紅 結論:假設2成立. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1molCu和足量熱濃硫酸反應可生成SO3分子數為0.1NA | |
| B. | 標準狀況下,5.6LCO2與足量Na2O2反應轉移的電子數為0.5NA | |
| C. | 常溫常壓下,6.0g SiO2含有的SiO2分子數為0.1NA | |
| D. | 工業上將氨氣與氧氣在催化劑作用下發生氧化反應,若有標準狀況下V L氨氣完全反應,并轉移n個電子,則阿伏加德羅常數NA可表示為:$\frac{22.4n}{5V}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
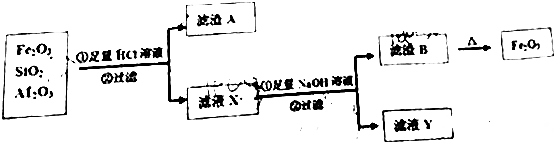
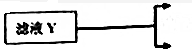
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 晶體硅 | B. | 二氧化硅 | C. | 鋼 | D. | 鋁硅合金 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.0 | B. | 2.0 | C. | 13.0 | D. | 14.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2O、CH4、HF | B. | 紅磷、硫、碘 | ||
| C. | CO2、SO2、NO2 | D. | H2SO4、CH3CH2OH、HCHO |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com