
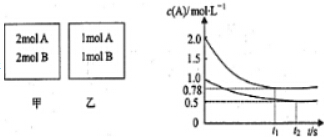
分析 (1)乙容器中,A參加反應的物質的量=(1-0.5)mol/L×1L=0.5mol,根據A和B的關系式知,參加反應的B的物質的量也是0.5mol,則B的轉化率=$\frac{0.5mol/L}{1mol/L}$×100%;
(2)計算甲、乙容器中A的轉化率,再根據壓強對A轉化率的影響來確定x值;
(3)根據化學平衡常數K=$\frac{c(C)}{c(A)•c(B)}$;
(4)根據反應處于平衡狀態,正逆反應速率,各組成成分不變,及某些物理量不變進行判斷;
(5)A.恒容容器中,A的濃度不變,則平衡不移動;
B.升高溫度,平衡向吸熱反應方向移動;
C.若向甲容器中再充入2molA、2molB,相當于增大壓強,A在轉化率比原來大;
D.若甲容器為等壓可變容器,則甲中沖入惰性氣體,容器體積增大,相當于減壓,則c(A)減小,v(正)、v(逆)減小,根據壓強對平衡移動的影響可判斷平衡移動方向.
解答 解:(1)乙容器中,A參加反應的物質的量=(1-0.5)mol/L×1L=0.5mol,根據A和B的關系式知,參加反應的B的物質的量也是0.5mol,則B的轉化率=$\frac{0.5mol/L}{1mol/L}$×100%=50%,
故答案為:50%;
(2)甲容器反應達到平衡后,c(A)=0.78 mol•L-1,A的轉化率=$\frac{(2.0-0.78)mol/L}{2mol/L}$=61%,乙容器中,A參加反應的物質的量=(1-0.5)mol/L×1L=0.5mol,A的轉化率=$\frac{0.5mol/L}{1mol/L}$=50%,即壓強越大,A的轉化率越高,所以正反應為氣體體積減小的反應,則x=1,
故答案為:1;
(3)反應達到平衡時,乙容器中c(A)=c(B)=c(C)=0.5 mol•L-1,T℃時,該反應的平衡常數K=$\frac{c(C)}{c(A)•c(B)}$=$\frac{0.5}{0.5×0.5}$=2,
故答案為:2;
(4)A.v(A)=c(C),未說明是正反應速率還是逆反應速率,故不能判斷反應是否處于平衡狀態,故A錯誤;
B.該反應為氣體體積減小的反應,容器中壓強不變時,說明反應已經處于平衡狀態,故B正確;
C.該反應是恒容條件下進行,反應中氣體質量守恒,所以容器中混合氣體的密度始終不變,故密度不能作為平衡狀態 的判斷依據,故C錯誤;
D.容器中A的體積分數不變,則說明反應處于平衡狀態,故D正確,
故選BD;
(5)A.向平衡后的乙容器中充入惰性氣體氦氣,氣體的濃度不變,平衡不發生移動,所以c(A)不變,故A錯誤;
B.將乙容器單獨升溫,平衡逆向移動,A的體積分數增大,更大于甲容器中A的體積分數,故B錯誤;
C.若向甲容器中再充入2 mol A、2 mol B,相當于增大壓強,平衡向正反應方向移動,則達到平衡時A的轉化率比不加前增大,所以平衡時甲容器中0.78 mol•L-1<c(A)<1.56 mol•L-1,故C正確;
D.若甲容器為等壓可變容器,則甲中沖入惰性氣體,容器體積增大,相當于減壓,則c(A)減小,v(正)、v(逆)減小,該反應的正反應為氣體體積減小的反應,減壓平衡逆向移動,故D錯誤.
故答案為:C.
點評 本題考查了化學平衡的移動、化學平衡的計算、等效平衡等知識點,根據圖象計算轉化率,根據轉化率計算x值,再結合等效平衡及影響化學平衡的因素來分析(4),注意等效平衡的應用,難度中等.


 期末金牌卷系列答案
期末金牌卷系列答案 輕松課堂標準練系列答案
輕松課堂標準練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 9 mol | B. | 7 mol | C. | 6 mol | D. | 8 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 吸熱44kJ | B. | 吸熱2.44KJ | C. | 放熱44kJ | D. | 放熱2.44KJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 晶體硅是良好的半導體材料 | |
| B. | 光導纖維中成分和沙子中的主要成分相同 | |
| C. | 用通入澄清石灰水的方法可以區分出CO2和SO2氣體 | |
| D. | SO2的漂白原理與木炭、過氧化鈉及濕潤氯氣的漂白原理不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 飽和氯水中加水稀釋,促進氯水中水的電離 | |
| B. | 向氨水中加入氯化銨,由于氯化銨溶液呈酸性,所以溶液pH降低 | |
| C. | 碳酸鈉溶液中存在CO32-+H2O?HCO3-+OH-平衡,若通入CO2,則平衡逆向移動 | |
| D. | 向氫氧化鎂懸濁液中加水稀釋,Mg(OH)2沉淀溶解平衡正向移動,但c(Mg2+)降低 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④⑤ | B. | ①③⑤ | C. | ①②⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使甲基橙變紅的溶液中:Na+、Cl-、CH3COO-、Fe2+ | |
| B. | 水電離的OH-濃度為10-12mol/L-1的溶液中:Mg2+、NH4+、AlO2-、SO32- | |
| C. | 無色溶液中:Al3+、NO3-、Cl-、SO42- | |
| D. | c(H2C2O4)=0.5 mol/L溶液中:Na+、K+、MnO4-、Cl- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com