
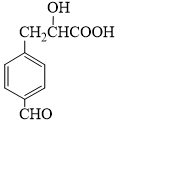
| A. | 能發生縮聚反應 | B. | 能發生消去反應 | ||
| C. | 1mol X最多消耗5 mol H2 | D. | 1mol X最多消耗2 mol Na |
科目:高中化學 來源: 題型:選擇題
| A. | 銅與硝酸反應 | B. | 明礬溶液與燒堿溶液反應 | ||
| C. | 碳酸鈉溶液和鹽酸反應 | D. | 硫在氧氣中燃燒 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
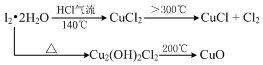
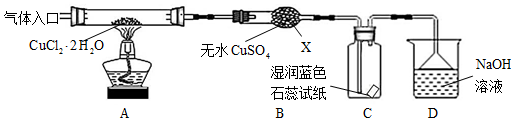
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 縮小體積加壓 | B. | 擴大體積減壓 | C. | 增加E的濃度 | D. | 降溫 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
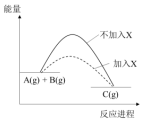
| A. | 反應速率增大 | B. | 反應物轉化率增大 | ||
| C. | 生成物的能量降低 | D. | 反應的熱效應降低 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,其屬于非極性(填“極
,其屬于非極性(填“極
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 丙烯的加聚反應產物 | |
| B. | 乙醇的消去反應產物 | |
| C. | 甲烷與氯氣的取代反應中的有機產物 | |
| D. | 苯與氫氣按1:3加成反應的產物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com