
實驗室模擬回收某廢舊含鎳催化劑(主要成分為NiO,另含Fe2O3、CaO、CuO、BaO等)生產Ni2O3。其工藝流程如下:
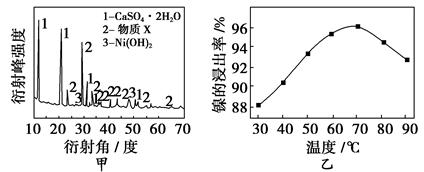
(1)根據圖甲所示的X射線衍射圖譜,可知浸出渣含有三種主要成分,其中“物質X”為________。圖乙表示鎳的浸出率與溫度的關系,當浸出溫度高于70 ℃時,鎳的浸出率降低,浸出渣中Ni(OH)2含量增大,其原因是
________________________________________________________________。
(2)工藝流程中副產品的化學式為______________。
(3)已知有關氫氧化物開始沉淀和沉淀完全的pH如下表:
| 氫氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 開始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
科目:高中化學 來源: 題型:填空題
(15分)空氣吹出法工藝,是目前“海水提溴”的最主要方法之一。其工藝流程如下: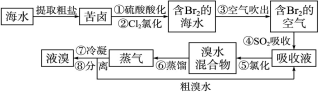
(1)溴在周期表中位于第______周期第________族。
(2)步驟①中用硫酸酸化可提高Cl2的利用率,理由是__________________________。
(3)步驟④利用了SO2的還原性,反應的離子方程式為________________________。
(4)步驟⑥的蒸餾過程中,溫度應控制在80~90 ℃。溫度過高或過低都不利于生產,請解釋原因____________________________________________________。
(5)步驟⑧中溴蒸氣冷凝后得到液溴與溴水的混合物,可利用它們的相對密度相差很大的特點進行分離。分離儀器的名稱是____________。
(6)步驟①、②之后并未直接用“含Br2的海水”進行蒸餾得到液溴,而是經過“空氣吹出”、“SO2吸收”、“氯化”后再蒸餾,這樣操作的意義是_________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下圖是關于藥物華素片(西地碘片)的使用說明書,以下為說明書的部分內容:
| 華素片(西地碘片)使用說明書 【品名或組成】 品名:西地碘片 組成:華素片 英文名:Cydiodine Tablets 華素片(西地碘片)的主要活性成分是分子碘,含量1.5 mg/片。將碘利用分子分散技術制成分子態西地碘,并含適量薄荷腦等 【貯藏】 遮光、密閉、陰涼處保存 【有效期】 二年 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
為了預防碘缺乏癥,國家規定每千克食鹽中應含40~50mg碘酸鉀。碘酸鉀晶體有較高的穩定性,但在酸性溶液中,碘酸鉀是一種較強的氧化劑,能跟某些還原劑作用生成碘;在堿性溶液中,碘酸鉀能被氯氣、次氯酸等強氧化劑氧化為更高價的碘的含氧酸鹽。
【問題1】工業生產碘酸鉀的流程如下: 
(1)碘、氯酸鉀和水混合后的反應為(未配平):I2+KClO3+H2O→KH(IO3)2+KCl+Cl2↑。該方程式配平時,系數有多組,原因是 。
(2)X的化學式為 ;寫出用試劑X調節pH的化學方程式: 。
(3)生產中,如果省去“酸化”、“逐氯”、“結晶①、過濾”這三步操作,直接用試劑X調整反應后溶液的pH,對生產碘酸鉀有什么具體影響? 。
【問題2】已知:KIO3+5KI+3H2SO4→3K2SO4+3I2+3H2O; I2+2S2O32-→2I-+S4O62-。
(4)檢驗加碘食鹽中的碘元素,學生甲利用碘酸鉀與碘化鉀在酸性條件下發生反應。用四氯化碳檢驗碘單質時,看到的明顯現象有 。
(5)測定加碘食鹽中碘的含量,學生乙設計的實驗步驟如下:
a.準確稱取w g食鹽,加適量蒸餾水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入過量KI溶液,使KIO3與KI反應完全;
c.以淀粉為指示劑,加入物質的量濃度為2.0×10-3mol·L-1的Na2S2O3溶液10.0mL恰好反應。
則加碘食鹽樣品中的碘元素含量是 mg/kg(以含w的代數式表示)。
(6)學生丙又對純凈的NaCl(不含KIO3)進行了下列實驗:
| 操作步驟 | 實驗現象 |
| 取1g純凈的NaCl,加3mL水配成溶液。 | 溶液無變化 |
| 滴入5滴淀粉溶液和1mL 0.1 mol·L-1 KI溶液,振蕩。 | 溶液無變化 |
| 然后再滴入1滴1mol·L-1的H2SO4,振蕩。 | 溶液變藍色 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鋇鹽行業生產中排出大量的鋇泥[主要含有BaCO3、BaSiO3、BaSO3、Ba(FeO2)2等]。某主要生產BaCl2、BaCO3、BaSO4的化工廠利用鋇泥制取Ba(NO3)2,其部分工藝流程如下:
(1)酸溶后溶液的pH=1,Ba(FeO2)2與HNO3反應的化學方程式為________。
(2)酸溶時通常控制反應溫度不超過70 ℃,且不使用濃硝酸,原因是________、________。
(3)該廠結合本廠實際,選用的X為________(填化學式);中和Ⅰ使溶液中________(填離子符號)的濃度減小(中和Ⅰ引起的溶液體積變化可忽略)。
(4)上述流程中洗滌的目的是________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業上可以從電解銅的陽極泥中提取很多重要物質,其工藝流程如下: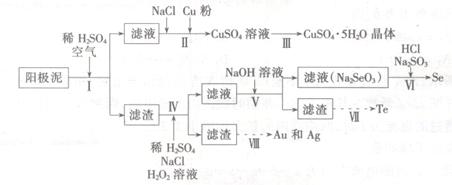
已知:①陽極泥的主要化學成分,如表1所示
表一
| 主要成份 | Cu Ag Au Se Te |
| 百分含量/% | 23.4 12.1 0.9 6.7 3.1 |
| | 固定浸出溫度 | | | 固定H2SO4濃度 |
| H2SO4濃度 mol/L | 浸出率/% | | 浸出溫度/℃ | 浸出率/% |
| Cu Ag Au Se Te | | Cu Ag Au Se Te | ||
| 4 | 95.1 4.67 <0.2 0.83 8.93 | | 30 | 87.1 4.58 <0.2 0.08 6.83 |
| 3 | 94.5 4.65 <0.2 0.28 6.90 | | 40 | 94.5 4.65 <0.2 0.28 6.90 |
| 2 | 78.1 2.65 <0.2 0.05 2.85 | | 50 | 96.1 5.90 <0.2 0.64 8.73 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
溴有“海洋元素”之稱,海水中溴含量為65 mg·L-1。實驗室模擬海水中溴的提取。
實驗方法:將適量新制氯水加入到20 mL富含溴離子的海水中(海水可以用0.1 mol·L-1的NaBr溶液代替),把溴置換出來。氯水中的氯氣作________________劑,涉及反應的離子方程式為__________________。
得到的單質溴可以用有機溶劑在________(儀器)中實現萃取富集,萃取試劑用________、苯等,得到的有機層顯________色。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
如圖所示a、b、c、d分別是幾種常見漏斗的上部,A、B、C、D是實際操作中各漏斗的下部插入容器中的示意圖,請指出A、B、C、D分別與a、b、c、d相匹配的組合,及其組合后裝置在實驗中的應用,例如:C和a組合,用于制取氣體。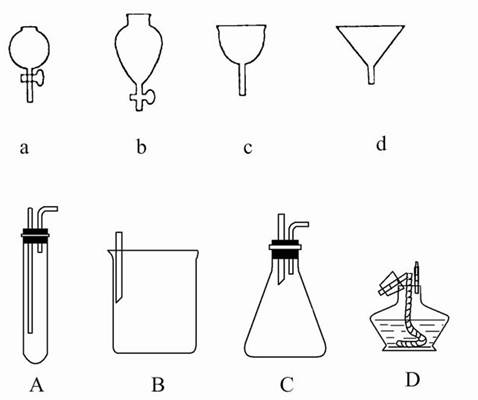
① A與____組合,用于____________________,
② B與____組合,用于____________________,
③ B與____組合,用于____________________,
④ D與____組合,用于____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
為提純含NaCl和Na2SO4兩種雜質的NaNO3溶液,且逐一分離出雜質,某同學設計了如下的實驗流程: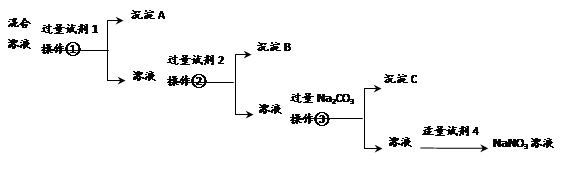
(1)操作①②③的名稱都是________(填操作名稱)。
(2)寫出試劑的名稱:試劑1___________;試劑2_____________。
(3)操作③之前加入Na2CO3的目的是________________________。
(4)加入試劑4后,發生反應的離子方程式為_________________。
控制試劑4的加入量“適量”的方法是_____________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com