

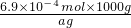 =
=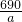 mg;
mg;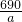 mg;
mg;

 期末1卷素質教育評估卷系列答案
期末1卷素質教育評估卷系列答案科目:高中化學 來源: 題型:
| 690 |
| a |
| 690 |
| a |
查看答案和解析>>
科目:高中化學 來源:2012-2013學年安徽省“江南十校”高三聯考理綜化學試卷(解析版) 題型:實驗題
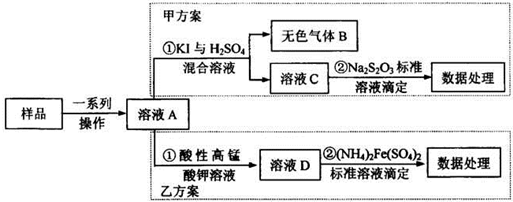
亞硝酸鹽是一祌常見的食品添加劑,使用時必須嚴格控制其用量。為檢測某食品中亞硝酸鹽含量(通常以1kg樣品中含NaNO2的質量計),某研究小組設計了如下兩種實驗方案:
(1)無色氣體B遇空氣顯紅棕色,B的化學式為_______寫出甲方案①中反應的離子方程式_______
(2)完成并配平乙方案①中反應的離子方程式
MnO4-+ NO2-+ = Mn2++ NO3-+ ,
(3)乙方案②中需配置100mL0.0010mol/L(NH4)2Fe(SO4)2標準溶液,在已準確稱量樣品的質量后,還需要的儀器有:量筒、燒杯、_______配制溶液時,定容的操作方法是______
(4)若取樣品ag,按乙方案進行測定,準確量取12.00mL0.0005mol/L的酸性高錳酸鉀 溶液(過童)與溶液A反應。反應后溶液用0.0010mol/L(NH4)2Fe(SO4)2標準溶液滴定至紫色 溶液剛好褪去;重復上述實驗2次,平均消耗(NH4)2Fe(SO4)2溶液10.00mL.則1kg樣品中 NaNO2的質量為_______mg.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com