
【題目】(1)現有A、B、X、Y、Z五種短周期元素,原子序數依次增大。它們的性質或原子結構如下表:
元素 | 性質或原子結構 |
A | 原子核內只有一個質子 |
B | 單質是空氣中含量最多的氣體 |
X | 原子的最外層電子數是次外層電子數的3倍 |
Y | 短周期元素中原子半徑最大的元素 |
Z | 最高正化合價與最低負化合價的代數和為6 |
請回答:
①X元素在元素周期表中的位置是______________;
②Z單質通入Y的最高價氧化物對應水化物的溶液中,可以得到漂白液,相應反應的離子方程式為___________________________________________________;
③化合物甲由A和B兩種元素組成且質量比為3:14,甲與X單質在催化劑、加熱條件下發生的反應是工業上制取硝酸的基礎,寫出該反應的化學方程式____________。
(2)短周期元素X、Y、Z在周期表中的位置關系如圖所示
X | ||
Y | ||
Z |
①X元素單質的化學式是_________,若X核內中子數與質子數相等,則X單質的摩爾質量為________;
②Y單質的電子式是_________;Z與鈣形成的化合物的電子式是__________。
【答案】第二周期第ⅥA族 Cl2+2OH-=Cl-+ClO-+H2O 4NH3+5O2![]() 4NO+6H2O He 4 g/mol
4NO+6H2O He 4 g/mol ![]()
![]()
【解析】
(1)A原子核內只有一個質子,A是H;B單質是空氣中含量最多的氣體,B是N;X原子的最外層電子數是次外層電子數的3倍,X是O;Y是短周期元素中原子半徑最大的元素,Y是Na;Z的最高正化合價與最低負化合價的代數和為6,則Z是Cl;
(2)根據短周期元素X、Y、Z在周期表中的位置關系可知X是He,Y是F,Z是S,據此解答。
(1)①X元素是O,在元素周期表中的位置是第二周期第ⅥA族;
②Z單質即氯氣通入Y的最高價氧化物對應水化物的溶液氫氧化鈉中,可以得到漂白液,相應反應的離子方程式為Cl2+2OH-=Cl-+ClO-+H2O;
③化合物甲由H和N兩種元素組成且質量比為3:14,則原子個數之比是3:1,即甲是氨氣,氨催化氧化反應的化學方程式為4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。
(2)①X元素是He,單質的化學式是He,若X核內中子數與質子數相等,He的質子數是2,因此X單質的摩爾質量為4 g/mol;
②Y單質是F2,電子式是![]() ;S與鈣形成的化合物是離子化合物CaS,電子式是
;S與鈣形成的化合物是離子化合物CaS,電子式是![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】下列有機物在酸性催化條件下發生水解反應, 生成兩種不同的有機物, 且這兩種有機物的相對分子質量相等, 該有機物可能是
A.蔗糖B.麥芽糖C.乙酸乙酯D.甲酸乙酯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碘化鈉在醫藥上用作祛痰劑和利尿劑,也用于治療甲狀腺腫病,生活中用作照相膠片感光劑,碘的助溶劑,也用于配制碘乳劑。某實驗小組用NaOH、單質碘和水合肼(N2H4·H2O)為原料制備碘化鈉。
回答下列問題:
(1)水合肼的制備原理為:NaClO+2NH3=N2H4·H2O+NaCl。
①用下圖裝置組裝制備水合肼,連接順序為_____→ → → → → (用字母表示).
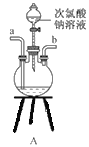
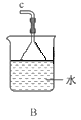
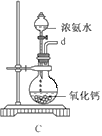
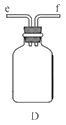
②裝置C中發生反應的化學方程式為________________,裝置D的作用是_______________。
(2)碘化鈉的制備步驟
向三頸燒瓶中加入8.2gNaOH及30mL水,攪拌冷卻,加入25.4g單質碘,開動磁力攪拌器,保持60-70℃至反應充分;繼續加入稍過量的N2H4·H2O(水合肼),還原NaIO和NaIO3,得NaI溶液粗品,同時釋放一種空氣中的某氣體;向上述反應液中加入1.0g活性炭,煮沸半小時,然后將溶液與活性炭分離;將分離出的溶液蒸發濃縮、冷卻結晶、過濾、洗滌、干燥,得產品24.3g。
①反應溫度不宜超過70℃的原因是___________________ ,該步驟反應完全的現象是______________。
②IO-被還原的離子方程式為_______________________________。
③“將溶液與活性炭分離”的方法是____________。
④該實驗小組產率為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是部分短周期主族元素原子半徑與原子序數的關系圖。下列說法正確的是

A. Z、N兩種元素的離子半徑相比,前者大
B. X、N兩種元素的氫化物的沸點相比,前者較低
C. M比X的原子序數多7
D. Z單質均能溶解于Y的氫氧化物和N的氫化物的水溶液中
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素A、B、C、D、E、G的原子序數依次增大,在元素周期表中A的原子半徑最小(稀有氣體元素除外),B與C相鄰且C的最外層電子數是次外層的3倍,C、D的最外層電子數之和與G的最外層電子數相等,E是地殼中含量最多的金屬元素。回答下列問題:
(1)C在元素周期表中的位置是_________周期、_________族;G的元素符號是_________。
(2)B的原子結構示意圖是_________;C與D組成的既含離子鍵又含共價鍵的化合物電子式是_________。
(3)E單質能與D的最高價氧化物的水化物濃溶液反應放出氫氣,反應的化學方程式是__________________;由上述六種元素中的三種組成的某種鹽,水溶液顯堿性,將該鹽溶液滴入硫酸酸化的KI淀粉溶液中,溶液變為藍色,則反應的離子方程式是__________________。
(4)由A、B、C、E中的某些元素組成的化合物X、Y、Z、W有如下轉化關系:

X、Y、Z、W中均由三種元素組成,Z是一種強酸,則Z的化學式是___________,Y溶液與過量W反應的離子方程式是___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:H2(g)+F2(g)![]() 2HF(g)+270kJ,下列說法正確的是( )
2HF(g)+270kJ,下列說法正確的是( )
A. 2L氟化氫氣體分解成1L的氫氣和1L的氟氣吸收270kJ熱量
B. 1mol氫氣與1mol氟氣反應生成2mol液態氟化氫放出的熱量小于270kJ
C. 在相同條件下,1mol氫氣與1mol氟氣的能量總和大于2mol氟化氫氣體的能量
D. 1個氫氣分子與1個氟氣分子反應生成2個氟化氫分子放出270kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中不正確的是()
①向溴乙烷中加入硝酸銀溶液可檢驗溴元素
②順-2-丁烯和反-2-丁烯的加氫產物相同
③苯和溴水混合可制溴苯
④可用銀鏡反應區分甲酸和乙醛
A.只有①和④B.只有②和③C.只有①和③D.①③④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com