
甲醇(CH3OH)是重要的溶劑和替代燃料,工業上用CO和H2在一定條件下制備CH3OH的反應為CO(g)+2H2(g) CH3OH(g) △H。
CH3OH(g) △H。
(1)在體積為1L的恒容密閉容器中,充入2molCO和4molH2,一定條件下發生上述反應,測得CO(g)和CH3OH(g)的濃度隨時間的變化如下圖甲所示。
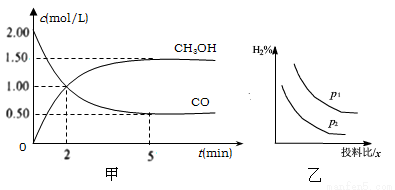
①從反應開始到5min,用氫氣表示的平均反應速率v(H2)=________。
②下列說法正確的是________(填序號)。
A. 達到平衡時,H2的轉化率為75%
B. 5min后容器中壓強不再改變
C. 達到平衡后,再充入氬氣,反應速率增大
D. 2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)某溫度下,在一恒壓容器中分別充入1.2molCO和1molH2,達到平衡時容器體積為2L,且含有0.4molCH3OH(g),則該反應平衡常數的值為_______,此時向容器中再通入0.35molCO氣體,則此平衡將___(填“正向移動”“不移動”或“逆向移動”)
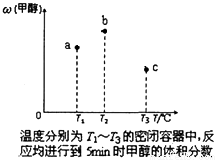
(3)若壓強、投料比x [n(CO)/n(H2)]對反應的影響如圖乙所示,則圖中曲線所示的壓強關系:p1___p2(填“=”“>”或“<”),其判斷理由是__________。
(4)甲醇是一種新型的汽車動力燃料。已知H2(g)、CO(g)、CH3OH(l)的燃燒熱分別為285.8kJ/mol、283.0kJ/mol和726.5kJ/mol,則甲醇不完全燃燒生成一氧化碳和液態水的熱化學方程式為_____。
(5)現有容積均為1L的a、b、c三個密閉容器,往其中分別充入1molCO和2molH2的混合氣體,控制溫度,進行反應,測得相關數據的關系如下圖所示。b中甲醇體積分數大于a中的原因是_____。達到平衡時,a、b、c中CO的轉化率大小關系為___________。
(6)甲醇作為一種燃料還可用于燃料電池。在溫度為650℃的熔融鹽燃料電池中用甲醇、空氣與CO2的混合氣體作反應物,鎳作電極,用Li2CO3和Na2CO3混合物作電解質。該電池的負極反應式為____。
科目:高中化學 來源:2016-2017學年黑龍江省高二下學期開學考試化學試卷(解析版) 題型:填空題
(1)若分子式為C4H6的某烴中所有的碳原子都在同一條直線上,則該烴的結構簡式為_________________。
(2)分子式為C9H20的某烴其一氯代物只有兩種產物,寫出符合要求的結構簡式________________。
(3)分子式為C5H10的烯烴中不存在順反異構的物質有_____種。
(4)已知烯烴、炔烴在臭氧作用下發生以下反應:
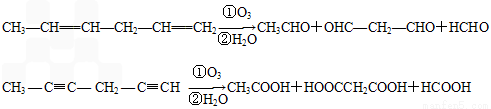
某烴化學式為C10H10,在臭氧作用下發生反應:C10H10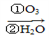 CH3COOH+3HOOC-CHO+CH3CHO ①C10H10分子中含________個雙鍵,________個三鍵。
CH3COOH+3HOOC-CHO+CH3CHO ①C10H10分子中含________個雙鍵,________個三鍵。
②C10H10結構簡式為________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省高一下學期第一次模塊考試化學試卷(解析版) 題型:選擇題
①燒杯②坩堝③蒸發皿④試管⑤蒸餾燒瓶⑥錐形瓶⑦燃燒匙
A. ①⑤⑥ B. ③⑥⑦ C. ①⑤ D. ⑤⑥⑦
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省大連市高二上學期期末考試(理)化學試卷(解析版) 題型:選擇題
下列說法可以證明可逆反應N2+3H2 2NH3已達到平衡狀態的是
2NH3已達到平衡狀態的是
①一個N≡N鍵斷裂的 同時,有6個N-H鍵斷裂
同時,有6個N-H鍵斷裂
②v(H2)=0.6 mol·L-1·min-1,v(NH3)=0.4 mol·L-1·min-1
③保持其他條件不變時,體系壓強不再改變
④NH3、N2、H2的體積分數都不再改變
⑤恒溫恒容時,混合氣體質量保持不變
A. ②③④ B. ①③④ C. ①②④ D. ③④⑤
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省大連市高二上學期期末考試(理)化學試卷(解析版) 題型:選擇題
對于任何一個平衡體系,采用以下措施,一定會使平衡移動的是
A. 升高溫度 B. 加入一種反應物 C. 增大壓強 D. 使用催化劑
查看答案和解析>>
科目:高中化學 來源:2017屆重慶市高三適應性月考(五)理綜化學試卷(解析版) 題型:選擇題
短周期元素X、Y、Z、W、R的原子序數依次增大,Y原子達到穩定結構獲得的電子數目和它的內層電子數目相等,X與Z同主族,Z是所在周期主族元素中原子半徑最大的元素,W的最外層電子數與電子層數相同,R與Z形成的化合物其水溶液呈堿性。下列說法正確的是
A. 離子半徑由大到小的順序為R、Z、Y、W
B. X、Y分別與Z形成的多種化合物中化學鍵類型相同
C. Y、R分別與X形成的化合物沸點依次升高
D. Z、W、R最高價氧化物對應的水化物兩兩之間均能發生反應
查看答案和解析>>
科目:高中化學 來源:2017屆河南省高三3月高考適應性測試理綜化學試卷(解析版) 題型:簡答題
消除氮氧化物污染對優化空氣質境至關重要。
(1)用CH4催化還原氮氧化物消除氮氧化物的污染發生的反應如下:
CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+4NO2(g) 2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ/mol
2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ/mol
若用0.2molCH4將NO2還原為N2,則整個過程中放出的熱量為________kJ。(假設水全部以氣態形式存在)
(2)用活性炭可處理大氣污染物NO。在2L密閉容器中加入NO和活性炭(無雜質),生成氣體E和F。當沮度分別在T1和T2時.測得反應達到平衡時各物質物質的量如下表;
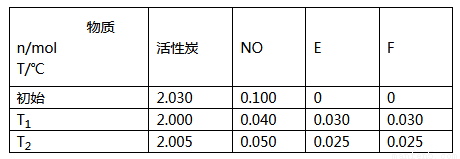
①請結合上表數據.寫出NO與活性炭反應的化學方程式_______________。
②T1℃ 時,上述反應的平衡常數的值為________。如果已知T2>T1,則該反應正反應的△H___(填“>”“<”或“=”)0
③ 在T1溫度下反應達到平衡后,下列措施不能增大NO轉化率的是_______。
a.降低溫度 b.增大壓強 c.增大c(NO) d.移去部分F
(3)汽車尾氣處理中的反應有2NO+2CO 2CO2+N2。某溫度時,在1L密閉容器中充入0.1molCO和0.1mol NO,5s時反應達到平衡,測得NO的濃度為0.02mol/L,則反應開始至平衡時,NO的平均反應速率v(NO)=________。若此溫度下,某時刻測得CO、NO、N2、CO2的濃度分別為0.01mol/L、amol/L、0.01mol/L、0.04mol/L,要使反應向正反應方向進行,a的取值范圍為_____________。
2CO2+N2。某溫度時,在1L密閉容器中充入0.1molCO和0.1mol NO,5s時反應達到平衡,測得NO的濃度為0.02mol/L,則反應開始至平衡時,NO的平均反應速率v(NO)=________。若此溫度下,某時刻測得CO、NO、N2、CO2的濃度分別為0.01mol/L、amol/L、0.01mol/L、0.04mol/L,要使反應向正反應方向進行,a的取值范圍為_____________。
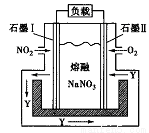
(4)某課題組利用下圖所示裝置,探究NO2和O2化合生成N2O5形成原電池的過程。物質Y的名稱為_______,該電池的正極反應式應為___________。
查看答案和解析>>
科目:高中化學 來源:2017屆湖南省衡陽市高三第二次質檢化學試卷(解析版) 題型:選擇題
下列熱化學方程式書寫正確的
A. 甲烷的燃燒熱為-890 kJ/mol,則甲烷燃燒的熱化學方程式可表示為:CH4(g)+2O2(g)=CO2(g)+ 2H2O(g)△H=-890 kJ/mol
B. 在一定條件下將1 molSO2和0.5molO2置于密閉容器中充分反應,放出熱量79.2kJ,則反應的熱化學方程式為:2SO2(g)+O2(g) 2SO3(g) △H=-158.4kJ·mol-1
2SO3(g) △H=-158.4kJ·mol-1
C. NaOH(s)+1/2H2SO4(濃)=1/2Na2SO4(aq)+H2O(l) △H=-57.3kJ·mol-1
D. 2.00gC2H2氣體完全燃燒生成液態水和二氧化碳氣體放出99.6kJ的熱量,該反應的熱化學方程式為:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2589.6kJ·mol-1
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省七市(州)高三第一次聯合調考(3月聯考)理科綜合化學試卷(解析版) 題型:實驗題
從古至今,鐵及其化合物在人類生產生活中的作用發生了巨大變化。
(1)古代中國四大發明之一的指南針是由天然磁石制成的,其主要成分是______(填字母序號)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
(2)硫酸渣的主要化學成分為:SiO2約45%,Fe2O3約40%,Al2O3約10%,MgO約5%。用該廢渣制取藥用輔料——紅氧化鐵的工藝流程如下(部分操作和條件略):
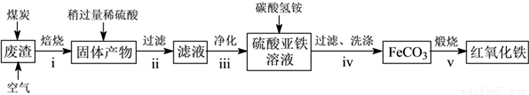
回答下列問題:
①在步驟i中產生的有毒氣體可能有__________________。
②在步驟iii操作中,要除去的離子之一為Al3+。若常溫時Ksp[Al(OH)3]=1.0×10-32,此時理論上將Al3+沉淀完全,則溶液的pH為____________。
③步驟iv中,生成FeCO3的離子方程式是_________________。
(3)氯化鐵溶液稱為化學試劑中的“多面手”,向氯化銅和氯化鐵的混合溶液中加入氧化銅粉末會產生新的沉淀,寫出該沉淀的化學式_________________。請用平衡移動的原理,結合必要的離子方程式,對此現象作出解釋:___________________。
(4)①古老而神奇的藍色染料普魯士藍的合成方法如下:

復分解反應ii的離子方程式是________________。
②如今基于普魯士藍合成原理可檢測食品中CN-,方案如下:
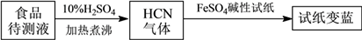
若試紙變藍則證明食品中含有CN-,請解釋檢測時試紙中FeSO4的作用:
_____________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com