
【題目】已知化學(xué)平衡、電離平衡、水解平衡和溶解平衡均符合勒夏特列原理。請(qǐng)回答下列問題:
(1)可逆反應(yīng)FeO(s)+CO(g)![]() Fe(s)+CO2(g)是煉鐵工業(yè)中一個(gè)重要反應(yīng),其溫度與平衡常數(shù)K的關(guān)系如下表:
Fe(s)+CO2(g)是煉鐵工業(yè)中一個(gè)重要反應(yīng),其溫度與平衡常數(shù)K的關(guān)系如下表:
T/K | 938 | 1 100 |
K | 0.68 | 0.40 |
若該反應(yīng)在體積固定的密閉容器中進(jìn)行,在一定條件下達(dá)到平衡狀態(tài),若升高溫度,混合氣體的平均相對(duì)分子質(zhì)量__;充入氦氣,混合氣體的密度__(填“增大”“減小”或“不變”)。
(2)830℃,反應(yīng)CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)的平衡常數(shù)K=1,在2L恒容反應(yīng)器中發(fā)生上述反應(yīng),分別充入3molCO2、2molH2、1molCH3OH、4molH2O(g),反應(yīng)向__方向進(jìn)行。(填“正”、“逆”或“不移動(dòng)”)
CH3OH(g)+H2O(g)的平衡常數(shù)K=1,在2L恒容反應(yīng)器中發(fā)生上述反應(yīng),分別充入3molCO2、2molH2、1molCH3OH、4molH2O(g),反應(yīng)向__方向進(jìn)行。(填“正”、“逆”或“不移動(dòng)”)
(3)25℃時(shí),部分物質(zhì)的電離平衡常數(shù)如表所示:
化學(xué)式 | CH3COOH | NH3·H2O | H2CO3 | H2SO3 |
電離平衡常數(shù) | 1.7×10-5 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.3×10-2 K2=6.3×10-8 |
①寫出CH3COOH的電離方程式____,其電離平衡常數(shù)表達(dá)式K a=___;
②根據(jù)表中數(shù)據(jù)判斷,濃度均為0.01mol·L-1的下列三種物質(zhì)的溶液中,酸性最強(qiáng)的是___(填編號(hào));將下列各溶液分別稀釋100倍,pH變化最小的是___(填編號(hào))。
A.CH3COOH B.H2CO3 C.H2SO3
【答案】減小 增大 正 CH3COOH ![]() H++CH3COO-
H++CH3COO- 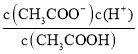 C B
C B
【解析】
(1)根據(jù)表格數(shù)據(jù)可知,升高溫度,平衡常數(shù)減小,說明平衡向逆反應(yīng)方向移動(dòng),據(jù)此分析解答;
(2)首先計(jì)算c(CO2)、c(H2)、c(CH3OH)、c(H2O),再計(jì)算濃度商,與K比較后判斷反應(yīng)的方向;
(3)①CH3COOH為弱酸,據(jù)此書寫電離方程式,并根據(jù)電離方程式書寫電離平衡常數(shù)表達(dá)式;②K越大,酸性越強(qiáng);酸性越強(qiáng),稀釋100倍后pH變化越大,據(jù)此分析解答。
(1)升高溫度,平衡常數(shù)減小,說明平衡向逆反應(yīng)方向移動(dòng),氣體的質(zhì)量減小,物質(zhì)的量不變,混合氣體的平均相對(duì)分子質(zhì)量減小;充入氦氣,反應(yīng)體積不變,氣體質(zhì)量增大,混合氣體的密度增大,故答案為:減小;增大;
(2)c(CO2)=![]() =1.5mol/L,c(H2)=
=1.5mol/L,c(H2)=![]() =1mol/L,c(CH3OH)=
=1mol/L,c(CH3OH)=![]() =0.5mol/L ,c(H2O)=
=0.5mol/L ,c(H2O)=![]() =2mol/L,則濃度商=
=2mol/L,則濃度商=![]() =
=![]() <K=1,反應(yīng)正向進(jìn)行,故答案為:正;
<K=1,反應(yīng)正向進(jìn)行,故答案為:正;
(3)①CH3COOH為弱酸,電離方程式為CH3COOH ![]() H++CH3COO-,電離平衡常數(shù)表達(dá)式K a=
H++CH3COO-,電離平衡常數(shù)表達(dá)式K a=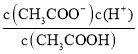 ,故答案為:CH3COOH
,故答案為:CH3COOH ![]() H++CH3COO-;
H++CH3COO-;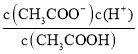 ;
;
②K越大,表示電離程度越大,酸性越強(qiáng),根據(jù)表格數(shù)據(jù)可知,H2SO3的K1最大,因此H2SO3酸性最強(qiáng);酸性越強(qiáng),稀釋100倍后pH變化越大,則pH變化最小的是酸性最弱的H2CO3,故答案為:C;B。


 名校課堂系列答案
名校課堂系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:
【題目】(1)已知反應(yīng)2HI(g)=H2(g)+I2(g)的△H=+11kJ·mol-1,1molH2(g)、1molI2(g)分子中化學(xué)鍵斷裂時(shí)分別需要吸收436kJ、151kJ的能量,則1molHI(g)分子中化學(xué)鍵斷裂時(shí)需吸收的能量為______________kJ。
(2)已知某密閉容器中存在下列平衡:CO(g)+H2O(g)![]() CO2(g)+H2(g),CO的平衡物質(zhì)的量濃度c(CO)與溫度T的關(guān)系如圖所示。
CO2(g)+H2(g),CO的平衡物質(zhì)的量濃度c(CO)與溫度T的關(guān)系如圖所示。
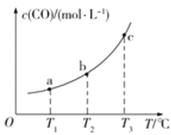
①該反應(yīng)△H_____________0(填“>”或“<”)
②若T1、T2時(shí)的平衡常數(shù)分別為K1、K2,則K1_____________K2(填“>”、“<”或“=”)。
(3)在恒容密閉容器中,加入足量的MoS2和O2,僅發(fā)生反應(yīng):2MoS2(s)+7O2(g)![]() 2MoO3(s)+4SO2(g)ΔH。測(cè)得氧氣的平衡轉(zhuǎn)化率與起始?jí)簭?qiáng)、溫度的關(guān)系如圖所示:
2MoO3(s)+4SO2(g)ΔH。測(cè)得氧氣的平衡轉(zhuǎn)化率與起始?jí)簭?qiáng)、溫度的關(guān)系如圖所示:
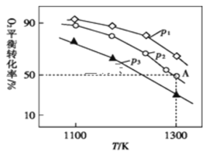
①p1、p2、p3的大小:___________。
②若初始時(shí)通入7.0molO2,p2為7.0kPa,則A點(diǎn)平衡常數(shù)Kp=___________(用氣體平衡分壓代替氣體平衡濃度計(jì)算,分壓=總壓×氣體的物質(zhì)的量分?jǐn)?shù),寫出計(jì)算式即可)。
(4)中科院蘭州化學(xué)物理研究所用Fe3(CO)12/ZSM-5催化CO2加氫合成低碳烯烴反應(yīng),所得產(chǎn)物含CH4、C3H6、C4H8等副產(chǎn)物,反應(yīng)過程如圖。
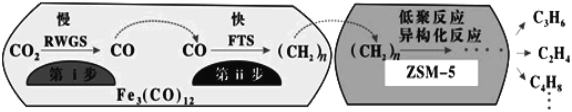
催化劑中添加Na、K、Cu助劑后(助劑也起催化作用)可改變反應(yīng)的選擇性,在其他條件相同時(shí),添加不同助劑,經(jīng)過相同時(shí)間后測(cè)得CO2轉(zhuǎn)化率和各產(chǎn)物的物質(zhì)的量分?jǐn)?shù)如表。
助劑 | CO2轉(zhuǎn)化率(%) | 各產(chǎn)物在所有產(chǎn)物中的占比(%) | ||
C2H4 | C3H6 | 其他 | ||
Na | 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
Cu | 9.8 | 80.7 | 12.5 | 6.8 |
①欲提高單位時(shí)間內(nèi)乙烯的產(chǎn)量,在Fe3(CO)12/ZSM-5中添加_______助劑效果最好;加入助劑能提高單位時(shí)間內(nèi)乙烯產(chǎn)量的根本原因是:___________
②下列說法正確的是______;
a.第ⅰ步的反應(yīng)為:CO2+H2![]() CO+H2O
CO+H2O
b.第ⅰ步反應(yīng)的活化能低于第ⅱ步
c.催化劑助劑主要在低聚反應(yīng)、異構(gòu)化反應(yīng)環(huán)節(jié)起作用
d.Fe3(CO)12/ZSM-5使CO2加氫合成低碳烯烴的ΔH減小
e.添加不同助劑后,反應(yīng)的平衡常數(shù)各不相同
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】三草酸合鐵酸鉀[K3Fe(C2O4)33H2O]是制備負(fù)載型活性鐵催化劑的主要原料。某化學(xué)小組探究用廢鐵屑(含少量-2價(jià)S元素)為原料制備三草酸合鐵(Ⅲ)酸鉀晶體。具體流程如圖:
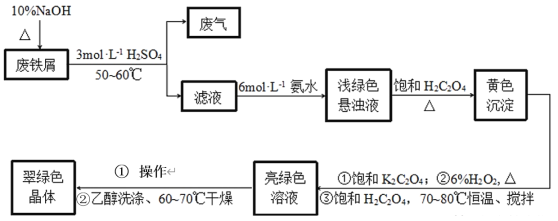
已知:①(NH4)2Fe(SO4)26H2O為藍(lán)綠色晶體,FeC2O4·2H2O為難溶于水的黃色晶體,K3Fe(C2O4)3·3H2O為可溶于水、難溶于乙醇的翠綠色晶體。
②25℃時(shí),[Fe(C2O4)3]3-(aq)+SCN-(aq)![]() [Fe(SCN)]2+(aq)+3C2O
[Fe(SCN)]2+(aq)+3C2O![]() (aq) K=6.31×10-17。
(aq) K=6.31×10-17。
③[Fe(SCN)]2+(aq)為血紅色。
回答下列問題:
(1)三草酸合鐵酸鉀[K3Fe(C2O4)33H2O]中鐵的化合價(jià)是_____。
(2)廢鐵屑中加入10%NaOH并加熱的目的是__。
(3)為防止污染空氣,反應(yīng)所產(chǎn)生的“廢氣”可選擇__凈化處理。(填選項(xiàng))
A.H2O B.NaOH溶液 C.鹽酸 D.CuSO4溶液
(4)寫出淺綠色懸濁液中加入飽和H2C2O4生成黃色沉淀的化學(xué)方程式:__。
(5)制備過程中加入6%H2O2的目的是__,溫度保持70~80℃,采用的合適加熱方式是__。
(6)獲得翠綠晶體的操作①是___。
(7)用乙醇洗滌晶體的原因是___。
(8)某同學(xué)欲檢驗(yàn)所制晶體中的Fe(Ⅲ),取少量晶體放入試管中,加蒸餾水使其充分溶解,再向試管中滴入幾滴0.1molL-1KSCN溶液。請(qǐng)判斷上述實(shí)驗(yàn)方案是否可行并說明理由:___。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】下列關(guān)于熱化學(xué)方程式的說法正確的是
A. H2的燃燒熱為285.8 kJ·mol1,則表示H2燃燒的熱化學(xué)方程式可表示為:H2(g)+ ![]() O2
O2![]() H2O(g) ΔH=285.8 kJ·mol1
H2O(g) ΔH=285.8 kJ·mol1
B. 中和熱為57.3 kJ·mol1,則NaOH與醋酸反應(yīng)的中和熱可以表示如下:NaOH(aq)+CH3COOH(aq)![]() CH3COONa(aq)+H2O(l) ΔH=57.3 kJ·mol1
CH3COONa(aq)+H2O(l) ΔH=57.3 kJ·mol1
C. 已知:C(s,金剛石)+O2(g)![]() CO2(g) ΔH=395.4 kJ·mol1,C(s,石墨)+O2(g)
CO2(g) ΔH=395.4 kJ·mol1,C(s,石墨)+O2(g)![]() CO2(g) ΔH=393.5 kJ·mol1,則C(s,金剛石)
CO2(g) ΔH=393.5 kJ·mol1,則C(s,金剛石)![]() C(s,石墨)ΔH=1.9 kJ·mol1
C(s,石墨)ΔH=1.9 kJ·mol1
D. 已知1 mol CH4完全燃燒生成CO2和液態(tài)水放出890.4 kJ的熱量,則該反應(yīng)中轉(zhuǎn)移1 mol電子時(shí)放出的熱量為222.6 kJ
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】下列說法正確的是___(填序號(hào))。
①將1 mol NaCl溶解在1 L水中,可得1 mol·L-1NaCl的溶液
②將11.2 L HCl氣體通入水配成0.5 L溶液,得到1 mol·L-1的鹽酸
③1 L 10 mol·L-1的鹽酸與9 L水混合,得到1 mol·L-1的鹽酸
④將0.4 g NaOH溶解水中形成100 mL溶液,從中取出10 mL,所取溶液物質(zhì)的量濃度為0.1 mol·L-1(不考慮溶液體積的變化)
⑤將1 mol Na2O溶于水配成1 L溶液,所得溶質(zhì)的物質(zhì)的量濃度為1 mol·L-1(不考慮溶液體積的變化)
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】有人設(shè)計(jì)了如圖所示實(shí)驗(yàn)裝置,目的是做鈉與水反應(yīng)實(shí)驗(yàn),并驗(yàn)證①鈉的物理性質(zhì);②鈉與水反應(yīng)的產(chǎn)物是什么。

(1)當(dāng)進(jìn)行適當(dāng)操作時(shí)還需要的儀器有________。
(2)如何進(jìn)行操作?__________。
(3)實(shí)驗(yàn)現(xiàn)象是_______________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】今年6月比亞迪正式發(fā)布刀片電池,大幅度提高了電動(dòng)汽車的續(xù)航里程可媲美特斯拉,刀片電池采用磷酸鐵鋰技術(shù)。可利用鈦鐵礦[主要成分為FeTiO3(難溶性亞鐵鹽),還含有少量MgO等雜質(zhì)]來制備LiFePO4和Li4Ti5O12等鋰離子電池的電極材料,工藝流程如圖:
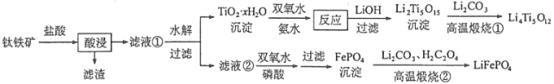
回答下列問題:
(1)“酸浸”后,鈦主要以TiOCl42-形式存在,寫出相應(yīng)反應(yīng)的離子方程式 _______。
(2)TiO2xH2O沉淀與雙氧水、氨水“反應(yīng)”轉(zhuǎn)化成(NH4)2Ti5O15溶液時(shí),Ti元素的浸出率與反應(yīng)溫度的關(guān)系如圖所示:
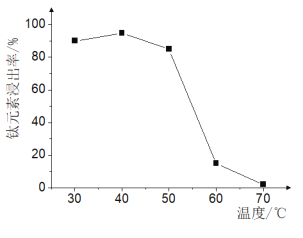
反應(yīng)溫度過高時(shí),Ti元素浸出率變化的原因是 ________。
(3)“濾液②”中含有的金屬離子是 _______;加入雙氧水和磷酸使Fe3+恰好沉淀完全,即溶液中c(Fe3+)=1.0×10-5 mol·L-1,此時(shí)溶液中 c(PO43-)=________。(FePO4的 Ksp=1.3×10 -22)
(4)寫出“高溫煅燒②”中由FePO4制備LiFePO4的化學(xué)方程式______。
(5)Li2Ti5O15中Ti的化合價(jià)為+4,其中過氧鍵的數(shù)目為_____。
(6)作為刀片電池正極材料的磷酸鐵鋰在充、放電時(shí)的局部放大示意圖如圖,則正極電極反應(yīng)式是_________。
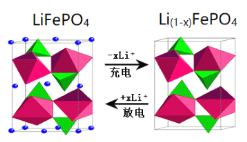
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】在一塊表面無銹的鐵片上滴食鹽水,放置一段時(shí)間后看到鐵片上有鐵銹出現(xiàn)。鐵片腐蝕過程中發(fā)生的總化學(xué)方程式:2Fe+2H2O+O2===2Fe(OH)2,Fe(OH)2進(jìn)一步被氧氣氧化為Fe(OH)3,再在一定條件下脫水生成鐵銹,其原理如圖。下列說法正確的是( )

A. 鐵片發(fā)生還原反應(yīng)而被腐蝕
B. 鐵片腐蝕最嚴(yán)重區(qū)域應(yīng)該是生銹最多的區(qū)域
C. 鐵片腐蝕中負(fù)極發(fā)生的電極反應(yīng):2H2O+O2+4e-===4OH-
D. 鐵片里的鐵和碳與食鹽水形成無數(shù)微小原電池,發(fā)生了電化學(xué)腐蝕
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】(1)①H2(g)+![]() O2(g)= H2O(l) △H= —285.8 kJ/mol
O2(g)= H2O(l) △H= —285.8 kJ/mol
②H2(g)+![]() O2(g)= H2O(g) △H= —241.8kJ/mol
O2(g)= H2O(g) △H= —241.8kJ/mol
③C(s)+![]() O2 (g) = CO (g) △H= —110.5kJ/mol
O2 (g) = CO (g) △H= —110.5kJ/mol
④C(s)+ O2 (g) = CO2 (g) △H= —393.5kJ/mol
回答下列問題:
上述反應(yīng)中屬于放熱的是_________;H2的燃燒熱為________;C的燃燒熱為_____;
(2)汽油的重要成分是辛烷(C8H18),1 mol C8H18(l)在O2(g)中燃燒,生成CO2(g)和H2O(l),放出5518 kJ熱量。請(qǐng)寫出此反應(yīng)的熱化學(xué)方程式___________
(3)由氫氣和氧氣反應(yīng)生成1mol水蒸氣放熱241.8kJ,若1g水蒸氣轉(zhuǎn)化成液態(tài)水時(shí)放熱2.444kJ,試寫出氫氣的燃燒熱的熱化學(xué)方程式________
查看答案和解析>>
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com