
已知:可逆反應N:(g)+3H2(g)![]() 2NH3(g)△H<0。現(xiàn)有甲、乙兩個容積相同且不變的真空密閉容器,向甲容器中加入1mol N2(g)和3mol H2(g),在一定條件下發(fā)生反應,達到平衡時放出熱量為Q1kJ。在相同條件下,向乙容器中加入2mol NH3(g)并發(fā)生反應,達到平衡時吸收熱量為Q2kJ,若Q1=3Q2。下列敘述中正確的是( )
2NH3(g)△H<0。現(xiàn)有甲、乙兩個容積相同且不變的真空密閉容器,向甲容器中加入1mol N2(g)和3mol H2(g),在一定條件下發(fā)生反應,達到平衡時放出熱量為Q1kJ。在相同條件下,向乙容器中加入2mol NH3(g)并發(fā)生反應,達到平衡時吸收熱量為Q2kJ,若Q1=3Q2。下列敘述中正確的是( )
A.達平衡時甲中N:的轉化率為75%
B.達平衡時甲、乙中NH,的體積分數(shù)乙>甲
C.達到平衡后,再向乙中加入0.25mol N2(g)、0.75mol H2(g)和1.5mol NH3(g),平衡向生成N2的方向移動
D.乙中反應的熱化學方程式為2NH3(g)![]() N2(g)+3H2(g)△H=+Q2kJ/mol
N2(g)+3H2(g)△H=+Q2kJ/mol
 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:
 qC(g)在密閉容器中進行.如圖所示反應在不同時間t,溫度T和壓強P與反應物B的體積分數(shù)的關系曲線.根據(jù)圖象填空((1)、(2)、(3)題填“>”、“<”或“=”):
qC(g)在密閉容器中進行.如圖所示反應在不同時間t,溫度T和壓強P與反應物B的體積分數(shù)的關系曲線.根據(jù)圖象填空((1)、(2)、(3)題填“>”、“<”或“=”):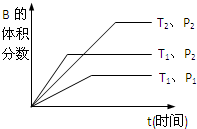
查看答案和解析>>
科目:高中化學 來源: 題型:
 (1)將4molSO2和2molO2充入2L的密閉容器中,在一定條件下發(fā)生反應,經(jīng)10s后達到平衡,測得SO3的濃度為0.6mol?L-1,請回答下列問題:
(1)將4molSO2和2molO2充入2L的密閉容器中,在一定條件下發(fā)生反應,經(jīng)10s后達到平衡,測得SO3的濃度為0.6mol?L-1,請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
 已知某可逆反應:mA(g)+nB(g)?pC(g)△H 在密閉容器器中進行,如圖所示,反應在不同時間t,溫度T和壓強P與反應物B在混合氣體中的百分含量(B%)的關系曲線,由曲線分析下列判斷正確的是( )
已知某可逆反應:mA(g)+nB(g)?pC(g)△H 在密閉容器器中進行,如圖所示,反應在不同時間t,溫度T和壓強P與反應物B在混合氣體中的百分含量(B%)的關系曲線,由曲線分析下列判斷正確的是( )查看答案和解析>>
科目:高中化學 來源: 題型:
 已知某可逆反應:mA(g)+nB(g) xC(g)△H=Q kJ/mol,在密閉容器中進行如圖表
已知某可逆反應:mA(g)+nB(g) xC(g)△H=Q kJ/mol,在密閉容器中進行如圖表查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com