
| A. | 分子中含有三種含氧官能團 | |
| B. | 1 mol 該化合物最多能與5mol NaOH反應 | |
| C. | 既可以發生取代反應,又能夠發生加成反應 | |
| D. | 能與FeCl3發生顯色反應,不能和NaHCO3反應放出CO2 |
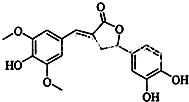
分析 有機物含有酚羥基,可發生取代、氧化和顯色反應,含有酯基,可發生水解反應,酚羥基和酯基都可與氫氧化鈉反應,以此解答該題.
解答 解:A.由結構簡式可知,分子中含有羥基、酯基和醚基三種含氧官能團,故A正確;
B.分子中含有3個酚羥基,1個酯基,故1mol該化合物最多能與4molNaOH反應,故B錯誤;
C.分子中含有苯環,既可以發生取代反應,又能夠發生加成反應,故C正確;
D.含有酚羥基,能與FeCl3發生顯色反應;不含有羧基,故不能與NaHCO3反應放出CO2,故D正確;
故選B.
點評 本題考查有機物的結構和性質,為高考常見題型,側重于學生的分析能力的考查,注意常見有機物的官能團的性質,為解答該類題目的關鍵,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 78gNa2O2與62gNa2O中所含陰離子數目都是NA | |
| B. | 常溫常壓下,NA個Cl2通入水中,轉移電子數為NA | |
| C. | 電解精煉銅時,若陰極得到2NA個電子,則陽極質量減少64g | |
| D. | 5.6g鐵粉與足量硫粉充分反應,轉移電子數為0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
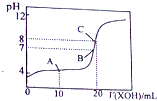 X、Y是元素周期表前20號元素,且X的原子序數比Y大4,請填空(X、Y要用具體的元素符號表示):
X、Y是元素周期表前20號元素,且X的原子序數比Y大4,請填空(X、Y要用具體的元素符號表示):查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2種 | B. | 4種 | C. | 6種 | D. | 8種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銅與濃硫酸反應所得白色固體甲是CuSO4 | |
| B. | 加BaCl2溶液后所得白色沉淀是BaSO3 | |
| C. | 白色固體甲中夾雜的少量黑色物質乙中不可能含有CuO | |
| D. | 白色固體甲中夾雜的少量黑色物質乙中含元素Cu、S |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
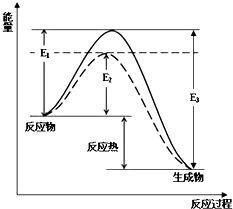 (1)工業合成氨是一個可逆反應:N2(g)+H2(g)?2NH3(g).圖中虛線部分是通過改變化學反應中的條件,請解釋原因:下表為不同溫度下該反應的平衡常數.由此可推知,表中T1<573K(填“>”、“<”或“=”).
(1)工業合成氨是一個可逆反應:N2(g)+H2(g)?2NH3(g).圖中虛線部分是通過改變化學反應中的條件,請解釋原因:下表為不同溫度下該反應的平衡常數.由此可推知,表中T1<573K(填“>”、“<”或“=”). | T/K | T1 | 573 | T3 |
| K | 1.00×107 | 2.54×105 | 1.88×103 |
| pH | <8.0 | 8.0~9.6 | >9.6 |
| 顏色 | 黃色 | 綠色 | 藍色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 液面在“0”刻度時,50 mL堿式滴定管和25 mL堿式滴定管所盛液體的體積,其比值一定為2:1 | |
| B. | 將NaOH溶液和氨水溶液各稀釋一倍,兩者的OH-濃度均減少到原來的二分之一 | |
| C. | 如果鹽酸的濃度是醋酸濃度的二倍,則鹽酸的H+濃度也是醋酸的二倍 | |
| D. | 制取TiO2可用TiCl4加大量水,同時加熱:TiCl4+(x+2)H2O(過量)?TiO2•xH2O↓+4HCl,所得的TiO2•H2O經焙燒得TiO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 兩個反應中均為硫元素被氧化 | |
| B. | 反應①、②中生成等量的I2時轉移電子數比為1:5 | |
| C. | 氧化性:MnO2>SO42->IO3->I2 | |
| D. | 碘元素在反應①中被還原,在反應②中被氧化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com