
(1)根據反應Na2SO3(固)+H2SO4(濃)![]() Na2SO4+SO2↑+H2O,制備SO2氣體。
Na2SO4+SO2↑+H2O,制備SO2氣體。
①用下列簡圖,畫出制備并收集SO2的實驗裝置(含試劑)示意圖。?

②實驗過程中,使用分液漏斗滴加濃硫酸的操作是________________________________。?
(2)將SO2氣體分別通入下列溶液中:?
①品紅溶液,現象是________________________________ 。?
②溴水溶液,現象是________________________________ 。?
(3)有一小組在實驗中發現,SO2氧化產生緩慢,以致后續實驗現象很不明顯,但又不存在氣密性問題。請你推測可能的原因并說明相應的驗證方法(可以不填滿):?
①原因________,驗證方法________________________________。?
②原因________,驗證方法________________________________。?
③原因________,驗證方法________________________________。
科目:高中化學 來源: 題型:閱讀理解
| ||
| ||
| ||
| ||
| ||
| ||


| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
向草酸(H2C2O4)溶液中逐滴加入酸性高錳酸鉀溶液時,溶液褪色總是先慢后快。對其原因,某研究性學習小組結合化學反應原理提出猜想與假設,并設計了一系列實驗進行探究:
實驗(1):在兩支試管中分別加入10mL等濃度的草酸溶液,在②號試管中加入少量硫酸錳固體。然后在兩支試管中分別加入5滴0.1 mol·L-1的硫酸酸化高錳酸鉀溶液。現象如下(表1)
|
| ①號試管 | ②號試管 |
| 加入藥品 | 草酸溶液 硫酸酸化高錳酸鉀溶液 | 草酸溶液 硫酸酸化高錳酸鉀溶液 硫酸錳固體 |
| 實驗現象(褪色時間) | 溶液褪色很慢(30s) | 溶液褪色很快(2s) |
實驗(2):在兩支試管中分別加入5 mL等濃度的草酸溶液,在②號試管中再滴加10滴稀硫酸,然后各加入5滴0.1mol·L-1的高錳酸鉀溶液。現象如下(表2)
| 編號 | ①號試管 | ②號試管 |
| 褪色時間 現象 | 100 s | 90 s |
| 均有氣泡產生;②號試管的溶液褪色比①號試管的溶液快,它們顏色變化如下:紫紅色→紅色→橙紅色→橙色→黃色→無色。 |
實驗(3):取3支試管分別加入5 mL等濃度草酸溶液,然后在①、②、③號試管中依次加入10滴、1 mL、2 mL稀硫酸溶液,各加入5滴0.1 mol·L-1的高錳酸鉀溶液,然后置于溫度為65℃的水浴中加熱。觀察現象(表3)。
| 編號 | ①號試管 | ②號試管 | ③號試管 |
| 褪色時間
實驗現象 | 80 s | 100 s | 120 s |
| 均有氣泡產生;①號試管的溶液褪色比②、③號試管的溶液快,它們顏色變化如下:紫紅色→紅色→橙紅色→橙色→黃色→無色。 |
(1) 該研究性學習小組的實驗目的是 。
(2)該研究性學習小組進行實驗時所用的方法是科學實驗中常用的一種方法,該方法叫 法;
(3)實驗(1)得出的結論是 。
(4)由實驗(2)和實驗(3)得出的結論是(寫三點)
_________________________,_____________________,_______________;
(5)據有關現象寫出草酸溶液與酸性高錳酸鉀溶液反應的離子方程式:
H2C2O4+ MnO4—+ = Mn2++ + H2O
查看答案和解析>>
科目:高中化學 來源:2012-2013學年湖北武漢部分重點中學高一上學期期末考試化學試卷(帶解析) 題型:實驗題
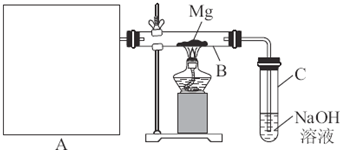
S2C12是一種金黃色易揮發的液體,具有強烈的窒息性,在工業生產上可用于橡膠的硫化。為在實驗室合成S2C12,某化學研究性學習小組進行了以下探究。 【查閱資料】① 干燥的氯氣在110℃~140℃與硫反應,即可得到S2C12。② S的熔點為112.8℃、沸點為444.6℃;S2C12的熔點為
【查閱資料】① 干燥的氯氣在110℃~140℃與硫反應,即可得到S2C12。② S的熔點為112.8℃、沸點為444.6℃;S2C12的熔點為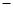 76℃、沸點為138℃。
76℃、沸點為138℃。
③ S2C12+C12 2SCl2。④ S2C12易和水發生反應,生成H2S、SO2、H2SO3、H2SO4等。⑤ClO3-+5Cl-+6H
2SCl2。④ S2C12易和水發生反應,生成H2S、SO2、H2SO3、H2SO4等。⑤ClO3-+5Cl-+6H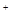 =3C12↑+3H2O 請回答下列問題:
=3C12↑+3H2O 請回答下列問題: 【實驗裝置設計】
【實驗裝置設計】
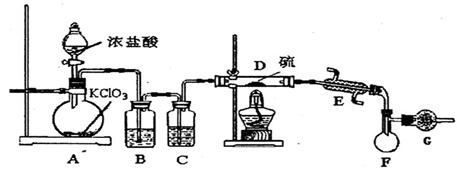

 (1)B中所放試劑為 ; C中所放試劑為 。
(1)B中所放試劑為 ; C中所放試劑為 。 (2)在加熱D時溫度不宜過高,其原因是 ;
(2)在加熱D時溫度不宜過高,其原因是 ;
為了提高S2C12的純度,關鍵的操作是控制好溫度和 ; (3)G裝置的作用是 ;
(3)G裝置的作用是 ;
(4)寫出工業上制漂白粉的化學方程式 ;
查看答案和解析>>
科目:高中化學 來源:2010年廣東省高二上學期期中考試化學卷 題型:填空題
向草酸(H2C2O4)溶液中逐滴加入酸性高錳酸鉀溶液時,溶液褪色總是先慢后快。對其原因,某研究性學習小組結合化學反應原理提出猜想與假設,并設計了一系列實驗進行探究:
實驗(1):在兩支試管中分別加入10mL等濃度的草酸溶液,在②號試管中加入少量硫酸錳固體。然后在兩支試管中分別加入5滴0.1 mol·L-1的硫酸酸化高錳酸鉀溶液。現象如下(表1)
|
|
①號試管 |
②號試管 |
|
加入藥品 |
草酸溶液 硫酸酸化高錳酸鉀溶液 |
草酸溶液 硫酸酸化高錳酸鉀溶液 硫酸錳固體 |
|
實驗現象(褪色時間) |
溶液褪色很慢(30s) |
溶液褪色很快(2s) |
實驗(2):在兩支試管中分別加入5 mL等濃度的草酸溶液,在②號試管中再滴加10滴稀硫酸,然后各加入5滴0.1 mol·L-1的高錳酸鉀溶液。現象如下(表2)
|
編號 |
①號試管 |
②號試管 |
|
褪色時間 現象 |
100 s |
90 s |
|
均有氣泡產生;②號試管的溶液褪色比①號試管的溶液快,它們顏色變化如下:紫紅色→紅色→橙紅色→橙色→黃色→無色。 |
實驗(3):取3支試管分別加入5 mL等濃度草酸溶液,然后在①、②、③號試管中依次加入10滴、1 mL、2 mL稀硫酸溶液,各加入5滴0.1 mol·L-1的高錳酸鉀溶液,然后置于溫度為65℃的水浴中加熱。觀察現象(表3)。
|
編號 |
①號試管 |
②號試管 |
③號試管 |
|
褪色時間
實驗現象 |
80 s |
100 s |
120 s |
|
均有氣泡產生;①號試管的溶液褪色比②、③號試管的溶液快,它們顏色變化如下:紫紅色→紅色→橙紅色→橙色→黃色→無色。 |
(1) 該研究性學習小組的實驗目的是 。
(2)該研究性學習小組進行實驗時所用的方法是科學實驗中常用的一種方法,該方法叫 法;
(3)實驗(1)得出的結論是 。
(4)由實驗(2)和實驗(3)得出的結論是(寫三點)
_________________________,_____________________,_______________;
(5)據有關現象寫出草酸溶液與酸性高錳酸鉀溶液反應的離子方程式:
H2C2O4+ MnO4—+ = Mn2++ + H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com