
【題目】試推測第 82 號元素 X 的單質及其化合物不可能具有的性質:
A. X 的氧化物的水化物可能有兩種
B. 單質是能導電的固體
C. 單質不能與氫氣直接化合
D. X 是非金屬元素
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】A、B、D、E、F五種元素的原子序數依次增大,除F為過渡元素外,其余四種均是短周期元素。已知:①F的單質為生活中最常見的金屬之一,原子最外層有2個電子;②E原子的價電子排布為msnmpn,B原子的核外L層電子數為奇數;③A、D原子p軌道的電子數分別為2和4.請回答下列問題:
(1)F的穩定價態離子的電子排布式是__________________________;A、B、D、E四種元素的第一電離能由大到小的順序為________________(用元素符號表示)。
(2)對于B的簡單氫化物,其中心原子的軌道雜化類型是________________。分子的立體構型為________________,該氫化物易溶于D的簡單氫化物的主要原因是________________。
(3)D原子分別與A、B原子形成的單鍵中,鍵的極性較強是________________(用具體的化學鍵表示)。
(4)如圖所示的晶胞是由AD兩元素組成的,下列有關該晶體的說法中正確的是_______。

a.該晶體的化學式為AD
b.該晶體中A、D原子間形成的是雙鍵
c.該晶體熔點可能比SiO2晶體高
d.該晶體可溶于水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【化學——選修2:化學與技術】
元素鋁是在生產、生活中應用廣泛的金屬元素。
(1)氧化鋁是一種耐高溫材料,也是工業上制取鋁的原料。從鋁土礦(主要成分是Al2O3,含SiO2、Fe2O3、MgO等雜質)中提取氧化鋁的兩種工藝流程如下圖所示:
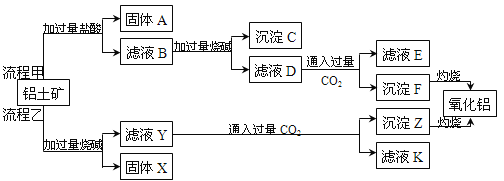
體A的主要成分是 (填化學式,下同),固體X的主要成分是 。
②濾液E中溶質的主要成分是 ,寫出該溶質的一種用途: 。
③在濾液D中通入過量CO2時反應的離子方程式為 。
(2)工業上電解氧化鋁冶煉鋁時加入冰晶石(Na3AlF6)的作用是 。在電解池的工作過程中,需要不斷補充陽極材料(石墨),原因是 。
(3)一種新型高效凈水劑PAFC——聚合氯化鐵鋁[AlFe(OH)nCl6-n]m(n<5,m<10)可廣泛應用于日常生活用水和工業污水的處理。下列有關PAFC的說法正確的是 (填序號)。
A.PAFC中鐵元素顯+2價
B.PAFC用于凈水時,比用相同物質的量的氯化鋁和氯化鐵的pH改變小
C.PAFC可看作一定比例的氯化鐵與氯化鋁水解的中間產物
D.PAFC在強酸性或強堿性溶液中都能穩定存在
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氧氣(O2)和臭氧(O3)是氧元素的兩種同素異形體,已知熱化學方程式:
4Al(s)+3O2(g)===2Al2O3(s) ΔH1
4Al(s)+2O3(g)===2Al2O3(s) ΔH2
3O2(g)===2O3(g) ΔH3則( )
A.ΔH1-ΔH2=ΔH3
B.ΔH1+ΔH2=ΔH3
C.ΔH2-ΔH1=ΔH3
D.ΔH2+ΔH1+ΔH3=0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將一定質量的Mg、Zn、Al混合物與足量稀H2SO4反應,生成H22.8L(標準狀況),原混合物質量可能是( )
A. 2g B. 4g C. 10g D. 12g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖表示4個碳原子相互結合的幾種方式。小圓球表示碳原子,小棍表示化學鍵,假如碳原子上其余的化學鍵都是與氫結合,則下列說法正確的是 ( )
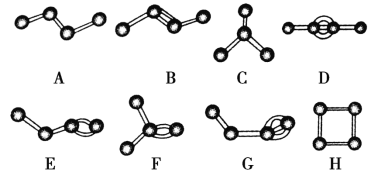
A.圖中屬于烷烴的是A、C、H
B.圖中C和F分子中氫原子數相同
C.圖中物質碳元素的質量分數最大的是C
D.圖中與B互為同分異構體的有E、F、H
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D是四種常見的有機物,其中A是一種氣態烴,在標準狀況下的密度為1.25 g/L;B與C在濃硫酸和加熱條件下發生反應,生成的有機物有特殊香味;A、B、C、D在一定條件下的轉化關系如圖所示(反應條件已省略):
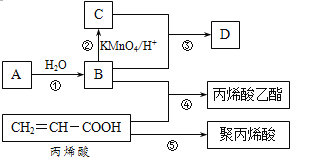
(1)A的電子式為___________,C中官能團的名稱為__________。
(2)丙烯酸(CH2=CH-COOH)的性質可能有_______________。
A.加成反應
B.取代反應
C.加聚反應
D.中和反應
E.氧化反應
(3)用兩種方法鑒別B和C,所用試劑分別是___________、___________。
(4)丙烯酸乙酯的結構簡式為 。
(5)寫出下列反應方程式和有機反應基本類型:
①____________________ _ _______,_________反應;
④____________________ _ _______,_________反應;
⑤____________________ _ _______,_________反應。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】運用化學反應原理分析解答以下問題:
(1)弱酸在水溶液中存在電離平衡,部分0.1 mol·L-1弱酸的電離平衡常數如下表:
弱酸 | 電離平衡常數(25 ℃) |
HClO | K=2.98×10-8 |
H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
H2SO3 | K1=1.54×10-2 K2=1.02×10-7 |
①當弱酸的濃度一定時,降低溫度,K值________(填“變大”“變小”或“不變”)。
②下列離子方程式和有關說法錯誤的是____________。
a.少量的CO2通入次氯酸鈉溶液中:2ClO-+H2O+CO2===2HClO+CO32-
b.少量的SO2通入碳酸鈉溶液中:SO2+H2O+2CO32-===2HCO3-+SO32-
c.相同溫度時,等物質的量濃度的三種弱酸與足量NaOH溶液完全中和消耗NaOH的體積為V(H2CO3)>V(H2SO3)>V(HClO)
d.相同溫度時,等pH三種鹽溶液的物質的量濃度關系:c(Na2CO3)<c(NaClO)<c(Na2SO3)
③亞硒酸(H2SeO3)也是一種二元弱酸,有較強的氧化性。往亞硒酸溶液中不斷通入SO2會產生紅褐色單質,寫出該反應的化學方程式:___ 。
(2)工業廢水中常含有一定量的Cr2O72-和CrO42-,它們對人類及生態系統會產生很大損害,必須進行處理后方可排放。
①在廢水中存在平衡:2CrO42- (黃色)+2H+![]() Cr2O72- (橙色)+H2O。若改變條件使上述平衡向逆反應方向移動,則下列說法正確的是_______。
Cr2O72- (橙色)+H2O。若改變條件使上述平衡向逆反應方向移動,則下列說法正確的是_______。
a.平衡常數K值可以不改變
b.達到新平衡CrO42-的消耗速率等于Cr2O72-的消耗速率
c.達到新平衡后,溶液pH一定增大
d.再達平衡前逆反應速率一定大于正反應速率
②Cr2O72-和CrO42-最終生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) ![]() Cr3+(aq)+3OH-(aq),常溫下Cr(OH)3的Ksp=10-32,當c(Cr3+)降至10-3 mol·L-1,溶液的pH調至4時,________(填“有”或“沒有”)沉淀產生。
Cr3+(aq)+3OH-(aq),常溫下Cr(OH)3的Ksp=10-32,當c(Cr3+)降至10-3 mol·L-1,溶液的pH調至4時,________(填“有”或“沒有”)沉淀產生。
(3)已知:①2CH3OH(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
②CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
③CO(g)+H2O(g) ![]() CO2(g)+H2(g)
CO2(g)+H2(g)
某溫度下三個反應的平衡常數的值依次為K1、K2、K3,則該溫度下反應3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g)的化學平衡常數K=________(用含K1、K2、K3的代數式表示)。向某固定體積的密閉容器中加入3 mol CO和3 mol H2,充分反應后恢復至原溫度,測定容器的壓強為反應前的1/2,則CO的轉化率為_________。
CH3OCH3(g)+CO2(g)的化學平衡常數K=________(用含K1、K2、K3的代數式表示)。向某固定體積的密閉容器中加入3 mol CO和3 mol H2,充分反應后恢復至原溫度,測定容器的壓強為反應前的1/2,則CO的轉化率為_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com