
【題目】某溫度時在2L容器中X、Y、Z三種氣體物質的物質的量(n)隨時間(t)變化的曲線如下圖所示,由圖中數據分析: 
(1)該反應的化學方程式為:
(2)反應開始至2min,用Z表示的平均反應速率為
(3)下列敘述能說明上述反應達到化學平衡狀態的是(填序號)
A.混合氣體的總物質的量不隨時間的變化而變化
B.混合氣體的壓強不隨時間的變化而變化
C.單位時間內每消耗3mol X,同時生成2mol Z
D.混合氣體的總質量不隨時間的變化而變化.
【答案】
(1)3X+Y?2Z
(2)0.05mol/(L?min)
(3)AB
【解析】解:(1)由圖象可以看出,反應中X、Y的物質的量減少,應為反應物,Z的物質的量增多,應為生成物,當反應進行到2min時,△n(X)=0.3mol,△n(Y)=0.1mol,△n(Z)=0.2mol,則△n(X):△n(Y):△n(Z)=3:1:2,參加反應的物質的物質的量之比等于化學計量數之比,則反應的方程式為:3X+Y2Z,所以答案是:3X+Y2Z;(2)反應開始至2min末,Z的反應速率v= ![]() =
= ![]() =
= ![]() =0.05mol/(Lmin),所以答案是:0.05mol/(Lmin);(3)A、反應前后氣體物質的量不同,所以氣體物質的量不變,能說明反應達到平衡狀態,故A正確; B、反應前后氣體物質的量不同,所以混合氣體的壓強不變,能說明反應達到平衡狀態,故B正確;
=0.05mol/(Lmin),所以答案是:0.05mol/(Lmin);(3)A、反應前后氣體物質的量不同,所以氣體物質的量不變,能說明反應達到平衡狀態,故A正確; B、反應前后氣體物質的量不同,所以混合氣體的壓強不變,能說明反應達到平衡狀態,故B正確;
C.單位時間內每消耗3mol X,同時生成2mol Z,都是正反應,無論是否平衡,其速率之比等于化學計量數之比,不能說明反應達到平衡狀態,故C錯誤;
D.據質量守恒定律,氣體質量始終不變,故D錯誤;
故選AB.
【考點精析】本題主要考查了反應速率的定量表示方法和化學平衡狀態的判斷的相關知識點,需要掌握反應速率的單位:mol/(L·min)或mol/(L·s) v=△c-△t;狀態判斷:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不變④若A、B、C、D為氣體,且m+n≠x+y,壓強恒定⑤體系顏色不變⑥單位時間內某物質內化學鍵的斷裂量等于形成量⑦體系平均式量恒定(m+n ≠ x+y)等才能正確解答此題.


科目:高中化學 來源: 題型:
【題目】常溫下,取pH=2的鹽酸和醋酸溶液各100mL,向其中分別加入適量的Zn粒,反應過程中兩溶液的pH變化如右圖所示。下列說法不正確的是
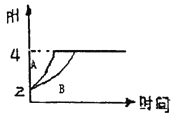
A. 圖中表示醋酸溶液中pH變化曲線的是B
B. 設鹽酸和醋酸中加入的Zn質量分別為m1、m2,則m1<m2
C. pH=2時鹽酸和醋酸的物質的量前者小
D. pH=4時兩溶液c(Zn2+)相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】20℃時,飽和NaCl溶液密度為1.1g.cm-3,物質的量濃度為5.0mol·L-1,下列說法不正確的是
A. 25℃時,飽和NaCl溶波的物質的量濃度大于5.0mol/L
B. 20℃時,飽和NaCl溶液的質量分數約為26.6%
C. 20℃時,密度小于1.1g/cm3的NaCl溶液是不飽和溶液
D. 將此飽和NaCl溶液蒸發部分水,再恢復到20℃時,溶液密度一定大于1.1g/cm3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】表為元素周期表的一部分,請用化學用語回答有關問題:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ⑨ | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①和⑧的元素符號是和;
(2)元素⑥形成的氫化物的電子式是;
(3)表中能形成兩性氫氧化物的元素是(填寫元素符號),請寫出該元素的氫氧化物與⑨最高價氧化物對應的水化物發生反應的化學方程式 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關材料用途的說法中不正確的是( )。
A.氧化鋁陶瓷可用作高壓鈉燈的燈管
B.氮化硅陶瓷可用作陶瓷發動機的材料
C.光導纖維可用作遙測遙控、照明等
D.氧化鋁陶瓷可用作半導體材料
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com