
【題目】如圖,用2mL95%的乙醇,3mL無水醋酸,2mL濃H2SO4,制某有機溶劑的反應裝置,試管b中加入5mL飽和碳酸鈉溶液。連接好裝置。用酒精燈對試管a加熱,當觀察到試管b中有明顯現象時停止實驗。

(1)在大試管a中配制一定比例的乙醇、乙酸和濃硫酸的混合液的方法是:_______________
(2)寫出a試管中的主要化學反應的方程式:________________
(3)加入濃H2SO4的作用是_____________________。
(4)實驗中球形干燥管除起冷凝作用外,另一個重要作用是___________________________。
(5)試管b中發生的反應_____________________________(離子方程式)
(6)生成乙酸乙酯的反應是可逆反應,反應物不能完全變成生成物,反應一段時間后,就達到了該反應的限度,也即達到化學平衡狀態。下列描述能說明乙醇與乙酸的酯化反應已達到化學平衡狀態的有(填序號)______。
①單位時間里,生成1mol乙酸乙酯,同時生成1mol水
②單位時間里,生成1mol乙酸乙酯,同時生成1mol乙酸
③單位時間里,消耗1mol乙醇,同時消耗1mol乙酸
④正反應的速率與逆反應的速率相等
⑤混合物中各物質的濃度不再變化
(7)現擬分離含乙酸、乙醇和水的乙酸乙酯粗產品,下圖是分離操作步驟流程圖,圖中圓括號表示加入適當的試劑,編號表示適當的分離方法。

①寫出各有機物的名稱:
A __________________,B ____________________ ,E __________________ 。
②寫出加入的試劑:(a)________________,(b)___________________。
③寫出有關的操作分離方法:①______________③_________________。
【答案】先往試管中加入乙醇,慢慢加入濃硫酸,冷卻后,再加入醋酸 CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 催化劑、吸水劑 防止倒吸 2CH3COOH + CO32- = 2CH3COO- + H2O +CO2↑ ②④⑤ 乙酸乙酯 乙酸鈉、乙醇 乙醇 飽和碳酸鈉溶液 硫酸 分液 蒸餾
CH3COOCH2CH3+H2O 催化劑、吸水劑 防止倒吸 2CH3COOH + CO32- = 2CH3COO- + H2O +CO2↑ ②④⑤ 乙酸乙酯 乙酸鈉、乙醇 乙醇 飽和碳酸鈉溶液 硫酸 分液 蒸餾
【解析】
(1)在大試管中配制一定比例的乙醇、乙酸和濃硫酸的混合液的方法是先在試管中加入一定量的乙醇,然后邊加邊振蕩試管將濃硫酸慢慢加入試管,最后再加入乙酸;故答案為:先往試管中加入乙醇,慢慢加入濃硫酸,冷卻后,再加入醋酸;
(2)乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水,同時該反應可逆,反應的方程式為CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;故答案為:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;故答案為:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(3)酯化反應需濃硫酸作催化劑,該反應為可逆反應,濃硫酸吸水利于平衡向生成乙酸乙酯方向移動;故答案為:催化劑、吸水劑;
(4)a試管受熱不均,試管b中的導管伸入液面下可能發生倒吸,球形干燥管由于容積較大,可防止倒吸,故答案為:防止倒吸;
(5)隨乙酸乙酯揮發出來的乙酸會與碳酸鈉反應,故答案為:2CH3COOH + CO32- = 2CH3COO- + H2O +CO2↑;
(6)①用不同物質的速率表示達到平衡,要求反應方向一正一逆,且速率之比=化學計量數之比,生成1mol乙酸乙酯和1mol水,反應方向都是向正反應方向進行,故①不能說明反應達到平衡狀態;
②單位時間里,生成1mol乙酸乙酯,同時生成1mol乙酸,說明正反應速率與逆反應達到相等,反應達到平衡狀態;
③單位時間里,消耗1mol乙醇,同時消耗1mol乙酸,均指正反應速率,不能說明正逆反應速率相等,故不能說有反應達到平衡狀態;
④正反應的速率與逆反應的速率相等時,可逆反應達到平衡狀態;
⑤混合物中各物質的濃度不再變化時,說明可逆反應達到平衡狀態;
故答案為:②④⑤;
(7)①由分離流程可知,分離粗產品乙酸乙酯、乙酸和乙醇的混合物,加入飽和碳酸鈉溶液,乙酸乙酯不溶于飽和碳酸鈉,采用分液的方法分離,則A為乙酸乙酯,B為水層含有乙醇、乙酸鈉,利用蒸餾方法分離出乙醇,水層中的乙酸鈉要用硫酸反應得到乙酸,再蒸餾得到乙酸,故E為乙醇,C為乙酸鈉,D為乙酸和硫酸鈉的混合液;故答案為:乙酸乙酯; 乙酸鈉、乙醇;乙醇;
②試劑a是飽和碳酸鈉溶液,試劑b將乙酸鈉轉化為乙酸,且不揮發,則試劑b是硫酸;故答案為:飽和碳酸鈉溶液、硫酸;
③由上述分析可知,操作①是分液,操作③是蒸餾;故答案為:分液、蒸餾;


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】t ℃時,將一定量的混合氣體在密閉容器中發生反應:aA(g)+bB(g) ![]() cC(g)+dD(g),平衡后測得B氣體的濃度為0.6 mol·L-1。恒溫下,將密閉容器的容積擴大1倍,重新達到平衡后,測得B氣體的濃度為0.4 mol·L-1。下列敘述中正確的是
cC(g)+dD(g),平衡后測得B氣體的濃度為0.6 mol·L-1。恒溫下,將密閉容器的容積擴大1倍,重新達到平衡后,測得B氣體的濃度為0.4 mol·L-1。下列敘述中正確的是
A. 重新達到平衡時,D的體積分數減小 B. a+b<c+d
C. 重新達到平衡時,A氣體的濃度增大 D. 平衡向右移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種以肼(N2H4)為燃料的新型環保電池的工作原理如圖所示。下列說法正確的是
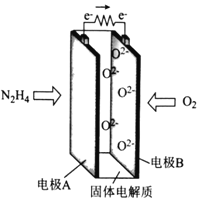
A. 電極A的電勢比電極B的低
B. 電極A的電極反應式為N2H4-4e-+4OH-===N2+4H2O
C. 電極B發生氧化反應
D. 每消耗11.2L的O2,轉移的電子數為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨是一種重要的化工原料,可以用來制備氮化硅(Si3N4)肼(N2H4)、氫氰酸(HCN)。
(1)已知:Si(s)+2Cl2(g)====SiCl4(g) △H1=akJ·mol-1
N2(g)+3H2(g) ![]() 2NH3(g) △H2=bkJ·mol-1
2NH3(g) △H2=bkJ·mol-1
3Si(s)+2N2(g)====Si3N4(s) △H3=ckJ·mol-1
H2(g)+Cl2(g)====2HCl(g) △H4=dkJ·mol-1
則反應3SiCl4(g)+4NH3(g)====Si3N4(s)+12HCl(g)的△H=________________kJ·mol-1(用a、b、c、d表示)。
(2)肼的制備方法是用次氯酸鈉氧化過量的氨。
已知ClO-水解的方程式為:ClO-+H2 O=HClO+OH-。常溫下,該水解反應的平衡常數為K=1.0×10-6mol·L-1,則1.0mol· L -1NaCIO溶液的pH=________。
(3)工業上利用氨氣生產氫氰酸(HCN)的反應為:CH4(g)+NH3(g) ![]() HCN(g)+3H2 (g) △H>O
HCN(g)+3H2 (g) △H>O
①其他條件一定,達到平衡時NH3轉化率隨外界條件X變化的關系如圖所示。X代表的是________(填“溫度”或“壓強”)。
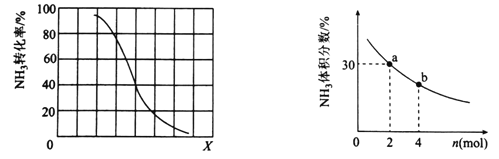
②其他條件一定,向2L密閉容器中加人 n mol CH4和2 mol NH3,平衡時NH3體積分數隨n變化的關系如圖所示。若反應從開始到a點所用時間為10min,該時間段內用CH4的濃度變化表示的反應速率為________mol·L-1·min-1;平衡常數:K(a) ________K(b)(填“>”“=”或“<”)
③工業上用電解法處理含氰電鍍廢水(pH=10)的裝置如圖所示。
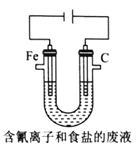
陽極產生的氯氣與堿性溶液反應生成ClO-,ClO-將CN-氧化的離子方程式為:_____CN-+ _____ClO-+ ________====_____CO32-+_____N2↑+________+________若電解處理2 mol CN-,則陰極產生氣體的體積(標準狀況下)為________L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,濃度均為1mol/L的A2和B2兩種氣體,在密閉容器內反應生成氣體C,達平衡后,測得:c(A2)=0.58mol/L,c(B2)=0.16mol/L,c(C)=0.84mol/L,則該反應的正確表達式為
A. 2A2+B2![]() 2A2B B. A2+2B2
2A2B B. A2+2B2![]() 2AB2
2AB2
C. A2+B2![]() A2B2 D. A2+B2
A2B2 D. A2+B2![]() 2AB
2AB
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖甲和乙是雙液原電池裝置。由圖可判斷下列說法錯誤的是( )

A. 乙圖電池反應的離子方程式為:Co(s)+2Ag+(aq)=2Ag(s)+Co2+(aq)
B. 反應2Ag(s)+Cd2+(aq)=Cd(s)+2Ag+(aq) 不能發生
C. 鹽橋的作用是形成閉合回路,并使兩邊溶液保持電中性
D. 甲圖當有1mol電子通過外電路時,正極有59g Co析出
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A、B、D、E均為化學中的常見物質,它們之間的轉化關系如圖所示(部分產物略去),則下列有關物質的推斷不正確的是( )

A. 若A是鐵,則E可能為稀硝酸
B. 若A是CuO,E是碳,則B為CO
C. 若A是NaOH溶液,E是CO2,則B為NaHCO3
D. 若A是AlCl3溶液,E可能是氨水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨原子序數的遞增,八種短周期元素(用英文小寫字母表示)原子半徑的相對大小、最高正價或最低負價的變化如下圖所示。
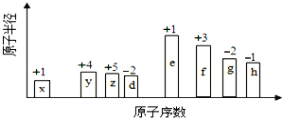
根據判斷出的元素回答問題:
(1)f在元素周期表的位置是_________________。
(2)比較d、e簡單離子的半徑大小(用化學式表示,下同)_____________;比較g、h的最高價氧化物對應的水化物的酸性強弱是______________。
(3)任選上述元素組成一種四原子共價化合物,寫出其電子式________________。
(4)已知1mol e的單質在足量d2中燃燒,恢復至室溫,放出255.5kJ熱量,寫出該反應的熱化學方程式:____________________________________________。
(5)由元素f、h形成的物質X與由元素x、z形成的化合物Y可發生以下反應:
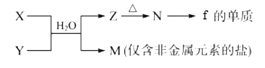
①寫出X溶液與Y溶液反應的離子方程式____________________________________;
②寫出工業上制備f的單質的化學方程式____________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com