
Fe(CO)5
常溫下呈液態,熔點為-20.5℃,沸點為103℃,易溶于非極性溶劑,據此可判斷Fe(CO)5晶體屬于________晶體.科目:高中化學 來源: 題型:
[選修—物質結構與性質](5分)
羰基鐵[Fe(CO)5]會使合成甲醇和合成氨等生產過程中的催化劑中素。請回答下列問題:
(1)Fe(CO)5中鐵的化合價為0,寫出鐵原子的基態電子排布式 。
(2)CO分子中C原子上有一對孤對電子,C、O原子都符合8電子穩定結構,CO分子中C原子的雜化類型為 雜化。與CO分子互為等電子體的分子和離子各寫出1種,分別為 和 (填化學式),CO分子的結構式可表示為 。
(3)Fe(CO)5常溫下呈液態,熔點為—20.5℃,沸點為103℃,易溶于非極性溶劑。據此可以判斷Fe(CO)5晶體為 。
(4)科學家通過X射線探明,FeO、MgO、CaO的晶體結構與NaCl的晶體結構相似(如23所示)①比較晶體熔點的高低MgO CaO(填“高于”或“低于”)
②若在FeO晶體中陰陽離子間最近距離為a cm,晶體密度為dg/cm3。則阿伏伽德羅常數NA表達式為 mol-1。
查看答案和解析>>
科目:高中化學 來源:2010年遼寧省大連市高三第二次模擬考試(理綜)化學部分 題型:填空題
[選修—物質結構與性質](5分)
羰基鐵[Fe(CO)5]會使合成甲醇和合成氨等生產過程中的催化劑中素。請回答下列問題:
(1)Fe(CO)5中鐵的化合價為0,寫出鐵原子的基態電子排布式 。
(2)CO分子中C原子上有一對孤對電子,C、O原子都符合8電子穩定結構,CO分子中C原子的雜化類型為 雜化。與CO分子互為等電子體的分子和離子各寫出1種,分別為 和 (填化學式),CO分子的結構式可表示為 。
(3)Fe(CO)5常溫下呈液態,熔點為—20.5℃,沸點為103℃,易溶于非極性溶劑。據此可以判斷Fe(CO)5晶體為 。
(4)科學家通過X射線探明,FeO、MgO、CaO的晶體結構與NaCl的晶體結構相似(如23所示)①比較晶體熔點的高低MgO CaO(填“高于”或“低于”)
②若在FeO晶體中陰陽離子間最近距離為a cm,晶體密度為dg/cm3。則阿伏伽德羅常數NA表達式為 mol-1。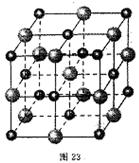
查看答案和解析>>
科目:高中化學 來源:2014屆江蘇泰州二中高二第一次(10月)限時作業化學試卷(解析版) 題型:填空題
(14分)隨著石油資源的日趨緊張,天然氣資源的開發利用受到越來越多的關注。以天然氣(主要成分CH4)為原料經合成氣(主要成分CO、H2)制化學品,是目前天然氣轉化利用的主要技術路線。而采用渣油、煤、焦炭為原料制合成氣,常因含羰基鐵[Fe(CO)5]等而導致以合成氣為原料合成甲醇和合成氨等生產過程中的催化劑產生中毒。
請問答下列問題:
(1)Fe(CO)5中鐵的化合價為0,寫出鐵原子的基態電子排布式
(2)原子數目和電子總數(或價電子總數)相同的微粒互為等電子體,等電子體具有相似的結構特征。與CO分子互為等電子體的分子和離子分別為 和 (填化學式),CO分子的結構式可表示成 。
(3)Fe(CO)5常溫下呈液態,熔點為-20.5℃,沸點為103℃,易溶于非極性溶劑。據此可判斷Fe(CO)5晶體為 晶體。
(4)在CH4、CO、CH3OH中,碳原子采取sp3雜化的分子有 ,CH3OH的熔、沸點比CH4的熔、沸點比高,其主要原因是 。
查看答案和解析>>
科目:高中化學 來源:2010年江蘇省高一第二學期期中考試化學(實驗班)試題 題型:填空題
(12分)
A.原子數相同、電子總數相同的分子,互稱為等電子體。
Ⅰ.已知A、B、C、D和E五種分子所含原子的數目依次為1、2、3、6和6,且都含有18個電子,又知B、C和D是由兩種元素的原子組成,且D分子中兩種原子個數比為1 :2。
請回答:
(1)組成A分子的原子的元素符號是 ;已知E是有毒的有機物,E的熔、沸點比CH4的熔、沸點高,其主要原因是____________________________________。
(2)C的立體結構呈 ____ 形,該分子屬于 分子(填“極性”或“非極性”);
(3)火箭中可充入四氧化二氮和D作為燃料反應生成氮氣和水,該反應的化學方程式為_______ __________________ 。(不需要寫反應條件)
Ⅱ.CO與N2互為等電子體。
(4)CO的總鍵能大于N2的總鍵能,但CO比N2容易參加化學反應。
根據下表數據,說明CO比N2活潑的原因是____________________________________。
|
|
|
A-B |
A=B |
A≡B |
|
CO |
鍵能(kJ/mol) |
357.7 |
798.9 |
1071.9 |
|
鍵能差值kJ/mol) |
441.2 273 |
|||
|
N2 |
鍵能(kJ/mol) |
154.8 |
418.4 |
941.7 |
|
鍵能差值kJ/mol) |
263.6 523.3 |
(5)它們的分子中都包含___________個σ鍵,______________個π鍵。
(6)Fe、Co、Ni等金屬能與CO反應的原因與這些金屬原子的電子層結構有關。
Ni原子的價電子排布式為 _____ 。Fe(CO)5常溫下呈液態,熔點為
-20.5℃,沸點為103℃,易溶于非極性溶劑,據此可判斷Fe(CO)5晶體屬于 ____(填晶體類型);Fe(CO)5是配合物,配體是__________ 。
B.茶中含有多種有益于人體健康的成分,據測定茶葉中含有450種以上的有機成分與15種以上的元素。某化學研究小組欲探究茶葉中鈣元素的含量,設計了探究實驗方案如下:(已知茶葉中的鋁、鐵元素對鈣離子的測定有影響)
步驟1:稱取500g干燥的茶葉,置于通風櫥中,充分灼燒使茶葉灰化,再用研缽磨細后移入燒杯中,然后將200mL 1 mol·L-1鹽酸加入灰中攪拌、過濾、洗滌。
步驟2:向步驟1所得濾液中逐滴加入稀氫氧化鈉溶液,調節溶液的pH至6~7左右,使鋁、鐵元素以氫氧化物的形式完全沉淀,再加熱煮沸30 min,加入7.95g無水碳酸鈉,充分攪拌,待沉淀完全后,過濾,洗滌,過濾后得到濾液和沉淀。
步驟3:將步驟2所得的濾液稀釋至500 mL,取其中的20.00 mL溶液以甲基橙作指示劑,用0.100mol·L-1的HCl標準溶液滴定,終點時消耗鹽酸的體積為20.00mL,計算結果。
請回答下列問題:
步驟 1中,使茶葉灰化時需要用到三角架、泥三角、酒精噴燈、 ___ 、 ____ 等儀器。
步驟2中,改用試劑 _______ (寫試劑名稱)來調節pH將更為方便;判斷沉淀已經洗凈的方法是 。
步驟3中,滴定過程中,眼睛應注視 ____________________,被滴定的20 mL濾液中含CO32-的物質的量為 __ mol,試計算原500g茶葉中鈣離子的質量分數為 _______ ,計算過程如下:
查看答案和解析>>
科目:高中化學 來源:2012屆江蘇省如皋市五校高二下學期期中調研化學試卷 題型:填空題
(12分)元素周期表中第四周期元素由于受3d電子的影響,性質的遞變規律與短周期元素略有不同。
⑴第四周期過渡元素的明顯特征是形成多種多樣的配合物。
①CO可以和很多過渡金屬形成配合物,如羰基鐵[Fe(CO)5]、羰基鎳[Ni(CO)4]。CO分子中C原子上有一對孤對電子,C、O原子都符合8電子穩定結構,CO的結構式為 ,與CO互為等電子體的離子為 (填化學式)。
②金屬鎳粉在CO氣流中輕微加熱,生成液態Ni(CO)4分子。423K時,Ni(CO)4分解為Ni和CO,從而制得高純度的Ni粉。試推測Ni(CO)4易溶于下列 。
a.水 b.四氯化碳 c.苯 d.硫酸鎳溶液
⑵第四周期元素的第一電離能隨原子序數的增大,總趨勢是逐漸增大的。鎵的基態原子的電子排布式是 ,Ga的第一電離能卻明顯低于Zn,原因是 。
⑶用價層電子對互斥理論預測H2Se和BBr3的立體結構,兩個結論都正確的是 。
a.直線形;三角錐形 b.V形;三角錐形
c.直線形;平面三角形 d.V形;平面三角形
⑷Fe、Co、Ni、Cu等金屬能形成配合物與這些金屬原子的電子層結構有關。
①Fe(CO)5常溫下呈液態,熔點為-20.5℃,沸點為103℃,易溶于非極性溶劑,據此可判斷Fe(CO)5晶體屬于 (填晶體類型)。
②CuSO4·5H2O(膽礬)中含有水合銅離子因而呈藍色,寫出膽礬晶體中水合銅離子的結構簡式(必須將配位鍵表示出來) 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com