
分別用一種試劑鑒別下列物質:
(1)(NH4)2SO4、NaCl與CH3COONa的溶液;
(2)Al2(SO4)3、MgSO4、FeSO4、Fe2(SO4)3、CuSO4與Na2SO4的溶液;
(3)Na2SiO3、Na2S、Na2CO3、Na2S2O3、NaCl的溶液;
(4)Na2SO4、NH4Cl、NaCl、(NH4)2SO4的溶液;
(5)Al2(SO4)3、H2SO4、Ba(OH)2、CaCl2的溶液;
(6)HCOOH、CH3COOH、C2H5OH、葡萄糖的溶液。
解題思路:只允許用一種試劑鑒別的題目,由于限制了試劑的種類,因而也就增加了題目的難度。要熟練解答這類習題,不但要熟練地掌握各類物質的性質和它們與某物質相互反應的規律及實驗現象,而且還必須有科學的解題思路。 常見的解題思路有以下幾種: ①若幾種溶液的酸堿性不同時,可選適當的指示劑或pH試紙鑒別。如(1)題因NaCl不水解,溶液呈中性;而(NH4)2SO4和CH3COONa都能水解分別使溶液呈酸性和堿性。所以用石蕊試液或pH試紙就可鑒別開來。 ②若幾種溶液含有不同的陽離子,可考慮用強堿溶液與它們分別反應,根據生成物的顏色、穩定性,及在過量堿液中的溶解情況而加以鑒別。如(2)題可用NaOH溶液鑒別。根據生成藍色沉淀鑒出 CuSO4;紅褐色沉淀鑒出Fe2(SO4)3;白色沉淀且立即變灰綠色,最終變紅褐色鑒出FeSO4;有白色沉淀且沉淀能溶于NaOH溶液鑒出Al2(SO4)3;白色沉淀不溶于NaOH溶液鑒出MgCl2;無現象的為Na2SO4。 ③若幾種溶液中含有不同的陰離子,可考慮使用強酸,根據生成物的狀態、顏色、氣味等差別加以鑒別。如(3)題可用稀硫酸或稀鹽酸鑒別。6種溶液分別與稀鹽酸反應,產生白色沉淀的為Na2SiO3;有臭雞蛋氣味的為Na2S;有無色無味氣體產生的為Na2CO3;有無色刺激性氣味氣體產生的為Na2SO3;使溶液變渾濁且產生無色刺激性氣味氣體的為 Na2S2O3;無現象的為NaCl。 ④若幾種物質間有的含有相同的陽離子,有的含有相同的陰離子,可考慮用既與相同的陽離子反應,又與相同的陰離子反應的試劑來鑒別。如(4)題可用Ba(OH)2溶液鑒別,實驗在加熱的情況下進行,只有白色沉淀產生的為Na2SO4;只有氣體產生的為 NH4Cl;既有白色沉淀又有氣體產生的為(NH4)2SO4;無現象的為NaCl。 ⑤若被鑒別物質中有能強烈水解的鹽,可考慮用與之能發生雙水解反應且與該組中其他物質發生不同反應的鹽溶液鑒別。如(5)題可用(NH4)2CO3溶液鑒別。分別反應時,若既有白色沉淀,又有無色無味氣體產生的是Al2(SO4)3;只有無色無味氣體產生的是H2SO4;既有白色沉淀,又有刺激性氣味氣體生成的是Ba(OH)2;只有白色沉淀的是CaCl2。此外,也可選用NaHCO3溶液鑒別。 ⑥鑒別有機物時,若被鑒別物質中含有醛基、羧基,應先考慮用新制得的Cu(OH)2懸濁液鑒別。被鑒別物質中含有酚的,可考慮用Fe3+利用顯色反應鑒別。如(6)中可用新制得的Cu(OH)2懸濁液鑒別。分別反應時懸濁液變為藍色溶液的是甲酸和乙酸;變為深藍色溶液,加熱煮沸時又產生紅色沉淀的是葡萄糖;無此現象的是乙醇。 參考答案:(1)石蕊試液等 (2)NaOH溶液 (3)稀鹽酸等 (4)Ba(OH)2溶液 (5)(NH4)2CO3溶液 (6)新制堿性Cu(OH)2懸濁液
|


 海淀黃岡名師導航系列答案
海淀黃岡名師導航系列答案 普通高中同步練習冊系列答案
普通高中同步練習冊系列答案 優翼小幫手同步口算系列答案
優翼小幫手同步口算系列答案科目:高中化學 來源: 題型:閱讀理解
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 A、B、C、D分別是HNO3、Ba(NO3)2、NH4Cl、NaOH四種溶液中的一種.現利用另一種常見溶液X,用下圖所示的方法,可將它們一一確定.請回答以下問題:
A、B、C、D分別是HNO3、Ba(NO3)2、NH4Cl、NaOH四種溶液中的一種.現利用另一種常見溶液X,用下圖所示的方法,可將它們一一確定.請回答以下問題:

| 電解質 | HF | HCOOH | CH3COOH | HCN | NH3?H2O |
| 電離度 | 8.00% | 7.16% | 1.32% | 0.01% | 1.33% |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
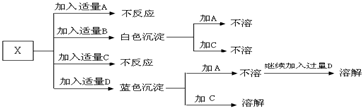 A、B、C、D分別是HNO3、Ba(NO3)2、NH4Cl、NaOH四種溶液中的一種.現利用另一種常見溶液X,用下圖所示的方法,可將它們一一確定.請回答以下問題:
A、B、C、D分別是HNO3、Ba(NO3)2、NH4Cl、NaOH四種溶液中的一種.現利用另一種常見溶液X,用下圖所示的方法,可將它們一一確定.請回答以下問題:| 電解質 | HF | HCOOH | CH3COOH | HCN | NH3?H2O |
| 電離度 | 8.00% | 7.16% | 1.32% | 0.01% | 1.33% |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com