
 ,B最外層電子數是2,C的氣態氫化物的水溶液呈堿性,據此填空:
,B最外層電子數是2,C的氣態氫化物的水溶液呈堿性,據此填空:分析 根據A的原子結構示意圖可知,x=2,故A的質子數為14,則A為Si元素;
C的氣態氫化物的水溶液呈堿性,則C為N元素;
原子序數D>A>B>C,且C、D同主族,則D為P元素;
B最外層電子數是2,原子序數D>A>B>C,且A、B同周期,則B為Mg元素,
根據元素所在周期表中的位置結合元素周期律的遞變規律解答該題.
解答 解:根據A的原子結構示意圖可知,x=2,故A的質子數為14,則A為Si元素;
C的氣態氫化物的水溶液呈堿性,則C為N元素;
原子序數D>A>B>C,且C、D同主族,則D為P元素;
B最外層電子數是2,原子序數D>A>B>C,且A、B同周期,則B為Mg元素,
(1)由上分析知A為硅元素,由于Si原子半徑大于C原子半徑,Si-H鍵能小于C-H鍵能,其氣態氫化物的穩定性比CH4弱,
故答案為:硅;弱;
(2)元素非金屬性越強,其最高價氧化物的水化物的酸性越強,故N、P的最高價氧化物的水化物的酸性大小為HNO3>H3PO4,
故答案為:HNO3;H3PO4;
(3)同主族金屬元素自上而下活潑型逐漸增強,Mg的活潑性比鈣的弱,
故答案為:弱;
(4)N的氣態氫化物與其最高價氧化物對應的水化物反應方程式為NH3+HNO3=NH4NO3,
故答案為:NH3+HNO3=NH4NO3.
點評 本題考查原子結構和元素周期律的關系,題目難度不大,注意根據元素的原子結構特點推斷元素的種類,掌握原子核外電子排布規律.


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 錐形瓶洗凈后還留有蒸餾水 | |
| B. | 取堿液的滴定管開始有氣泡,放出液體后氣泡消失 | |
| C. | 溶液顏色較淺時滴入酸液過快,停止滴定后反加一滴NaOH溶液無變化 | |
| D. | 用堿式滴定管取一定體積的NaOH溶液時,量取前仰視讀數,量取后俯視讀數 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷和氯氣混合后光照發生反應 | B. | 乙炔和氯氣的加成反應 | ||
| C. | 甲苯與等物質的量的Br2發生反應 | D. | 乙烯與水的加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 有機物CH2Cl-CH2Cl用系統命名法命名為:二氯乙烷 | |
| B. | 1mol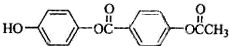 與足量的NaOH溶液充分反應,消耗NaOH的物質的量為3mol 與足量的NaOH溶液充分反應,消耗NaOH的物質的量為3mol | |
| C. | 標準狀況下,22.4L己烷所含分子數為NA | |
| D. | 乙醇與乙酸發生酯化反應時,乙醇分子中的碳氧鍵沒斷裂 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2SiO3的酸性比H2CO3的強 | |
| B. | Mg(OH)2的堿性比Be(OH)2的強 | |
| C. | HF、HCl、HBr、HI的熱穩定性依次增強 | |
| D. | 若M+和R2-的核外電子層結構相同,則原子序數:R>M |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
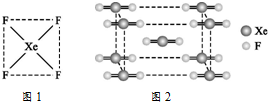 自從英國化學家巴特列(N.Bartlett)首次合成了第一種稀有氣體的化合物XePtF6以來,人們又相繼發現了氙的一系列化合物,如XeF2、XeF4等.巴特列為開拓稀有氣體化學作出了歷史性貢獻.
自從英國化學家巴特列(N.Bartlett)首次合成了第一種稀有氣體的化合物XePtF6以來,人們又相繼發現了氙的一系列化合物,如XeF2、XeF4等.巴特列為開拓稀有氣體化學作出了歷史性貢獻.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
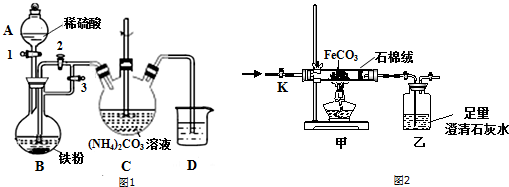
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只用試管和膠頭滴管就可區分純堿溶液和稀鹽酸 | |
| B. | Fe(OH)3是難溶于水的堿,但能通過化合反應生成 | |
| C. | 在FeCl3溶液中加入足量Cu充分反應后,溶液中的溶質只有CuCl2 | |
| D. | 有Al2O3制取Al(OH)3的途徑如下圖,則X可能是NaOH,也可能是HCl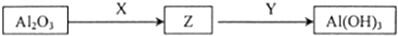 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com