
【題目】![]() 時,用濃度為
時,用濃度為![]() 的NaOH溶液滴定
的NaOH溶液滴定![]() 相同濃度的HX溶液,滴定曲線如圖所示。下列說法正確的是
相同濃度的HX溶液,滴定曲線如圖所示。下列說法正確的是![]()
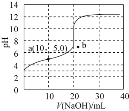
A.達到滴定終點時,溶液的![]()
B.根據圖象可估算出![]() 的值約為
的值約為![]()
C.a點所得溶液中:![]()
D.若用相同濃度的氨水替代NaOH溶液,滴定終點移向b點
 贏在課堂名師課時計劃系列答案
贏在課堂名師課時計劃系列答案科目:高中化學 來源: 題型:
【題目】請結合下列有機物回答相關問題,
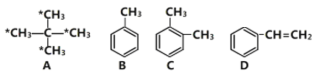
(1)應用系統命名法對有機物A進行命名:___________,標注“*”的碳原子連接起來構成的圖形為________(填“菱形”、“正方形”或“正四面體形”)。E是A的同系物,且比A少一個碳原子,則E的一氯代物有______種。
(2)相同質量的上述四種有機物完全燃燒時耗氧量最小的是_____________(填名稱)。
(3)有機物B能實現如下轉化:
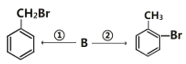
各步轉化的反應方程式為①___________________________;②___________________________。
(4)D在一定條件下生成高分子化合物的反應化學方程式為________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 時,向
時,向![]() 中不斷滴入
中不斷滴入![]() ,混合溶液pH變化如圖所示。此過程溶液下列說法不正確的是
,混合溶液pH變化如圖所示。此過程溶液下列說法不正確的是![]() 已知:
已知:![]() 時一元酸
時一元酸![]() 電離平衡常數
電離平衡常數![]()
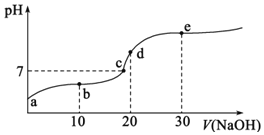
A.a點溶液的pH大于3
B.b點溶液中離子:![]()
C.c點表示酸![]() 和
和![]() 溶液恰好完全反應
溶液恰好完全反應
D.d點溶液加水稀釋后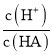 的值會增大
的值會增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關系式中,正確的是
A. 等濃度等體積的CH3COOH和CH3COONa溶液混合:c(CH3COO- )+c(OH-)=c(H+)+c(CH3COOH)
B. 常溫下,0.1 mol·L-1HA溶液與0.1 mol·L NaOH溶液等體積完全反應時,溶液中一定存在:c(Na+)=c(A-)>c(OH )=c(H+)
C. 常溫下,0.1 mol·L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S)
D. 常溫下,將0.1 mol·L-1CH3COOH溶液加水稀釋,當溶液的pH從3.0升到5.0時,溶液中c(CHCOO-)/c(CHCOOH)的值增大到原來的100倍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(題文)一定溫度下,在容積固定的密閉容器中進行的可逆反應:2NO2![]() 2NO+O2,達到平衡的標志是
2NO+O2,達到平衡的標志是
①相同時間內,氧氣的生成速率為n mol·L-1·s-1,NO2的生成速率為2n mol·L-1·s-1
②單位時間內生成n mol O2的同時生成2n mol的NO
③混合氣體的顏色不再變化 ④混合氣體的密度保持不變
⑤混合氣體的平均相對分子質量不再改變 ⑥壓強不隨時間變化而變化
A. ①③⑤⑥ B. ②③⑤
C. ①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氟酸是一種弱酸,可用來刻蝕玻璃。已知25℃時
HF(aq)+OH—(aq)=F—(aq)+H2O(l)△H=—67.7 kJ·mol—1
②H+(aq)+OH—(aq)=H2O(l)△H=—57.3 kJ·mol—1
在20mL0.1mol·L—1氫氟酸中加入VmL0.1mol·L—1NaOH溶液,下列有關說法正確的是
A. 氫氟酸的電離方程式及熱效應可表示為HF(aq)=H+(aq) +F(aq) △H=+10.4kJ·mol—1
B. 當V=20時,溶液中:c(OH—)=c(HF) +c(H+)
C. 當V=20時,溶液中:c(F—)<c(Na+)=0.1mol·L—1
D. 當V>0時,溶液中一定存在:c(Na+)>c(F—)>c(OH—)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外小組分別用如圖所示裝置對原電池和電解原理進行實驗探究。
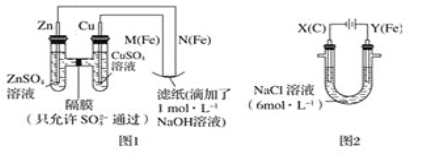
請回答:
Ⅰ.用圖1所示裝置進行第一組實驗。
(1)在保證電極反應不變的情況下,不能替代Cu作電極的是___(填字母序號)。
A.鋁 B.石墨 C.銀 D.鉑
(2)N極發生反應的電極反應式為___。
(3)實驗過程中,SO42-___(填“從左向右”,“從右向左”或“不”)移動;濾紙上能觀察到的現象有:___。
Ⅱ.用圖2所示裝置進行第二組實驗。實驗過程中,觀察到與第一組實驗不同的現象:兩極均有氣體產生,Y極區溶液逐漸變成紫紅色;停止實驗,鐵電極明顯變細,電解液仍然澄清。查閱資料得知,高鐵酸根離子(FeO42-)在溶液中呈紫紅色。
(4)電解過程中,X極區溶液的pH___(填“增大”“減小”或“不變”)。
(5)電解過程中,Y極發生的電極反應之一為Fe﹣6e-+8OH-=FeO42-+4H2O,若在X極收集到784mL氣體,在Y極收集到112mL氣體(均已折算為標準狀況時氣體體積),則Y電極(鐵電極)質量減少___g。
(6)在堿性鋅電池中,用高鐵酸鉀作為正極材料,電池反應為2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,該電池正極發生的反應的電極反應式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知X、Y、Z、W四種元素是元素周期表中連續三個不同短周期的元素,且原子序數依次增大。X、W同主族,Y、Z為同周期的相鄰元素。W原子的質子數等于Y、Z原子最外層電子數之和。Y的氫化物分子中有3個共價鍵。Z原子最外層電子數是次外層電子數的3倍。試推斷:
(1)X、Y、Z、W四種元素的符號: X________、Y__________、Z____________、W、________
(2)由以上元素中的兩種元素組成的能溶于水且水溶液顯堿性的化合物的電子式分別為__________________,______________________。
(3)由X、Y、Z所形成的離子化合物是________________,它與W的最高氧化物的水化物的濃溶液加熱時反應的離子方程式是________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由已知電離常數判斷,下列關于SO2與Na2CO3(aq)反應的離子方程式的書寫中,不合理的是( )
酸 | 電離常數 |
碳酸 | K1=4×10-7 K2=5.6×10-11 |
亞硫酸 | K1=1.54×10-2 K2=1.02×10-7 |
A.SO2+H2O+2CO32-=2HCO3-+SO32-
B.SO2+H2O+CO32-=H2O+CO2+SO32-
C.2SO2+2H2O+CO32-=H2O+CO2+2HSO3-
D.SO2+H2O+CO32-=HCO3-+HSO3-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com