
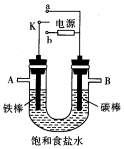
 根據如圖裝置進行電化學的相關實驗,回答下列問題.
根據如圖裝置進行電化學的相關實驗,回答下列問題.分析 (1)若把開關K與a連接,是原電池裝置,碳棒作正極,鐵棒發生氧化反應,電極反應式為Fe-2e-=Fe2+;
(2)開關K與b連接,裝置為電解池,鐵為陰極,發生還原反應,氫離子得到電子生成氫氣,電解飽和食鹽水生成氫氧化鈉、氫氣和氯氣,總反應式為2NaCl+2H2O$\frac{\underline{\;通電\;}}{\;}$2NaOH+H2↑+Cl2↑;
①石墨為陽極,發生氧化反應生成氯氣,能使濕潤的KI淀粉試紙變藍,鐵為陰極;
②氯氣與氫氧化鈉溶液反應生成氯化鈉、次氯酸鈉和水.
解答 解:(1)若把開關K與a連接,是原電池裝置,碳棒作正極,鐵棒發生氧化反應,電極反應式為Fe-2e-=Fe2+,故答案為:正;Fe-2e-=Fe2+;
(2)開關K與b連接,裝置為電解池,鐵為陰極,發生還原反應,氫離子得到電子生成氫氣,電解飽和食鹽水生成氫氧化鈉、氫氣和氯氣,總反應式為2NaCl+2H2O$\frac{\underline{\;通電\;}}{\;}$2NaOH+H2↑+Cl2↑,2H2O+2Cl- $\frac{\underline{\;通電\;}}{\;}$H2↑+Cl2↑+2OH-;
故答案為:2H2O+2Cl- $\frac{\underline{\;通電\;}}{\;}$H2↑+Cl2↑+2OH-;
①石墨為陽極,發生氧化反應生成氯氣,能使濕潤的KI淀粉試紙變藍,鐵為陰極,碳棒上發生的電極反應為2Cl--2e-=Cl2↑,故答案為:正;2Cl--2e-=Cl2↑;
②氯氣與氫氧化鈉溶液反應生成氯化鈉、次氯酸鈉和水,化學方程式:Cl2+2NaOH=NaCl+NaClO+H2O,故答案為:Cl2+2NaOH=NaCl+NaClO+H2O.
點評 本題綜合原電池和電解質知識,側重于學生的分析能力和電化學知識的綜合應用,注意解題時要注意分析電極反應及生成物,難度中等.


科目:高中化學 來源: 題型:多選題
| A. | N4和N2是氮元素的兩種不同單質 | |
| B. | ${\;}_{7}^{14}{N}_{4}$、${\;}_{7}^{15}{N}_{2}$互為同位素 | |
| C. | 相同質量的N4和N2所含原子個數比為1:2 | |
| D. | ${\;}_{7}^{14}{N}_{4}$的摩爾質量是56g/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
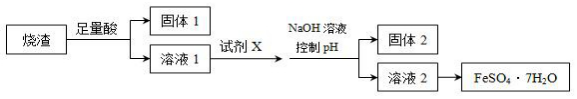
| A. | 溶解燒渣選用足量硫酸,試劑X選用鐵粉 | |
| B. | 固體1中一定含有SiO2,控制pH為使Al3+轉化為Al(OH)3,進入固體2 | |
| C. | 從溶液2得到FeSO4•7H2O產品的過程中,須控制條件防止其氧化 | |
| D. | 若改變方案,在溶液1中直接加NaOH至過量,得到的沉淀用硫酸溶解,其溶液經結晶分離也可得到FeSO4•7H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3COO-+H2O?CH3COOH+OH- | B. | NH4++H2O?NH4OH+H+ | ||
| C. | HCO3-+H2O?CO2↑+H2O | D. | NaCl+H2O?NaOH+HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2.8g鐵與0.05mol Cl2充分反應,轉移0.1NA電子 | |
| B. | 27g Al與足量NaOH溶液反應生成 33.6L H2 | |
| C. | 1mol由乙烯(C2H4)和乙烷(C2H6)組成的混合物中含有碳原子的數目為2NA | |
| D. | 0.1mol Na2O2與足量二氧化碳反應轉移0.1NA個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 11.7 g | B. | 5.85 g | C. | 8 g | D. | 15.5 g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
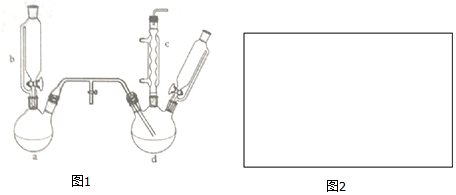
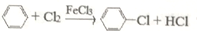 .
.| 項目 | 二氯苯 | 氯化尾氣 | 蒸氣 | 成品 | 不確定苯耗 | 合計 |
| 苯流失量(t/kg) | 11.7 | 5.4 | 20.8 | 2.0 | 49.3 | 89.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有② | B. | ②④ | C. | ③④ | D. | ①② |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com