
【題目】現有下列十種物質:①NaHCO3;②C2H5OH;③Cu;④H2O;⑤石灰乳;⑥CO;⑦Ba(OH)2;⑧鹽酸;⑨H2CO3;⑩濃硝酸。
(1)屬于電解質的是___(填寫序號),屬于非電解質的是___(填寫序號)。
(2)⑨在水溶液中的電離方程式為___。
(3)⑤與⑧反應的離子方程式為___。
(4)向⑦的溶液中滴加①的溶液至Ba2+恰好完全沉淀,離子方程式為___。
(5)③與⑩反應的離子方程式如下,請配平方程式(在中填入系數,在橫線上寫上缺少的物質),并用“單線橋”標出電子轉移的方向與數目。___
Cu+NO3-+ —Cu2++NO2↑+
【答案】①④⑦⑨ ②⑥ H2CO3![]() H++HCO3-、HCO3-
H++HCO3-、HCO3-![]() H++CO32- Ca(OH)2+2H+ ═Ca2++2H2O Ba2++HCO3-+OH-═BaCO3↓+H2O
H++CO32- Ca(OH)2+2H+ ═Ca2++2H2O Ba2++HCO3-+OH-═BaCO3↓+H2O 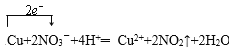
【解析】
①NaHCO3是鹽,屬于電解質;
②C2H5OH是有機物,屬于非電解質;
③Cu屬于金屬單質,既不是電解質也不是非電解質;
④H2O是非金屬氧化物,屬于電解質;
⑤石灰乳是氫氧化鈣懸濁液,為混合物,既不是電解質也不是非電解質;
⑥CO是非金屬氧化物,屬于非電解質;
⑦Ba(OH)2是堿,屬于電解質;
⑧鹽酸為混合物,既不是電解質也不是非電解質;
⑨H2CO3是酸,屬于電解質;
⑩濃硝酸為混合物,既不是電解質也不是非電解質。
(1)由分析可知,屬于電解質的是①④⑦⑨,屬于非電解質的是②⑥,故答案為:①④⑦⑨;②⑥;
(2)H2CO3是二元弱酸,在水溶液中分步電離,電離方程式為H2CO3![]() H++HCO3-、HCO3-
H++HCO3-、HCO3-![]() H++CO32-,故答案為:H2CO3
H++CO32-,故答案為:H2CO3![]() H++HCO3-、HCO3-
H++HCO3-、HCO3-![]() H++CO32-;
H++CO32-;
(3)石灰乳與鹽酸反應生成氯化鈣和水,石灰乳是氫氧化鈣懸濁液,不能拆寫,反應的離子方程式為Ca(OH)2+2H+ ═Ca2++2H2O,故答案為:Ca(OH)2+2H+ ═Ca2++2H2O;
(4)向氫氧化鋇溶液中滴加碳酸氫鈉的溶液至Ba2+恰好完全沉淀時,反應生成碳酸鋇沉淀、氫氧化鈉和水,反應的離子方程式為Ba2++HCO3-+OH-═BaCO3↓+H2O,故答案為:Ba2++HCO3-+OH-═BaCO3↓+H2O;
(5)銅與濃硝酸反應生成硝酸銅、二氧化氮和水,反應的化學方程式為Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O,反應中轉移2mol電子,電子轉移的方向與數目為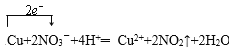 ,故答案為:
,故答案為: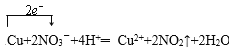 。
。


科目:高中化學 來源: 題型:
【題目】氮化鋁(AlN)是一種新型無機材料,廣泛應用于集成電路生產領域。某化學研究小組利用氮氣、氧化鋁和活性炭在高溫下制取氮化鋁。 請回答下列問題:
(1)請寫出制取氮化鋁的化學方程式________。
制得的AlN樣品僅含有Al2O3雜質,已知:AlN+NaOH+H2O=NaAlO2+NH3↑為測定AlN含量,設計如下三種實驗方案。(測定過程均忽略NH3在強堿溶液中的溶解)
(方案1)取一定量的樣品,用以下裝置測定樣品中AlN的純度(夾持裝置已略去)。
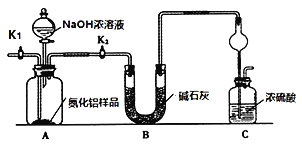
實驗步驟:組裝好實驗裝置,檢查裝置氣密性并加入實驗藥品,關閉K1,打開K2 ,打開分液漏斗活塞,加入NaOH濃溶液,至不再產生氣體。打開K1,通入氮氣一段時間,測定C裝置反應前后的質量變化。
(2)圖中C裝置中球形干燥管的作用是________。
(3)通入氮氣的目的是_______。
(4)圖中裝置會導致測定結果_______(填“偏高”“偏低”或“無影響”)。
(方案2)用如圖裝置測定mg樣品中AlN的純度(部分夾持裝置已略去)。
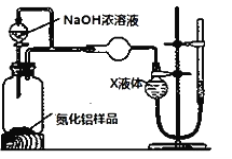
(5)為測定生成氣體的體積,量氣裝置中的X液體可以是___(填字母)
A.CCl4 B.H2O C.NH4Cl溶液 D.苯
(6)若mg樣品完全反應,測得生成氣體的體積為VmL(已轉換為標準狀況),則AlN的質量分數是______。若其他操作均正確,但反應結束后讀數時,右側量氣管中液面高于左側球型管中液面,則最后測得AlN的質量分數會_____(填“偏高”“偏低”或“無影響”)。
(方案3)按以下步驟測定樣品中A1N的純度:(過濾時使用無灰濾紙過濾)
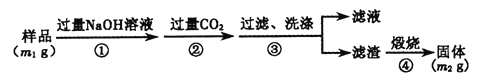
(7)步驟②生成沉淀的離子方程式為_______。
(8)樣品中A1N的質量分數為_______(用含m1、m2的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+ O2 (g)![]() 2SO3(g) ΔH<0
2SO3(g) ΔH<0
(1)降低溫度,該反應K值______,二氧化硫轉化率____,化學反應速度____ ,(以上均填增大、減小或不變)
(2)600℃時,在一密閉容器中,將二氧化硫和氧氣混合,反應過程中SO2、O2、SO3物質的量變化如圖,反應處于平衡狀態的時間是_____。
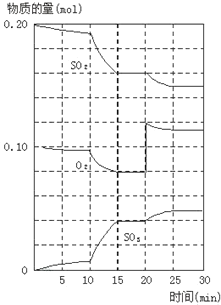
(3)據圖判斷,反應進行至20min時,曲線發生變化的原因_____(用文字表達)
(4)10min到15min的曲線變化的原因可能是____(填寫編號)。
a.加了催化劑 b.縮小容器體積 c.降低溫度 d.增加SO3的物質的量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】學習小組研究鈉的燃燒反應產物,取金屬鈉(表面已被氧化),吸干煤油,置于坩堝內,上方倒扣盛滿O2集氣瓶,加熱一段時間,充分反應后觀察到產物為白色固體和淡黃色固體的混合物,測得反應前后各物質的質量如下表:
質量/g | ||
反應前 | 坩堝 | 100 |
盛有金屬鈉的坩堝 | 105.4 | |
反應后 | 盛有固體產物的坩堝 | 107.4 |
請回答下列問題:
(1)根據實驗現象,推測固體產物成分為___________________(填化學式)
(2)將產物全部溶于水,觀察到有氣泡生成,寫出該反應的化學方程式為________。
(3)測得上述溶液中n(Na+)=0.2mol,通過計算證實加熱過程中存在表面的Na2O轉化為Na2O2。___________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA為阿伏加德羅常數的值,下列說法正確的是( )
A.16gO2和O3的混合氣體中含有的分子數為0.5NA
B.0.3molAgNO3受熱完全分解(2AgNO3=2Ag+2NO2↑+O2↑),用排水法收集到氣體的分子數為 0.25NA
C.0.5NA個氯氣分子所占體積約是11.2L
D.2.3g金屬鈉在裝有氧氣的集氣瓶中完全燃燒,轉移的電子數為0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳酸鑭[La2(CO3)3]可用于治療終末期腎病患者的高磷酸鹽血癥。制備反應2LaCl3+6NH4HCO3=La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O;某化學興趣小組利用下列裝置模擬制備碳酸鑭。
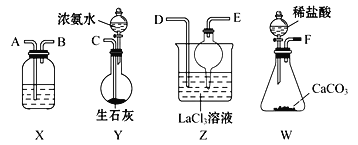
(1)盛放稀鹽酸的儀器名稱為________________。
(2)制備碳酸鑭實驗流程中導管從左向右的連接順序為F→____→____→____→____→______。
(3)W中發生反應的離子方程式為_______Y中發生反應的化學反應方程式為__________
(4)X中盛放的試劑是_________,干燥管的作用為_________________。
(5)Z中通入氣體的方式________
A.先通入足量NH3,后通入過量的CO2
B.先通入足量CO2,后通入過量的NH3
C.NH3和CO2同時通入
(6)該化學興趣小組為探究La2(CO3)3和La(HCO3)3的穩定性強弱,設計了如下的實驗裝置,則甲試管中盛放的物質為________________,實驗過程中,發現乙試管中固體質量與灼燒時間的關系曲線如圖所示,則關于兩種物質穩定性實驗結論為_____。
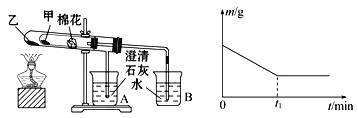
A.穩定性La2(CO3)3>La(HCO3)3
B.穩定性La2(CO3)3<La(HCO3)3
C.無法判斷
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年是“國際化學元素周期表年”。1869年門捷列夫把當時己知的元素根據物理、化學性質進行排列,準確預留了甲、乙兩種未知元素的位置,并預測了二者的相對原子質量,部分原始記錄如下。

下列說法不正確的是
A.元素甲比Al的最高價氧化物的水化物的堿性弱B.原子半徑比較:甲>乙>Si
C.元素乙位于現行元素周期表第四周期第ⅣA族D.推測乙可以用作半導體材料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】檳榔堿為油狀液體,有擬膽堿作用,在醫療上用于治療青光眼,能使絳蟲癱瘓。某學生設計了以X為原料的合成路線如下:
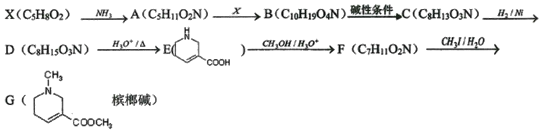
己知:①X能使溴水褪色、能水解,水解產物之一為乙醇。
②
③![]()
(1)檳榔堿中非氮官能團的名稱__________,C的結構簡式____________。
(2)下列說法正確的是_____________。
A.化合物A能形成內鹽
B.化合物C的1H-NMR譜表明含6組峰
C.化合物D有堿性
D.化合物E能溶于水
E.化合物F在一定條件下能發生加聚、氧化、取代等反應
(3)D→E反應的方程式____________。
(4)煙酸![]() 也可以合成檳榔堿。寫出煙酸的同分異構體,且符合下列條件的結構簡式________。
也可以合成檳榔堿。寫出煙酸的同分異構體,且符合下列條件的結構簡式________。
①1H-NMR譜表明分子中有3種氫原子
②只含有一個六元環,環上無氧原子,且只有1個取代基
(5)結合題給信息,請設計由乙醇和E![]() 為原料合成化合物M
為原料合成化合物M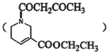 的路線,(用流程圖表示,試劑任選)__________________________。
的路線,(用流程圖表示,試劑任選)__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用Na2FeO4溶液氧化廢水中的還原性污染物M,為研究降解效果,設計如下對比實驗探究溫度、濃度、 pH、催化劑對降解速率和效果的影響,實驗測得M的濃度與時間關系如圖所示:
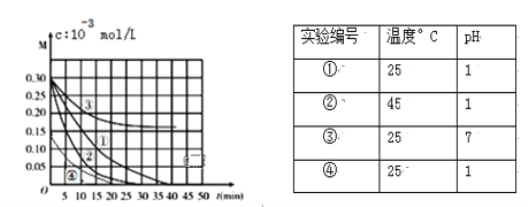
下列說法正確的是
A. 實驗①在15 min內M的降解速率為1.33×10-2mol/(L·min)
B. 若其他條件相同,實驗①②說明升高溫度,M降解速率增大
C. 若其他條件相同,實驗①③證明pH越高,越有利于M的降解
D. 實驗②④說明M的濃度越小,降解的速率越慢
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com