
| A. | 在原電池的負極和電解池的陰極上都發生失電子的氧化反應 | |
| B. | 用惰性電極電解Na2SO4溶液,陰陽兩極產物的物質的量之比為1:2 | |
| C. | 用惰性電極電解飽和NaCl溶液,若有0.1 mol電子轉移,則生成0.1 mol NaOH | |
| D. | 鍍層破損后,鍍鋅鐵板比鍍錫鐵板更易腐蝕 |
分析 A.得電子的發生還原反應,失電子的發生氧化反應;
B.用惰性電極電解Na2SO4溶液,陰極上析出氫氣,陽極上析出氧氣,根據轉移電子數相等確定產物的物質的量之比;
C.根據氫氧化鈉和轉移電子之間的關系式計算;
D.作原電池負極的金屬比作原電池正極的金屬易腐蝕.
解答 解:A.電解池陰極上得電子發生還原反應,故A錯誤;
B.用惰性電極電解Na2SO4溶液,陰極上析出氫氣,陽極上析出氧氣,氫離子得2mol電子生成1mol氫氣,4mol氫氧根離子失去4mol電子生成1mol氧氣,所以陰陽兩極產物的物質的量之比為2:1,故B錯誤;
C.設生成x氫氧化鈉,
2NaCl+2H2O$\frac{\underline{\;通電\;}}{\;}$2NaOH+H2↑+Cl2↑ 轉移電子
2mol 2mol
x 0.1mol
x=$\frac{2×0.1}{2}$mol=0.1mol,所以生成0.1mol氫氧化鈉,故C正確;
D.鍍層破損后,鍍錫鐵板中鐵作負極,鍍鋅鐵板中鐵作正極,所以鍍鋅鐵板比鍍錫鐵板更耐腐蝕,故D錯誤;
故選C.
點評 本題考查了原電池和電解池原理,難度不大,注意選項B中生成1mol氧氣需要轉移4mol電子.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
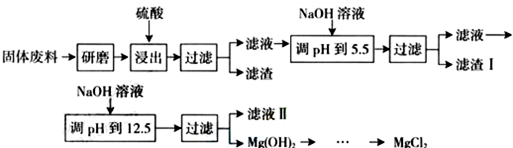
| 沉淀物 | Fe3+ | Al3+ | Mg2+ |
| pH | 3.2 | 5.2 | 12.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 盡可能使用稀溶液 | B. | 選擇合適的催化劑 | ||
| C. | 碾細固體反應物 | D. | 提高反應體系的溫度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CaCl2$\stackrel{CO_{2}}{→}$CaCO3$\stackrel{高溫}{→}$CaO | B. | Fe$\stackrel{少量Cl_{2}}{→}$FeCl2$\stackrel{NaOH溶液}{→}$Fe(OH)2 | ||
| C. | Al2O3$\stackrel{NaOH溶液}{→}$NaAlO2$\stackrel{CO_{2}}{→}$Al(OH)3 | D. | SiO2$\stackrel{水}{→}$H2SiO3$\stackrel{NaOH溶液}{→}$Na2SiO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 藥名 | 胃舒平 | 達喜 |
| 有效成分的化學式 | Al(OH)3 | Al2Mg6(OH)16CO3•4H2O |
| 相對分子質量 | 78 | 530 |
| 每片含有效成份的藥量 | 0.245g | 0.5g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
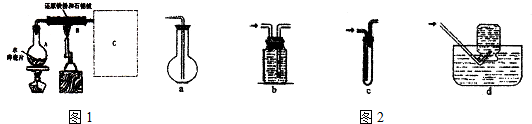
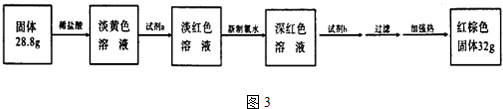
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com