
【題目】設NA為阿伏加德羅常數的值,下列敘述正確的是( )
A. 100 mL 0.1 mol·L-1 K2SO4溶液中,含有氧原子數為0.04NA
B. 1 mol Na與足量O2反應,生成Na2O和Na2O2的混合物,轉移的電子數為NA
C. 25 ℃時,1.0 L pH=13的Ba(OH)2溶液中,含有的OH-數目為0.2NA
D. 100 g 17%的氨水中,含有氨分子數為NA
 奪冠金卷全能練考系列答案
奪冠金卷全能練考系列答案科目:高中化學 來源: 題型:
【題目】(1)氨氣易溶于水生成氨水,氨水電離生成銨根離子,銨根離子中氮原子采取________雜化,NH4+中HNH鍵角比NH3中HNH鍵角大,原因是__________________。
(2)Cu3N形成的晶體結構如圖所示,N3-的配位數是________________。

(3)常溫常壓下,給水施加一個弱電場便可形成冰,稱之為“熱冰”,熱冰中微粒間存在的作用力有________,其大小順序是__________。
(4)NaF和NaCl屬于同一主族的鈉鹽,但NaF的莫氏硬度比NaCl大,原因是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了保護環境,充分利用資源,可將工業廢棄物轉變成重要的化工原料。
請回答下列問題:
(1)可用NaClO3氧化酸性FeCl2廢液得到FeCl3,FeCl3具有凈水作用,但腐蝕設備。
①寫出NaClO3氧化酸性FeCl2的離子方程式:__________________________。
②若酸性FeCl2廢液中:c(Fe2+)=2.0×10-2 mol∕L,c(Fe3+)=1.0×10-3 mol∕L,c(Cl-)=5.3×10-2 mol∕L,則該溶液的pH約為_________。
③FeCl3凈水的原理是:_________________(用離子方程式及適當文字回答);FeCl3溶液腐蝕鋼鐵設備,除H+作用外,另一主要原因是_________(用離子方程式表示)。
(2)可用廢鐵屑為原料,按下圖的工藝流程制備聚合硫酸鐵(PFS),PFS是一種新型的
絮凝劑,處理污水比FeCl3高效,且腐蝕性小。
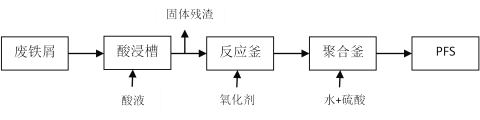
①酸浸時最合適的酸是______________。
②反應釜中加入的氧化劑,下列試劑中最合適的是____________(填標號)。
a.HNO3 b.KMnO4 c.Cl2 d.H2O2
檢驗其中Fe2+是否完全被氧化,應選擇____________________(填標號)。
a.K3[Fe(CN)6]溶液 b.Na2SO3溶液 c.KSCN溶液
③生成PFS的離子方程式為:xFe3++yH2O Fex(OH)y(3x-y)++yH+欲使平衡正向移動可采用的方法是____________(填標號)。
a.加入NaHCO3 b.降溫 c.加水稀釋 d.加入NH4Cl
(3)廢鐵屑在一定條件下,可制得FeS2(二硫化亞鐵)納米材料,該材料可用于制造高容量鋰電池,電池放電時的總反應為4Li+FeS2=Fe+2Li2S,維持電流強度為1A,a電池工作1小時,理論上消耗FeS2__________g。(已知1mol電子的電量為96500C)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在粗鹽提純的實驗中,蒸發時正確的操作是( )
A. 把渾濁的液體倒入蒸發皿內加熱
B. 蒸發皿中發現有大量固體析出時即停止加熱
C. 開始有固體析出后使用玻璃棒攪拌
D. 待水分完全蒸干后停止加熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[2017江蘇]某科研小組采用如下方案回收一種光盤金屬層中的少量Ag(金屬層中其他金屬含量過低,對實驗的影響可忽略)。

已知:①NaClO溶液在受熱或酸性條件下易分解,如:3NaClO![]() 2NaCl+NaClO3
2NaCl+NaClO3
②AgCl可溶于氨水:AgCl+2NH3·H2O ![]() Ag(NH3) 2++ Cl +2H2O
Ag(NH3) 2++ Cl +2H2O
③常溫時N2H4·H2O(水合肼)在堿性條件下能還原Ag(NH3)2+:
4Ag(NH3) 2++N2H4·H2O![]() 4Ag↓+N2↑+4
4Ag↓+N2↑+4![]() +4NH3↑+H2O
+4NH3↑+H2O
(1)“氧化”階段需在80℃條件下進行,適宜的加熱方式為__________________。
(2)NaClO溶液與Ag反應的產物為AgCl、NaOH和O2,該反應的化學方程式為________________。 HNO3也能氧化Ag,從反應產物的角度分析,以HNO3代替NaClO的缺點是_____________________。
(3)為提高Ag的回收率,需對“過濾Ⅱ”的濾渣進行洗滌,并_______________________。
(4)若省略“過濾Ⅰ”,直接向冷卻后的反應容器中滴加10%氨水,則需要增加氨水的用量,除因過量NaClO與NH3·H2O反應外(該條件下NaClO3與NH3·H2O不反應),還因為_________________。
(5)請設計從“過濾Ⅱ”后的濾液中獲取單質Ag的實驗方案:________________________(實驗中須使用的試劑有:2 mol·L1水合肼溶液,1 mol·L1H2SO4)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示為從固體混合物中分離X的兩種方案,請根據方案1和方案2指出下列說法中合理的是( )

A. 可以選用方案1分離碳酸氫鈉中含有的氯化銨
B. 方案1中的殘留物應該具有的性質是受熱易揮發
C. 方案2中加入的試劑一定能夠與除X外的物質發生化學反應
D. 方案2中加入NaOH溶液可以分離出SiO2和Fe2O3混合物中的Fe2O3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z三種短周期元素在周期表中的相對位置如圖所示,Y原子的最外層 電子數是次外層電子數的3倍,下列說法正確的是

A. 在三種元素形成的簡單氣態氫化物中,Y的氣態氫化物沸點最高
B. Z元素的氧化物對應的水化物一定是一種強酸
C. 三種元素原子半徑的大小順序為:X>Y>Z
D. Z的單質與Fe反應生成的化合物中,鐵元素顯+3價
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com