
【題目】某興趣小組的同學用下圖所示裝置研究有關電化學的問題(甲、乙、丙三池中的溶質足量),當閉合該裝置的電鍵K時,觀察到電流表的指針發生了偏轉。

請回答下列問題:
(1)甲池為_________(填“原電池”、“電解池”或“電鍍池”),A電極的電極反應式為______。
(2)丙池中F電極為____(填“正極”、“負極”、“陰極”或“陽極”),該池總反應的方程式為_____。
(3)當乙池中C極質量減輕4.32g時,甲池中B電極理論上消耗O2的體積為_____mL(標準狀況)。
(4)一段時間后,斷開電鍵K。下列物質能使乙池恢復到反應前濃度的是______(填字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu(OH)2CO3
(5)甲醇和乙醇都可以做燃料。已知乙醇液體完全燃燒生成CO2氣體和1mol液態水時放出熱量453.3kJ,請寫出乙醇燃燒的熱化學方程式:____________。
【答案】 原電池 CH3OH+8OH--6e-=CO32-+6H2O 陰極 2CuSO4+2H2O![]() 2H2SO4+2Cu+ O2↑ 224 A C2H5OH(l)+3O2(g)=2CO2(g)+3H2O △H=-1359.9kJ/mol
2H2SO4+2Cu+ O2↑ 224 A C2H5OH(l)+3O2(g)=2CO2(g)+3H2O △H=-1359.9kJ/mol
【解析】(1)甲池為燃料電池,是原電池;A電極的電極是燃料發生氧化反應,反應式為CH3OH+8OH--6e-═CO32-+6H2O,故答案為:原電池;CH3OH+8OH--6e-═CO32-+6H2O;
(2)丙池中F與電源的負極相連是陰極,惰性電極電解硫酸銅生成銅和氧氣,電極反應式為:2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑,故答案為:陰極;2CuSO4+2H2O
2H2SO4+2Cu+O2↑,故答案為:陰極;2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑;
2H2SO4+2Cu+O2↑;
(3)根據轉移電子數目相等,4Ag~~O2,
4×108g 22400mL
4.32g V
所以![]() =
=![]() ,解之得:V=224mL,故答案為:224;
,解之得:V=224mL,故答案為:224;
(4)甲池為燃料電池,A為負極,B為正極,則乙中C為陽極,D為陰極,陽極上Ag失電子生成銀離子,陰極上銅離子得電子生成Cu,溶液中減少了Cu元素的質量,所以要讓電解質復原,需要加入金屬銅,故選A;
(5)乙醇燃燒生成液態水的化學方程式為C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l),生成1mol液態水時放出熱量453.3kJ,則生成3mol液態水時放出熱量為453.3kJ×3=1359.9kJ,則乙醇燃燒的熱化學方程式為C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1359.9kJ/mol,故答案為:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1359.9kJ/mol。


科目:高中化學 來源: 題型:
【題目】W、X、Y、Z是四種常見的短周期元素,其原子半徑隨原子序數變化如右圖所示。已知W的一種核素的質量數為18,中子數為10;X和Ne原子的核外電子數相差1;Y的單質是一種常見的半導體材料;Z的電負性在同周期主族元素中最大。

(1)X位于元素周期表中第________周期第________族;W的基態原子核外有_____個未成對電子。
(2)Z的氣態氫化物和溴化氫相比,較穩定的是______(寫化學式)。
(3)Y與Z形成的化合物和足量水反應,生成一種弱酸和一種強酸,該反應的化學方程式是__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室要用CuSO4·5H2O晶體配制480mL 0.1mol/L CuSO4溶液,回答下列問題:
(1)應該用托盤天平稱取CuSO4·5H2O________g。
(2)所需儀器除了燒杯、玻璃棒、膠頭滴管,量筒、托盤天平外,還缺少_____________、_________。
(3)實驗中兩次用到玻璃棒,起作用分別是________________、______________。
(4)配制溶液時有以下幾個操作:
①溶解 ②搖勻 ③洗滌 ④冷卻 ⑤稱量 ⑥轉移溶液 ⑦定容
正確的操作順序是__________________(填序號)。
(5)若實驗中有下列情況,對配制溶液的濃度有何影響?(填“偏高”、“偏低”或“無影響”)
A.膽礬失去了部分結晶水_________________________;
B.定容時加水超過刻度線___________________________;
C.最終定容時仰視觀察液面_________________________。
(6)如圖是溫度計、量筒的一部分,下述讀數(虛線對應刻度)及說法正確的是________。

A.①是量筒,讀數為2.5 mL B.②是量筒,讀數為2.5 mL
C.①是溫度計,讀數為3.5℃ D.②是溫度計,讀數為2.5 ℃
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是某化學研究小組探究外界條件對化學反應速率和化學平衡影響的圖像,其中圖像和實驗結論表達均正確的是( )


A. ①是其他條件一定時,反應速率隨溫度變化的圖像,正反應ΔH<0
B. ②是在平衡體系的溶液中溶入少量KCl晶體后化學反應速率隨時間變化的圖像
C. ③是在有無催化劑存在下建立的平衡過程圖像,a是使用催化劑時的曲線
D. ④是一定條件下,向含有一定量A的容器中逐漸加入B時的圖像,壓強p1>p2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某綠色農藥結構簡式為圖1,回答下列問題。
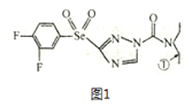
(1)基態硒原子的核外電子排布式為______________,該農藥組成元素中,第一電離能較大的前三種元素是______________(按由大到小顧序排列)。
(2)分子中編號為①的碳原子和與其成鍵的另外幾個原子構成的空間結構為____________;CSe2首次是由H2Se 和CCl4; 反應制取的,試比較上述三種分子的鍵角_____________(按出大到小順序排列)。
(3)H2SeO3 分子的中心原子雜化類型是____________,試比較H2SeO3、H2SeO4 和H2SO4三種酸的酸性強弱(按由強到弱順序排列)_______________。
(4)石墨是碳元素的一種同素異形體,石墨晶體可看作ABABA...堆積方式,晶胞結構和部分晶胞參數如圖2 所示; 堿金屬離子可填充在石墨層問形成石墨夾層化合物,同時堆積方式從ABABAB...變為AAAA...。
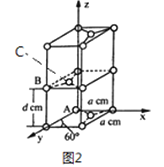
①原子坐標參數描述的是晶胞內原子間的相對位置。石墨晶胞中碳原子A、B 的坐標參數分別為: A(0,0,0)、B(0,1,1/2)。則C 原子的坐標參數為_____________,。
②晶胞參數用以描述品胞的大小和形狀。已知石墨晶胞底邊長為a pm,層間距為d pm,阿伏加德羅常數的值為NA,則石墨的密度為_____________g/cm3 (寫出表達式即可)。
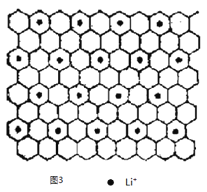
③圖3為石墨夾層化合物W 的投影圖,試寫出W 的化學式_____________,微粒之間存在的化學鍵有_____________,
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在反應mA+nB===pC+qD中,若v(A)=4 mol·L-1·min-1, 而v(B)=1 mol·L-1·min-1,A表示的反應速率比B表示的反應速率快,而m、n符合的關系
A. m∶n=4∶1 B. m∶n<4∶1 C. m∶n>4∶1 D. 無法判斷
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向Ba(OH)2溶液中逐滴加入稀硫酸,請完成下列問題:
(1)寫出反應的離子方程式:__________________。
(2)下列三種情況下,離子方程式與(1)相同的是________(填序號)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至過量
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液中顯中性
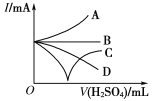
(3)若緩緩加入稀硫酸直至過量,整個過程中混合溶液的導電能力(用電流強度I表示)可近似地用下圖中的_______曲線表示(填序號)。
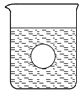
(4)若有一表面光滑的塑料小球懸浮于Ba(OH)2溶液中央,如圖所示,向該燒杯里緩緩注入與Ba(OH)2溶液等密度的稀硫酸至恰好完全反應。在此實驗過程中,小球將___ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列古詩中對應的化學物質及相關說法均正確的是
選項 | 詩句 | 相關物質 | 相關說法 |
A | 春蠶到死絲方盡 | 纖維素 | 高分子化合物 |
B | 蠟炬成灰淚始干 | 脂肪烴 | 飽和烴 |
C | 滄海月明珠有淚 | 碳酸鈣 | 弱電解質 |
D | 藍田日暖玉生煙 | 二氧化硅 | 兩性氧化物 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com