
【題目】一定溫度下,0.1mol N2和0.3molH2在恒容的密閉容器中發生如下反應:N2(g)+3H2(g) ![]() 2NH3(g) △H<0下列說法不正確的是
2NH3(g) △H<0下列說法不正確的是
A. 達到平衡狀態時,v正(NH3): v逆(N2)=2 : 1
B. c(N2):c(H2):c(NH3)=1:3:2時,說明反應已達到平衡狀態
C. 容器內的壓強不再變化時,說明反應已達到平衡狀態
D. 升高溫度時,v正(NH3)增大,v逆(NH3)增大
 黃岡天天練口算題卡系列答案
黃岡天天練口算題卡系列答案科目:高中化學 來源: 題型:
【題目】一種可充電鋰-空氣電池如圖所示。當電池放電時,O2與Li+在多孔碳材料電極處生成Li2O2-x(x=0或1)。下列說法正確的是

A. 放電時,多孔碳材料電極為負極
B. 放電時,外電路電子由多孔碳材料電極流向鋰電極
C. 充電時,電解質溶液中Li+向多孔碳材料區遷移
D. 充電時,電池總反應為Li2O2-x=2Li+(1-![]() )O2
)O2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素A、B、C、D 原子序數依次增加,X、Y、Z、W是由這四種元素中的兩種元素組成的常見化合物,X為有刺激性氣味的氣體,Y為淡黃色固體,甲是由C元素形成的氣體單質,乙為紅棕色氣體,上述物質之間的轉化關系如下圖所示(部分反應物或生成物省略)。下列說法正確的是

A. 原子半徑大小順序:D>C>B>A B. 最簡單氣態氫化物的穩定性:B>C
C. 圖示轉化關系涉及的反應均為氧化還原反應 D. 元素C、D形成的化合物中一定只含離子鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列說法正確的是
A. 1L0.lmol·L-1的氫氧化鉀溶液中O—H鍵的數目為0.1NA
B. 0.5mol·L-1的碳酸鈉溶液中CO32-的數目小于0.5NA
C. 4.6g金屬鈉與500mL0.2 mol·L-1稀鹽酸充分反應,轉移電子數為0.1 NA
D. 標準狀況下,2.24L乙烯和甲烷混合氣體中含有的氫原子數目為0.4 NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】古瓷中所用顏料的成分一直是個謎,近年來科學家才得知大多為硅酸鹽,如藍紫色的硅酸銅鋇(BaCuSi2Ox,銅為+2價),下列關于硅酸銅鋇的說法不正確的是( )
A.可用氧化物形式表示為BaO·CuO·2SiO2
B.性質穩定,不易脫色
C.易溶解于強酸和強堿
D.x等于6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素A、B、C、D、E、F,它們的原子序數依次增大;A元素的原子是半徑最小的原子;B元素的最高價氧化物對應水化物與其氣態氫化物反應生成一種鹽X;D與A同主族,且與F同周期;F元素的最外層電子數是其次外層電子數的3/4倍,A、B、D、F這四種元素,每一種與C元素都能形成元素的原子個數比不相同的若干種化合物。D、E、F三種元素對應的最高價氧化物的水化物間兩兩皆能反應。請回答下列問題:
(1)寫出B、C、E元素的名稱B___、C___、E___。
(2)請寫出含C質量分數最高的化合物的化學式:______ 。
(3)A、C、D、F四種元素可以形成兩種可以互相反應的酸式鹽(均由四種元素組成),這兩種酸式鹽的化學式分別為______、______。
(4)A、C、F間可形成甲、乙兩種微粒,它們均為負一價雙原子陰離子,且甲有18個電子,乙有10個電子,則甲與乙反應的離子方程式為________________________。
(5)向含有a molE離子的氯化物溶液中加入含b molD的最高價氧化物對應水化物的溶液,生成沉淀的物質的量不可能為_______________________________ 。
①a mol ②b mol ③a/3 mol ④b/3 mol ⑤0⑥(4a-b)mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組為探究難溶性鹽X(僅含三種元素)的組成和性質,設計并完成如下實驗:
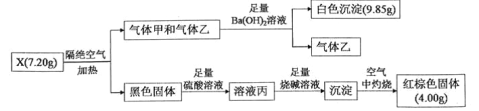
已知:氣體甲和氣體乙組成元素相同,物質的量之比為1:1。請回答:
(1)X的化學式為___________。
(2)溶液丙與H2O2溶液在酸性條件下反應的離子方程式是___________________________。
(3)寫出利用流程圖中某種物質將紅棕色固體重新轉化為黑色固體的化學方程式:____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com