
分析 I.(1)Cu與硝酸反應生成硝酸銅、NO和水,以此書寫離子反應;
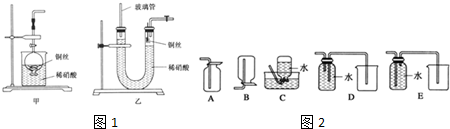
(2)①根據試驗的目的是證明金屬銅和硝酸之間的反應,根據目的選擇所用的材料;
②圖1中試管內有空氣,NO被氧化為紅棕色的氣體;
(3)根據一氧化氮的溶解性和裝置的特點解答;
(4)根據一氧化氮的溶解性與氧氣的反應確定收集方法;
(5)根據得失電子守恒解答,1個銅原子失去2個電子,1個氧分子得到4個電子變成-2價的氧;
II.從經濟角度出發,制取等量的硝酸銅時,所用的原料最少,成本最低;從環境保護的角度出發,制取硝酸銅時不對環境造成污染.
解答 解:I.(1)金屬銅可以和稀硝酸之間反應生成硝酸銅、一氧化氮以及水,即3Cu+8H++2NO3-═3Cu2++4H2O+2NO↑,
故答案為:3Cu+8H++2NO3-═3Cu2++4H2O+2NO↑;
(2)①實驗室若沒有銅絲,銅粒以代替銅絲進行實驗,則包裹桶里的不能是金屬鐵以及金屬鋁,因為他們的活潑性強于金屬銅,會先于金屬銅和硝酸之間發生反應,
故答案為:C、D;
②試管內有空氣,NO容易被氧化為紅棕色的氣體二氧化氮,即2NO+O2═2NO2,故答案為:2NO+O2═2NO2;
(3)①一氧化氮是難溶于水的氣體,當取一氧化氮的裝置產生一氧化氮氣體時,氣體難溶于水,氣體把U形管的液體壓出,
故答案為:接收被氣體壓出U形管的液體,防止稀硝酸溢出;
②讓反應停止,則應該使銅和稀硝酸分開,具體操作方法及原因是關閉U形管右端導氣管上的活塞,反應產生的氣體將U形管右端內的稀硝酸向下壓,使銅絲與稀硝酸分開,反應就會停止,
故答案為:關閉U形管右端導氣管上的活塞,反應產生的氣體將U形管右端內的稀硝酸向下壓,使銅絲與稀硝酸分開,反應就會停止;
(4)由于一氧化氮與氧氣在常溫下反應生成二氧化氮,故不能用排空法收集,所以只能用排水法,故C正確,而D和E排水法收集裝置,應該短進長出,所以D正確,E錯誤,故選:CD;
(5)銅和硝酸反應,銅失去電子,硝酸得到電子變成一氧化氮,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,一氧化氮和氧氣和水反應生成硝酸,4NO+2H2O+3O2=4HNO3,氧氣得電子,一氧化氮失去電子,所以銅失去的電子數等于氧氣得到的電子數,12.8g Cu為 0.2mol,全部溶解,失去0.4mol電子,1個氧分子得到4個電子變成-2價的氧,所以需氧氣0.1mol,0.1mol氧氣在標準狀況下的體積為2240mL,
故答案為:2240mL;
II.甲:銅與濃硝酸制取硝酸銅時的方程式是:Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O,生成的NO2會造成大氣污染,不環保,故甲不正確;
乙:銅與稀硝酸制取硝酸銅時的方程式是:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,生成的NO也會造成大氣污染,不環保,故乙不正確;
丙:此過程中使用到了氯氣,氯氣劇毒,對環保不利,且氯化銅不能與硝酸反應生成硝酸銅,故丙不正確;
丁:此過程用方程式可表示為:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,CuO+2HNO3=Cu(NO3)2+H2O,從過程可以看出該過程不會產生有毒氣體,環保且沒有多消耗原料,故丁正確;
故答案為:丁;制取相同質量的Cu(NO3)2,丁所消耗的HNO3的量最少(原料的利用率最高)且不產生污染環境的氣體;
點評 本題考查了銅與硝酸的反應,掌握相關的化學反應方程式是解答本題的關鍵,注意NO易被氧化及NO對環境的污染,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 石灰石與鹽酸反應:CO32-+2H+=H2O+CO2↑ | |
| B. | 氯化鋁溶液與氨水反應:Al3++3OH-=Al(OH)3↓ | |
| C. | 鐵粉與硝酸銀溶液反應:Fe+3Ag+=Fe3++3Ag | |
| D. | 醋酸與氫氧化鈉溶液反應:CH3COOH+OH-=CH3COO-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.5g-CH3中含有的電子數為6.02×1023 | |
| B. | 標準狀況下.22.4L NO和11.2L O2混合后氣體的分子總數為1.0×6.02×1023 | |
| C. | 工業上用電解法精煉粗銅時,每轉移1mo1電子,陽極上溶解的銅原子數必為0.5×6.02×1023 | |
| D. | VL amo1•L-1氯化鐵溶液中,若Fe3+的數目為6.02×1023,則Cl-的數目大于3×6.02×1023. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
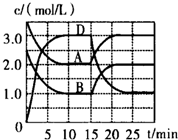 溫度為T時,向V L的密閉容器中充入一定量的A和B,發生反應:A(g)+B(g)?C(s)+xD(g)△H>0,容器中A、B、D的物質的量濃度隨時間的變化如圖所示,下列說法不正確的是( )
溫度為T時,向V L的密閉容器中充入一定量的A和B,發生反應:A(g)+B(g)?C(s)+xD(g)△H>0,容器中A、B、D的物質的量濃度隨時間的變化如圖所示,下列說法不正確的是( )| A. | 反應在前10min的平均反應速率v(B)=0.15mol/(L•min) | |
| B. | 該反應的平衡常數表達式K=$\frac{{c}^{2}(D)}{c(A)•c(B)}$ | |
| C. | 若平衡時保持溫度不變,壓縮容器體積平衡向逆反應方向移動 | |
| D. | 反應至1.5min時,改變的反應條件是降低溫度 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
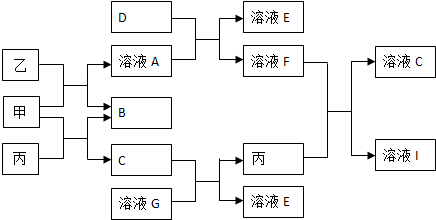
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
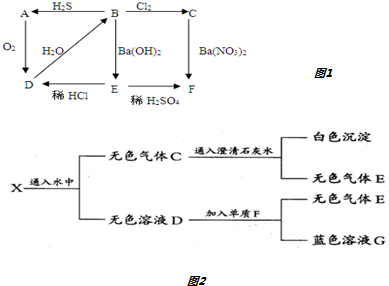
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
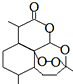 1971年,中國科學家發現、分離、提純了用于治療瘧疾的“青蒿素”,拯救了數千萬人的生命.屠呦呦起了重要的作用,因而與另兩位外國科學家獲得2015年諾貝爾醫學獎.青蒿素分子結構如圖.下列說法錯誤的是( )
1971年,中國科學家發現、分離、提純了用于治療瘧疾的“青蒿素”,拯救了數千萬人的生命.屠呦呦起了重要的作用,因而與另兩位外國科學家獲得2015年諾貝爾醫學獎.青蒿素分子結構如圖.下列說法錯誤的是( )| A. | 青蒿素可以起取代反應 | B. | 青蒿素中的氧均為-2價 | ||
| C. | 青蒿素可以和NaOH溶液反應 | D. | 青蒿素的分子式為C15H22O5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com