
【題目】一定能在下列溶液中大量共存的離子組是 ( )
A.K+、Na+、S2-、MnO4-B.Na+、NH4+、SO42-、Cl-
C.Fe3+、Mg2+、NO3-、SCN-D.NO3-、H+、Fe2+、Cl-
科目:高中化學 來源: 題型:
【題目】鈦的化合物如TiO2、Ti(NO3)4、TiCl4、Ti(BH4)2等均有著廣泛用途。
(1)寫出Ti的基態原子的外圍電子排布式_____。
(2)TiCl4熔點是﹣25℃,沸點136.4℃,可溶于苯或CCl4,該晶體屬于_____晶體;BH4﹣中B原子的雜化類型為_____。
(3)在 TiO2催化作用下,可將CN﹣氧化成CNO﹣,進而得到N2。與CNO﹣互為等電子體的分子化學式為(只寫一種)________。
(4)Ti3+可以形成兩種不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2H2O(綠色)。綠色晶體中配體是_______。

(5)TiO2難溶于水和稀酸,但能溶于濃硫酸,析出含有鈦酰離子的晶體,鈦酰離子常成為鏈狀聚合形式的陽離子,其結構形式如圖1,化學式為______。
(6)金屬鈦內部原子的堆積方式是面心立方堆積方式,如圖2。若該晶胞的密度為ρgcm﹣3,阿伏加德羅常數為NA,則該晶胞的邊長為___cm。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列對于某些離子的檢驗及結論中一定正確的
A. 加入稀鹽酸產生無色的氣體,將氣體通入澄清石灰水中,溶液變渾濁,一定有![]()
B. 加入氯化鋇溶液有白色沉淀產生,再加鹽酸,沉淀不消失,一定有![]()
C. 加入氫氧化鈉溶液并加熱,產生的氣體能使濕潤的紅色石蕊試紙變藍,一定有![]()
D. 加入碳酸鈉溶液產生白色沉淀,再加鹽酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在3S + 6KOH = 2K2S + K2SO3+ 3H2O反應中,作氧化劑的S原子與作還原劑的S原子的物質的量之比是:
A.1∶2B.2∶1C.1∶3D.3∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞氯酸鈉(NaClO2)是一種高效的漂白劑和消毒劑,它在酸性條件下生成NaCl并放出C1O2,C1O2有類似Cl2的性質。某興趣小組探究亞氯酸鈉的制備與性質。

Ⅰ.制備亞氯酸鈉
關閉止水夾②,打開止水夾①,從進氣口通入足量C1O2,充分反應。
(1)儀器a的名稱為_______,儀器b的作用是_____。
(2)裝置A中生成NaC1O2的離子方程式為_______。
(3)若從裝置A反應后的溶液中獲得NaClO2晶體,則主要操作有減壓蒸發濃縮、降溫結晶______、_____干燥等。
Ⅱ.探究亞氯酸鈉的性質
停止通ClO2氣體,再通入空氣一段時間后,關閉止水夾①,打開止水夾②,向A中滴入稀硫酸。
(4)開始時A中反應緩慢,稍后產生氣體的速率急劇加快,請解釋可能的原因_________。
(5)B中現象為_________ 。
(6)實驗完成后,為防止裝置中滯留的有毒氣體污染空氣,可以進行的操作是:再次打開止水夾①,_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵有兩種氯化物,都是重要的化工試劑,一些性質及制備方法如下:
氯化鐵:熔點306℃,沸點315℃,易吸收空氣中的水分而潮解。工業上采用向500600℃的鐵粉中通入氯氣來生產無水氯化鐵。
氯化亞鐵:熔點670℃,易升華。工業上采用向熾熱鐵粉中通入氯化氫來生產無水氯化亞鐵。實驗室可用下圖所示的裝置模擬工業生產無水氯化鐵,請回答相關問題。

(1)裝置A用于KMnO4固體與濃鹽酸反應制氯氣,反應的離子方程式為______________。
(2)彎曲的a管所起的作用是_____________;裝置采用較粗的導管來連接裝鐵粉的硬質玻璃管和廣口瓶C,其目的是____________________。
(3)導管b 口應與 (從虛線框裝置中選擇裝置的字母序號)連接,這樣可避免反應系統與環境間的相互影響。
(4)實驗完成后,取廣口瓶C中收集到的產物進行如下測定分析:
①稱取4.52g樣品溶于過量的稀鹽酸中:②加入足量H2O2;③再加入足量NaOH溶液:④過濾、洗滌后灼燒沉淀;⑤稱量所得紅棕色固體為2.40g。則該樣品中Fe元素的質量分數為________%。
(5)由上分析數據和計算得出結論:用此裝置制得的無水氯化鐵含鐵最偏高,顯然其中含有較多的FeCl2雜質。
①產生FeCl2雜質的原因是___________________。
②若要得到較純凈的無水氯化鐵,可采取的裝置改進措施是______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A. 鋼鐵表面水膜酸性很弱或呈中性,發生吸氧腐蝕

B. 鋼鐵表面水膜酸性較強,發生析氫腐蝕

C. 鋼閘門作為陰極而受到保護

D. 將鋅板換成銅板對鋼閘門保護效果更好

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】己二酸主要用于生產尼龍66鹽、合成樹脂及增塑劑等。已二酸的合成路線如下:

制備己二酸的裝置示意圖如圖所示(加熱和夾持裝置等略)。
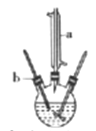
實驗步驟:
I.己二酸的制備
連裝好裝置后,通過瓶口b慢慢滴加1.5g環已醇至適量KMnO4和NaOH的混合溶液中,然后塞上帶有溫度計的膠塞,再用沸水浴加熱數分鐘。
II.分離提純
趁熱過濾,收集濾液,用少量熱水洗滌濾渣2次,合并濾液和洗滌液,邊攪拌邊滴加濃鹽酸至溶液呈強酸性,小心加熱蒸發濃縮至10mL左右,在冷水浴中冷卻,析出已二酸粗品。
回答下列問題:
(1)寫出儀器a的名稱:______________。
(2)分離提純過程中滴加的濃鹽酸的作用是______________。
(3)將已二酸粗品提純的方法是_______________。
A.過濾 B.萃取 C.重結晶 D.蒸餾
(4)步驟II中過濾時需要用到的玻璃儀器有玻璃棒____、_____。洗滌濾渣的目的是__________。
(5)若制得純已二酸的質量為1.5g,則己二酸的產率為__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com