
(1)對于下列反應:2SO2(g) + O2(g) 2SO3(g) , 如果2min內SO2的濃度由6 mol/L下降為2 mol/L,用SO2濃度變化來表示的化學反應速率為____________,如果開始時SO2濃度為4mol/L,2min后反應達平衡,若這段時間內v(O2)為0.5mol/(L·min),那么2min時SO2的濃度為_________。
2SO3(g) , 如果2min內SO2的濃度由6 mol/L下降為2 mol/L,用SO2濃度變化來表示的化學反應速率為____________,如果開始時SO2濃度為4mol/L,2min后反應達平衡,若這段時間內v(O2)為0.5mol/(L·min),那么2min時SO2的濃度為_________。
(2)下圖表示在密閉容器中反應:2SO2+O2 2SO3 △H<0達到平衡時,由于條件改變而引起反應速度和化學平衡的變化情況,a~b過程中改變的條件可能是________;b~c過程中改變的條件可能是_________; 若增大壓強時,反應速度變化情況畫在c~d處。
2SO3 △H<0達到平衡時,由于條件改變而引起反應速度和化學平衡的變化情況,a~b過程中改變的條件可能是________;b~c過程中改變的條件可能是_________; 若增大壓強時,反應速度變化情況畫在c~d處。

(3)以上反應達平衡后,若此時只將容器的體積擴大為原來的2倍,達新平衡時,容器內溫度將_______(容器不與外界進行熱交換,填“升高”或“降低”);達新平衡時,容器內混合氣體的平均相對分子質量比原平衡時________(填“增大”、“減小”或“相等”)。
 期末金牌卷系列答案
期末金牌卷系列答案 輕松課堂標準練系列答案
輕松課堂標準練系列答案科目:高中化學 來源:2015-2016學年江蘇省高二下學期期末化學試卷(解析版) 題型:選擇題
用4種溶液進行實驗,下表中“操作及現象”與“溶液”對應關系錯誤的是
選項 | 操作及現象 | 溶液 |
A | 通入CO2,溶液不變渾濁;先通入氨氣再通入CO2,溶液變渾濁 | CaCl2溶液 |
B | 通入CO2,溶液變渾濁,繼續通CO2至過量,渾濁消失 | Na2SiO3溶液 |
C | 通入CO2,溶液變渾濁,再加入品紅溶液,紅色不褪去 | Ca(ClO)2溶液 |
D | 通入CO2,溶液變渾濁,繼續通CO2至過量,渾濁消失,再加入足量NaOH溶液,又變渾濁 | Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高二6月月考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A、金屬鈉著火時使用泡沫滅火器
B、23克鈉與足量的水完全反應后可以生成0.5NA個H2
C、鈉與硫酸銅溶液反應的離子方程式是2Na+Cu2+=Cu↓+2Na+
D、工業電解氯化鈉的溶液制備金屬鈉
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省宿遷市高二下學期期末考試化學試卷(解析版) 題型:選擇題
下列反應的離子方程式正確的是
A.硫酸與氫氧化鋇溶液反應:H+ + OH-= H2O
B.稀H2SO4與鐵粉反應:2Fe+6H+=2Fe3+ + 3H2↑
C.氯氣通入水中:Cl2+H2O 2H+ +Cl-+ClO-
2H+ +Cl-+ClO-
D.AlCl3溶液中加入足量的氨水:Al3++ 3NH3·H2O = Al(OH)3↓+3NH4+
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省宿遷市高二下學期期末考試化學試卷(解析版) 題型:選擇題
化學與能源開發、環境保護、資源利用等密切相關。下列說法正確的是
A.垃圾是放錯地方的資源,應分類回收利用
B.實現化石燃料清潔利用,就無需開發新能源
C.為提高農作物的產量和質量,應大量使用化肥和農藥
D.將廢棄的植物油(即“地溝油”)蒸餾可以重新作為食用油
查看答案和解析>>
科目:高中化學 來源:2014-2015學年湖南省高二下學期期末考試化學試卷(解析版) 題型:選擇題
下圖 為直流電源,
為直流電源, 為浸透飽和氯化鈉溶液和酚酞試液的濾紙,
為浸透飽和氯化鈉溶液和酚酞試液的濾紙, 為電鍍槽.接通電路后發現
為電鍍槽.接通電路后發現 上的c點顯紅色.為實現鐵上鍍鋅,接通
上的c點顯紅色.為實現鐵上鍍鋅,接通 后,使c、d兩點短路.下列敘述正確的是
后,使c、d兩點短路.下列敘述正確的是
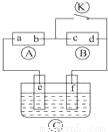
A.a為直流電源的負極
B.c極發生的反應為2H++2e-=H2↑
C.f電極為鋅板
D.e極發生還原反應
查看答案和解析>>
科目:高中化學 來源:2014-2015學年湖南省高二下學期期末考試化學試卷(解析版) 題型:選擇題
在體積恒定的密閉容器中,充入3 mol A和1 mol B發生反應:3A(g)+B(g) xC(g),達到平衡后,C在平衡混合氣體中的體積分數為φ。若維持溫度不變,按1.2 mol A、0.4 mol B、0.6 mol C為起始物質,達到平衡后壓強不變,C的體積分數仍為φ,則x值是( )
xC(g),達到平衡后,C在平衡混合氣體中的體積分數為φ。若維持溫度不變,按1.2 mol A、0.4 mol B、0.6 mol C為起始物質,達到平衡后壓強不變,C的體積分數仍為φ,則x值是( )
A.2 B.1 C.3 D.4
查看答案和解析>>
科目:高中化學 來源:2015-2016學年中國石油天然氣管道局中學高一下第二次月考化學試卷(解析版) 題型:填空題
通常把拆開1 mol某化學鍵所吸收的能量看成該化學鍵的鍵能.已知部分化學鍵的鍵能如下:
化學鍵 | N—H | N—N | O=O | N≡N | O—H |
鍵能(kJ·mol-1) | 386 | 167 | 498 | 946 | 460 |
(1)發射神舟飛船的長征火箭用了肼(N2H4,氣態)為燃料,若它在氧氣(氣態)中燃燒,生成N2(氣態)和H2O(液態)。肼完全燃燒的熱化學方程式可寫為____ ____。
(2)肼-空氣燃料電池是一種堿性燃料電池,電解質溶液是20%~30%的KOH 溶液。肼-空氣燃料電池放電時,負極的電極反應式是______________________________________。
(3)已知N60分子中每個N原子均以氮氮鍵結合三個氮原子,且N60分子結構中每個氮原子均形成8個電子的穩定結構。試推測1個N60的結構含有________個N—N鍵。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年中國石油天然氣管道局中學高二下第二次月考化學試卷(解析版) 題型:選擇題
用H2O2溶液處理含NaCN的廢水的反應原理為:NaCN+H2O2+H2O===NaHCO3+NH3,已知:HCN
的酸性比H2CO3弱。下列有關說法正確的是( )
A.該反應中氮元素被氧化
B.該反應中H2O2作還原劑
C.0.1mol·L-1NaCN溶液中含有HCN和CN-的總數為0.1×6.02×1023
D.實驗室配制NaCN溶液時,需加入適量的NaOH溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com