
【題目】某學校化學興趣小組為探索金屬回收物的綜合利用,專門設計實驗用含有鋁、鐵、銅的合金制取純凈的氯化鋁溶液、綠礬晶體(FeSO4·7H2O)和膽礬晶體(CuSO4·5H2O),其實驗方案如下:
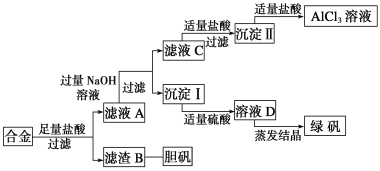
請回答下列問題:
(1)過濾用的玻璃儀器有___________________________________________________。
(2)在濾液C轉化為沉淀Ⅱ的過程中鹽酸的用量不易控制,可改為通CO2氣體,寫出濾液C中通入過量CO2的離子方程式:______________________________________________。
寫出由沉淀Ⅱ轉化為AlCl3溶液的離子方程式:_____________________________。
(3)小組成員經過檢測,發現制得的綠礬不純,試分析其主要含有哪些雜質:_______________________________,要想由沉淀Ⅰ最終制得純度較高的綠礬,應如何改進___________________________________
(4)小組成員從資料中獲知H2O2是一種綠色氧化劑,在濾渣B中加入稀硫酸和H2O2來制備膽礬晶體,則該反應的總化學方程式為_______________________________。
(5)有同學提出可將方案中最初溶解合金的鹽酸改為燒堿,重新設計方案,也能最終制得三種物質,你認為第二種方案相對于第一種方案________(填“更合理”或“不合理”),理由是________________________。
【答案】燒杯、漏斗、玻璃棒 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- Al(OH)3+3H+=Al3++3H2O 氯化鈉、硫酸鈉、硫酸鐵 向溶液D中加入足量鐵粉,反應后過濾,再將濾液蒸發濃縮、冷卻結晶、過濾即可得純度較高的綠礬 Cu+H2O2+H2SO4+3H2O=CuSO4·5H2O(或Cu+H2O2+H2SO4=CuSO4+2H2O) 更合理 前一種方案操作步驟多、時間長、消耗試劑量大
【解析】
合金鋁、鐵、銅加入足量鹽酸溶解后過濾,得到濾液A為氯化鋁、氯化亞鐵,加入足量氫氧化鈉溶液過濾得到濾液C為偏鋁酸鈉溶液,加入適量鹽酸過濾得到氫氧化鋁沉淀,氫氧化鋁加入鹽酸溶解生成氯化鋁溶液;沉淀Ⅰ為氫氧化亞鐵,加入硫酸生成硫酸亞鐵,溶液D蒸發結晶得到綠礬晶體;
(1)根據過濾實驗用到的儀器來回答;
(2)濾液C中含有偏鋁酸鈉,通入過量CO2生成氫氧化鋁沉淀和碳酸氫鈉,沉淀Ⅱ為氫氧化鋁,與鹽酸反應轉化為AlCl3溶液;
(3)制得的綠礬不純,部分亞鐵離子被氧化為鐵離子,要想由沉淀I最終制得純度較高的綠礬,需要向D溶液中加入過量鐵粉還原鐵離子過濾后溶液通過操作得到晶體;
(4)銅、稀硫酸、雙氧水的性質來判斷反應的發生,并結合質量守恒定律寫出該反應的化學方程式;
(5)根據實驗中的酸和堿的量的情況來對比回答。
合金鋁、鐵、銅加入足量鹽酸溶解后過濾,得到濾液A為氯化鋁、氯化亞鐵,加入足量氫氧化鈉溶液過濾得到濾液C為偏鋁酸鈉溶液,加入適量鹽酸過濾得到氫氧化鋁沉淀加入鹽酸溶解生成氯化鋁溶液;沉淀Ⅰ為氫氧化亞鐵,加入硫酸生成硫酸亞鐵溶液D蒸發結晶得到綠礬晶體;
(1)過濾實驗用到的儀器有:濾紙、鐵架臺、鐵圈、燒杯、玻璃棒和漏斗,故答案為:燒杯、漏斗、玻璃棒;
(2)濾液C中含有偏鋁酸鈉,通入過量CO2生成氫氧化鋁沉淀和碳酸氫鈉,反應的離子方程式為AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,沉淀Ⅱ為氫氧化鋁,與鹽酸反應轉化為AlCl3溶液,反應的離子方程式為Al(OH)3+3H+═Al3++3H2O;
(3)發現制得的綠礬不純,含有氯化鈉、硫酸鈉、硫酸鐵,是因為亞鐵離子被氧化為鐵離子,要想由沉淀I最終制得純度較高的綠礬,需要向D溶液中加入過量鐵粉還原鐵離子為亞鐵離子,過濾得到溶液蒸發濃縮,冷卻結晶,過濾洗滌得到綠礬晶體;
(4)銅與濃硫酸反應生成有毒有污染的二氧化硫氣體,若銅先和氧氣反應生成氧化銅,然后氧化銅會和硫酸反應生成硫酸銅,不會產生污染大氣的氣體,該過程原料利用率高,所以途徑②最佳,Cu中加入稀硫酸和H2O2可以制備膽礬晶體,反應方程式為:Cu+H2O2+H2SO4+3H2O═CuSO45H2O(或Cu+H2O2+H2SO4═CuSO4+2H2O;
(5)在實驗原方案中,需要的是適量的酸,且步驟繁瑣,這很難控制,改用燒堿,首先分離出來鋁,然后加入硫酸,分離出鐵,最后得銅的化合物,故比較合理。


 Happy holiday歡樂假期暑假作業廣東人民出版社系列答案
Happy holiday歡樂假期暑假作業廣東人民出版社系列答案 快樂暑假暑假能力自測中西書局系列答案
快樂暑假暑假能力自測中西書局系列答案科目:高中化學 來源: 題型:
【題目】I.(化學反應原理)
原電池原理的發現是儲能和供能技術的巨大進步,是化學對人類的一項重大貢獻。將純鋅片和純銅片按圖方式插入100mL相同濃度的稀硫酸中一段時間,回答下列問題:

(1)在相同時間內, 兩燒杯中產生氣泡的速度:甲__乙(填“>”“<”或“=”)。
(2)請寫出圖中構成原電池的負極電極反應式:__。
II.(化學與生活)
材料是人類生存和發展的物質基礎,合理使用材料可以改善我們的生活。
(1)在原子反應堆中得以廣泛應用的鈉鉀合金在常溫下呈液態,說明合金的熔點比其各成分金屬的熔點___。(選填“高”或“低”)
(2)石英玻璃纖維又稱光導纖維,其主要成分和NaOH溶液反應的化學方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學家用蘸墨汁書寫后的紙張作為空氣電極,設計并組裝了輕型、柔性、能折疊的可充電鋰空氣電池如圖甲,電池的工作原理如圖乙。下列有關說法正確的是

A. 放電時,紙張中的纖維素作為鋰電池的負極
B. 充電時,若陽極放出1molO2,則有4mol e-回到電源正極
C. 開關K閉合給鋰電池充電,X對應充電電極上的反應為Li++e-=Li
D. 放電時,Li+由正極經過有機電解質溶液移向負極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】阿伏加德羅常數的值為![]() 。下列說法正確的是
。下列說法正確的是
A. 1L0.1mol·![]() NH4Cl溶液中,
NH4Cl溶液中, ![]() 的數量為0.1
的數量為0.1![]()
B. 2.4gMg與H2SO4完全反應,轉移的電子數為0.1![]()
C. 標準狀況下,2.24LN2和O2的混合氣體中分子數為0.2![]()
D. 0.1mol H2和0.1mol I2于密閉容器中充分反應后,其分子總數為0.2![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于甲、乙、丙、丁四種有機物說法正確的是
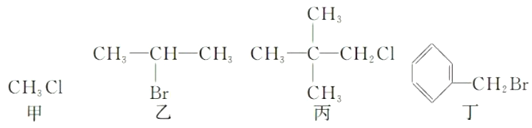
A.丁屬于芳香烴
B.四種物質中加入NaOH溶液共熱,然后加入稀硝酸調至酸性,再滴入AgNO3溶液,均有沉淀生成
C.四種物質中加入NaOH的醇溶液共熱,后加入稀硝酸至酸性,再滴入AgNO3溶液,均有沉淀生成
D.乙發生消去反應得到兩種烯烴
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向20.00mL0.1mol·L-1氨水中滴入0.1mol·L-1 鹽酸,溶液中由水電離出的c(H+)的負對數[-1gc水(H+)]與所加鹽酸體積的關系如圖所示,下列說法正確的是( )

A.常溫下,Kb(NH3·H2O)約為1×10-3
B.b=20.00
C.R、Q兩點對應溶液均呈中性
D.R到N、N到Q所加鹽酸體積相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】直接排放含SO2的煙氣會形成酸雨,危害環境。利用鈉堿循環法可脫除煙氣中的SO2。
(1)用化學方程式表示SO2形成硫酸型酸雨的反應:______________。
(2)在鈉堿循環法中,Na2SO3溶液作為吸收液,可由NaOH溶液吸收SO2制得,該反應的離子方程式是________________________
(3)吸收液吸收SO2的過程中,pH隨n(SO3﹣):n(HSO3﹣)變化關系如下表:
n(SO﹣):n(HSO﹣) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①上表判斷NaHSO3溶液顯______性,用化學平衡原理解釋:____________
②當吸收液呈中性時,溶液中離子濃度關系正確的是(選填字母):____________
a.c(Na+)=2c(SO32-)+c(HSO3-),
b.c(Na+)> c(HSO3-)> c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)= c(SO32-)+ c(HSO3-)+c(OH-)
(4)當吸收液的pH降至約為6時,需送至電解槽再生。再生示意圖如下:
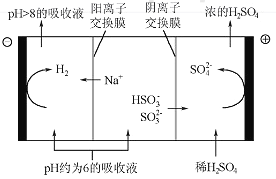
①HSO3-在陽極放電的電極反應式是_______________。
②當陰極室中溶液pH升至8以上時,吸收液再生并循環利用。簡述再生原理:__________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】秦皮是一種常用的中藥,具有抗炎鎮痛、抗腫瘤等作用。“秦皮素”是其含有的一種有效成分,結構簡式如圖所示,有關其性質敘述不正確的是( )

A.該有機物分子式為C10H8O5
B.分子中有四種官能團
C.該有機物能發生加成、氧化、取代等反應
D.1mol該化合物最多能與3molNaOH反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W為四種常見的短周期元素。其中Y元素原子核外最外層電子數是其電子層數的3倍,它們在周期表中的相對位置如圖所示:
X | Y | |
Z | W |
請回答以下問題:
(1)W在周期表中位置___;
(2)X和氫能夠構成+1價陽離子,其電子式是___,Y的氣態氫化物比Z的氣態氫化物的沸點高,緣故是___;
(3)X的最高價氧化物的水化物與其氫化物能化合生成M,M的晶體類型為___,M的水溶液顯酸性的緣故是___(用離子方程式表示)。
(4)①Y和Z可組成一種氣態化合物Q,Q能與W的單質在潮濕環境中反應,反應的化學方程式是___。
②在一定條件下,化合物Q與Y的單質反應達平衡時有三種氣態物質,反應時,每轉移4mol電子放熱190.0kJ,該反應的熱化學方程式是___。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com