

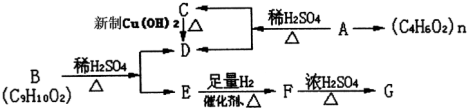
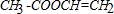 .B在稀硫酸、加熱條件下發生水解反應生成E和乙酸,則B屬于酯,根據碳原子守恒知,E中含有7個碳原子,分子式為C7H8O,E能溶于NaOH溶液,說明E含有酚羥基,F轉化為G時,產物只有一種結構且能使溴水褪色,說明G含有碳碳雙鍵,且F中酚羥基和甲基處于對位,則E的結構簡式為:
.B在稀硫酸、加熱條件下發生水解反應生成E和乙酸,則B屬于酯,根據碳原子守恒知,E中含有7個碳原子,分子式為C7H8O,E能溶于NaOH溶液,說明E含有酚羥基,F轉化為G時,產物只有一種結構且能使溴水褪色,說明G含有碳碳雙鍵,且F中酚羥基和甲基處于對位,則E的結構簡式為: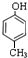 ,E和乙酸發生酯化反應生成B,B的結構簡式為:
,E和乙酸發生酯化反應生成B,B的結構簡式為: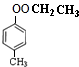 ,E和氫氣發生加成反應生成F,則F的結構簡式為:
,E和氫氣發生加成反應生成F,則F的結構簡式為: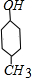 ,F發生消去反應生成G,則G的結構簡式為
,F發生消去反應生成G,則G的結構簡式為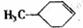 .
.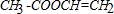 .B在稀硫酸、加熱條件下發生水解反應生成E和乙酸,則B屬于酯,根據碳原子守恒知,E中含有7個碳原子,分子式為C7H8O,E能溶于NaOH溶液,說明E含有酚羥基,F轉化為G時,產物只有一種結構且能使溴水褪色,說明G含有碳碳雙鍵,且F中酚羥基和甲基處于對位,則E的結構簡式為
.B在稀硫酸、加熱條件下發生水解反應生成E和乙酸,則B屬于酯,根據碳原子守恒知,E中含有7個碳原子,分子式為C7H8O,E能溶于NaOH溶液,說明E含有酚羥基,F轉化為G時,產物只有一種結構且能使溴水褪色,說明G含有碳碳雙鍵,且F中酚羥基和甲基處于對位,則E的結構簡式為 ,E和乙酸發生酯化反應生成B,B的結構簡式為
,E和乙酸發生酯化反應生成B,B的結構簡式為 ,E和氫氣發生加成反應生成F,則F的結構簡式為
,E和氫氣發生加成反應生成F,則F的結構簡式為 ,F發生消去反應生成G,則G的結構簡式為
,F發生消去反應生成G,則G的結構簡式為 ,
, ,故答案為:
,故答案為: ;
;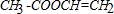 ,含有羧基、碳碳雙鍵,故答案為:羧基、碳碳雙鍵;
,含有羧基、碳碳雙鍵,故答案為:羧基、碳碳雙鍵; 發生消去反應生成
發生消去反應生成 ,故答案為:消去反應;
,故答案為:消去反應;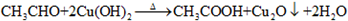 ,故答案為:
,故答案為: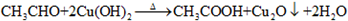 ;
; )的同分異構體滿足下列條件:①含苯環且苯環上只有兩個取代基,③遇FeCl3溶液顯紫色,含有酚羥基; ④能發生銀鏡反應,含有醛基,②苯環上的一取代物只有兩種,兩個取代基處于對位,符合條件的B的同分異構體有
)的同分異構體滿足下列條件:①含苯環且苯環上只有兩個取代基,③遇FeCl3溶液顯紫色,含有酚羥基; ④能發生銀鏡反應,含有醛基,②苯環上的一取代物只有兩種,兩個取代基處于對位,符合條件的B的同分異構體有 ,
, 任意一種.
任意一種.


科目:高中化學 來源: 題型:
| A、n | B、2n | C、3n | D、4n |
查看答案和解析>>
科目:高中化學 來源: 題型:
 浙江省“五水共治”是水質治理的重要舉措,其中化學需氧量(COD)是水質測定中的重要指標,可以反映水中有機物等還原劑的污染程度.COD是指在一定條件下,用強氧化劑氧化水樣中的還原劑及有機物時所消耗氧化劑的量,然后折算成氧化水樣中的這些還原劑及有機物時需要氧氣的量.某學習小組用重鉻酸鉀法測定某水樣中的COD.主要的實驗裝置、儀器及具體操作步驟如下:實驗裝置及儀器:
浙江省“五水共治”是水質治理的重要舉措,其中化學需氧量(COD)是水質測定中的重要指標,可以反映水中有機物等還原劑的污染程度.COD是指在一定條件下,用強氧化劑氧化水樣中的還原劑及有機物時所消耗氧化劑的量,然后折算成氧化水樣中的這些還原劑及有機物時需要氧氣的量.某學習小組用重鉻酸鉀法測定某水樣中的COD.主要的實驗裝置、儀器及具體操作步驟如下:實驗裝置及儀器: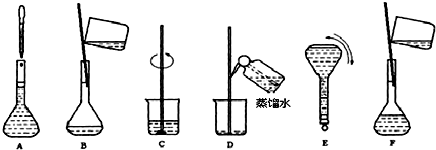
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
 短周期主族元素X、Y、Z、W的原子序數依次增大,X、Y、Z原子序數之和是W的2倍,X、Z在周期表中的相對位置如圖所示,X的最低負價絕對值與其原子最外層電子數相等.下列說法不正確的是( )
短周期主族元素X、Y、Z、W的原子序數依次增大,X、Y、Z原子序數之和是W的2倍,X、Z在周期表中的相對位置如圖所示,X的最低負價絕對值與其原子最外層電子數相等.下列說法不正確的是( )| A、原子半徑:Y>Z>W |
| B、一定條件下,Y可置換出X |
| C、氣態氫化物穩定性:Z>W |
| D、熔點YW2>XW4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 電離平衡常數(25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
| A、0.1mol?L-1NaHCO3溶液中濃度的大小:c(Na+)>c(HCO 3-)>c(H+)>c(OH-) |
| B、少量的CO2通入到NaCN溶液中 CN-+H2O+CO2=HCN+HCO 3- |
| C、用0.1mol?L-1NaOH溶液中和等濃度的HCN和HCOOH時前者所需NaOH溶液體積大 |
| D、0.1mol?L-1HCOONa溶液比0.1mol?L-1NaCN溶液所含離子總數小 |
查看答案和解析>>
科目:高中化學 來源: 題型:
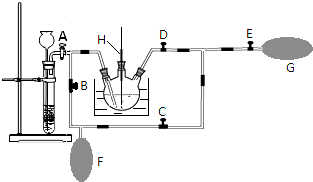 高錳酸鉀是一種用途廣泛的強氧化劑,實驗室制備高錳酸鉀所涉及的化學方程式如下:MnO2熔融氧化:3MnO2+KClO3+6KOH
高錳酸鉀是一種用途廣泛的強氧化劑,實驗室制備高錳酸鉀所涉及的化學方程式如下:MnO2熔融氧化:3MnO2+KClO3+6KOH
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、FeSO4在反應中作氧化劑 |
| B、隨著反應的進行,該廢水的pH會減小 |
| C、若該反應轉移0.6mol e-,則會有0.2mol Cr2O72- 被還原 |
| D、除去廢水中含鉻元素離子的過程包括氧化還原反應和復分解反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
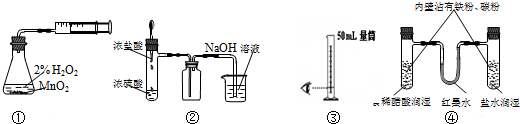
| A、裝置①測定化學反應速率 |
| B、裝置②制取并吸收HCl |
| C、裝置③量取8.5mL的稀硫酸 |
| D、裝置④模擬鐵的腐蝕 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com