
酸性條件下,錫在水溶液中有Sn2+、Sn4+兩種主要存在形式。SnSO4是一種重要的硫酸鹽,廣泛應用于鍍錫工業,其制備的工藝流程如下:
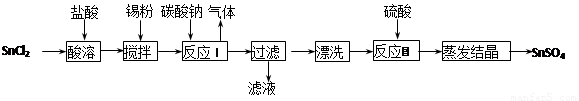
回答下列問題:
(1) SnCl2用鹽酸而不用水直接溶解的原因是 ,加入錫粉的作用是 。
(2) 反應I生成的沉淀為SnO,寫出該反應的化學方程式:
。
(3) 檢驗沉淀已經“洗滌”干凈的操作是: 。
(4)反應II硫酸的作用之一是控制溶液的pH。若溶液中c(Sn2+)=1.0mol·L-1,則室溫下應控制溶液pH 。(已知:Ksp[Sn(OH)2]=1.0×10-26)
(5)酸性條件下,SnSO4還可用作雙氧水的去除劑,試寫出所發生反應的離子方程式:
。
(6)潮濕環境中,鍍錫銅即使錫層破損也能防止形成銅綠,請結合有關的原理解釋其原因: 。
(16分)
(1)抑制Sn2+水解(2分) 防止Sn2+被氧化(2分)
(2)SnCl2 + Na2CO3 = SnO↓ + CO2↑+2NaCl(2分)
(3)取少量最后一次洗滌液于試管中,滴入幾滴AgNO3溶液,若無白色沉淀生成,則說明沉淀已洗滌干凈。(3分)
(4)小于1 (3分。若寫成≤1給1分)
(5)Sn2+ + H2O2 + 2H+ = Sn4+ + 2H2O(2分)
(6)潮濕環境中,Sn與Cu構成原電池,Sn作為負極,保護正極Cu不被氧化。(2分)
【解析】
試題分析:(1)SnCl2是強酸弱堿鹽,能水解,即SnCl2+2H2O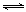 Sn(OH)2+2HCl,直接用水溶解或稀釋能促進Sn2+水解,用鹽酸溶解,增大氫離子或氯化氫濃度使水解平衡向逆反應方向移動,即抑制Sn2+水解;讀圖可知,目標產物是SnSO4,其中所含錫元素的化合價為+2價,已知錫在水溶液中有Sn2+、Sn4+,說明加入錫粉的主要目的是防止Sn2+氧化為Sn4+或者將Sn4+還原為Sn2+;(2)Na2CO3與HCl容易發生反應,生成NaCl、H2O和CO2氣體,促進SnCl2水解,生成的Sn(OH)2易分解為SnO沉淀和水,根據工藝流程圖順推和逆推,反應I的反應物為SnCl2、Na2CO3,生成物為SnO、NaCl、CO2,由于沒有元素化合價變化,則反應I屬于復分解反應,根據質量守恒定律,則SnCl2+Na2CO3=SnO↓+CO2↑+2NaCl;(3)由于沉淀具有較強的吸附性,則SnO沉淀中吸附了可溶性的NaCl和過量的Na2CO3,因此檢驗沉淀已經洗滌干凈的方法是設計焰色反應不是黃色或檢驗氯離子或碳酸根離子的實驗方案,最簡單合理的操作是取少量最后一次洗滌液于試管中,滴入幾滴AgNO3溶液,若無白色沉淀生成,則說明沉淀已洗滌干凈;(4)由于Sn(OH)2(s)
Sn(OH)2+2HCl,直接用水溶解或稀釋能促進Sn2+水解,用鹽酸溶解,增大氫離子或氯化氫濃度使水解平衡向逆反應方向移動,即抑制Sn2+水解;讀圖可知,目標產物是SnSO4,其中所含錫元素的化合價為+2價,已知錫在水溶液中有Sn2+、Sn4+,說明加入錫粉的主要目的是防止Sn2+氧化為Sn4+或者將Sn4+還原為Sn2+;(2)Na2CO3與HCl容易發生反應,生成NaCl、H2O和CO2氣體,促進SnCl2水解,生成的Sn(OH)2易分解為SnO沉淀和水,根據工藝流程圖順推和逆推,反應I的反應物為SnCl2、Na2CO3,生成物為SnO、NaCl、CO2,由于沒有元素化合價變化,則反應I屬于復分解反應,根據質量守恒定律,則SnCl2+Na2CO3=SnO↓+CO2↑+2NaCl;(3)由于沉淀具有較強的吸附性,則SnO沉淀中吸附了可溶性的NaCl和過量的Na2CO3,因此檢驗沉淀已經洗滌干凈的方法是設計焰色反應不是黃色或檢驗氯離子或碳酸根離子的實驗方案,最簡單合理的操作是取少量最后一次洗滌液于試管中,滴入幾滴AgNO3溶液,若無白色沉淀生成,則說明沉淀已洗滌干凈;(4)由于Sn(OH)2(s)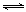 Sn2++2OH-,則Ksp[Sn(OH)2]=c(Sn2+)•c2(OH-),即c2(OH-)= Ksp[Sn(OH)2]/c(Sn2+),c(OH-)=
1.0×10-13mol/L;由于Kw= c(H+)•c(OH-)= 1.0×10-14,則c(H+)= Kw/c(OH-)= 1.0×10-1 mol/L,則pH=—lg c(H+)=1;為了防止析出Sn(OH)2沉淀,必須使溶液中Qc[Sn(OH)2]<Ksp[Sn(OH)2],則c(OH-)
<1.0×10-13mol/L,即c(H+)>1.0×10-1
mol/L,pH<1;(5)雙氧水具有氧化性,能將錫元素從+2價氧化為+4價,而過氧化氫被還原為水,根據最小公倍數法配平,由電子、電荷和原子守恒可得:Sn2+ + H2O2 +
2H+ = Sn4+ + 2H2O;(6)金屬活動順序表中錫位于銅前,構成原電池時,錫是負極,銅是正極,則錫被腐蝕,銅被保護,即使錫層破損也能防止銅腐蝕,這是犧牲陽極的陰極保護法的應用。
Sn2++2OH-,則Ksp[Sn(OH)2]=c(Sn2+)•c2(OH-),即c2(OH-)= Ksp[Sn(OH)2]/c(Sn2+),c(OH-)=
1.0×10-13mol/L;由于Kw= c(H+)•c(OH-)= 1.0×10-14,則c(H+)= Kw/c(OH-)= 1.0×10-1 mol/L,則pH=—lg c(H+)=1;為了防止析出Sn(OH)2沉淀,必須使溶液中Qc[Sn(OH)2]<Ksp[Sn(OH)2],則c(OH-)
<1.0×10-13mol/L,即c(H+)>1.0×10-1
mol/L,pH<1;(5)雙氧水具有氧化性,能將錫元素從+2價氧化為+4價,而過氧化氫被還原為水,根據最小公倍數法配平,由電子、電荷和原子守恒可得:Sn2+ + H2O2 +
2H+ = Sn4+ + 2H2O;(6)金屬活動順序表中錫位于銅前,構成原電池時,錫是負極,銅是正極,則錫被腐蝕,銅被保護,即使錫層破損也能防止銅腐蝕,這是犧牲陽極的陰極保護法的應用。
考點:考查有關物質制備的化學工藝流程,涉及解釋加入試劑的原因和作用、書寫關鍵步驟的化學方程式、設計檢驗沉淀是否洗滌干凈的實驗方案、溶度積和水的離子積的有關計算、書寫主要流程的離子方程式、根據原電池原理解釋錫層破損也能防止銅腐蝕的原因等。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2013-2014學年山東省淄博市高三3月模擬考試理綜化學試卷(解析版) 題型:填空題
硫酸亞錫(SnSO4)、四氯化錫(SnCl4)常用于印染和電鍍工業。
(1)某研究小組設計SnSO4制備路線如下:

已知:酸性條件下,錫在水溶液中有Sn2+、Sn4+兩種主要存在形式,Sn2+易被氧化;SnCl2極易水解。
①SnCl2酸溶后加入Sn粉的作用是??????????????????????? 。
②步驟Ⅱ中用到的玻璃儀器除燒杯外還有????????????? ;步驟Ⅳ中需要洗滌固體SnO中含有的雜質,檢驗SnO中的Cl-是否洗滌干凈的操作為???????????????? 。
③步驟Ⅴ涉及到的操作有:a.過濾? b.洗滌? c.蒸發濃縮? d.冷卻結晶? e.低溫干燥,則其正確的操作順序為??????????????????????? 。
(2)實驗室擬用以下裝置,用熔融的金屬錫與干燥純凈的氯氣制取無水SnCl4(SnCl4熔點-33℃,沸點114.1℃,遇潮濕空氣極易水解),此反應過程放出大量的熱。
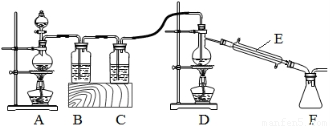
①裝置C中應加入試劑為___________;儀器E的名稱為____________________。
②反應開始生成SnCl4時,可以先熄滅___(填字母序號)處的酒精燈,理由是________。
③該實驗裝置設計尚存在缺陷,改進的方法是(包括儀器、試劑及連接位置等)______________。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年安徽省“江南十校”高三3月聯考理綜化學試卷(解析版) 題型:填空題
硫酸亞錫(SnSO4)是一種重要的能溶于水的硫酸鹽,廣泛應用于鍍錫工業。某研究小組
設計SnSO4制備路線如下:
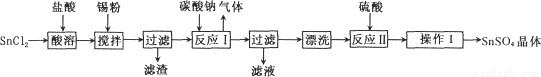
查閱資料:
I.酸性條件下,錫在水溶液中有Sn2+、Sn4+兩種主要存在形式,Sn2+易被氧化。
Ⅱ.SnC12易水解生成堿式氯化亞錫[Sn(OH)Cl]
回答下列問題:
(1)操作l的步驟為 ____、____、過濾、洗滌、干燥。對沉淀進行洗滌的方法是_____________。
(2) SnCl2粉末需加濃鹽酸進行溶解,請結合必要的化學方程式用平衡移動原理解釋原因:________。
(3)加入Sn粉的作用有兩個:①調節溶液pH;②__________。
(4)酸性條件下,SnSO4還可以用作雙氧水去除劑,發生反應的離子方程式是:________________。
(5)該小組通過下列方法測定所用錫粉的純度(雜質不參與反應):取ag錫粉溶于鹽酸中,向生成的SnC12中加入過量的FeC13溶液,用b mol/LK2Cr2O7滴定生成的Fe2+(已知酸性環境下,Cr2O72-可被還原為Cr3+),共用去K2Cr2O7溶液m ml。則錫粉中錫的質量分數是________。(Sn的摩爾質量為M g/mol,用含a、b、m、M的代數式表示)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com