
【題目】有A、B、C、D四種強電解質,它們在水中電離時可產生下列離子(每種物質只含一種陽離子和一種陰離子且互不重復)。
陽離子 | K+、Na+、Ba2+、NH |
陰離子 | CH3COO-、Cl-、OH-、SO |
已知:①A、C溶液的pH均大于7,B溶液的pH小于7,A、B溶液中水的電離程度相同;D物質的焰色反應呈黃色;②C溶液和D溶液相遇時只生成白色沉淀,B溶液和C溶液相遇時只生成有刺激性氣味的氣體,A溶液和D溶液混合時無明顯現象。
(1)A的名稱是_______B的化學式_______
(2)寫出C溶液和D溶液反應的化學方程式___________
(3)25 ℃時,pH=9的A溶液和pH=9的C溶液中水的電離程度小的是___(填A或C)。
(4) A溶液的pH大于7,用離子方程式表示原因______。
【答案】醋酸鉀 NH4Cl ![]() C
C ![]()
【解析】
①A、C溶液的pH均大于7,應為醋酸鹽和堿溶液,B溶液的pH小于7,應為銨鹽溶液,A、B的溶液中水的電離程度相同,則溶液水解程度相同;D溶液焰色反應顯黃色,溶液中含有鈉離子,所以A為醋酸鉀;②C溶液和D溶液相遇時只生成白色沉淀,B溶液和C溶液相遇時只生成刺激性氣味的氣體,A溶液和D溶液混合時無明顯現象,則說明C為Ba(OH)2,D為Na2SO4,則B為NH4Cl。
(1) A的名稱是醋酸鉀,B的化學式是NH4Cl;
(2) C溶液和D溶液反應的化學方程式:![]() ;
;
(3)酸堿抑制水的電離,鹽促進水的電離,故25 ℃時,pH=9的A溶液和pH=9的C溶液中水的電離程度小的是C;
(4) A溶液中醋酸根離子水解產生氫氧根離子,則溶液的pH大于7:![]() 。
。


科目:高中化學 來源: 題型:
【題目】氮及其化合物與生產生活關系密切。請完成下列填空:
(1)某學校化學學習小組為探究二氧化氮的性質,按下圖所示裝置進行實驗。

①裝置甲中盛放濃硝酸的儀器A的名稱是__________________, 裝置丙中的試管內發生反應的離子方程式為:______________________________。
②實驗過程中裝置乙、丙中出現的現象分別是________________________;______________。
(2)NO在醫療上有重要的應用,曾被科學家作為研究的重要物質。現有容積為aL的試管盛滿NO后倒扣于水槽中,再向試管中通入一定體積O2后,試管內氣體的體積為試管容積的一半,則通入的O2的在相同條件下體積為____________。
A.0.75aL B.0.375aL C.0.625aL D.1.25aL
(3)在盛有一定量濃硝酸的試管中加入12.8g的銅片發生反應。請回答下列問題:
①開始階段,反應的化學方程式為_______________________________,后一階段生成的氣體為
_______,若兩者恰好完全反應整個反應過程共產生標準狀況下氣體2.24L,則反應過程中被還原的HNO3的物質的量為__________ mol.,參加反應的HNO3的物質的量為__________ mol.。
②反應結束后往試管中加入銅片,再加入少量20%的稀硫酸,這時銅片上又有氣泡產生,反應的離子方程式為____________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
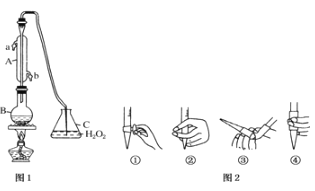
【題目】某實驗小組欲探究碳與濃硝酸反應的情況。甲同學設計了圖1裝置,認為若有紅棕色氣體產生就說明碳與濃硝酸發生了反應。
(1)乙同學認為甲同學的結論是錯誤的,他的理由是__________________________(用化學方程式表示),所以他認為應該檢驗__________(填化學式)的產生來證明碳與濃硝酸反應。為此乙同學查閱相關資料得知“0℃時四氧化二氮為液體”,從而改進了實驗裝置如圖2所示。

(2)為了減少干擾,對于A裝置有下面4種操作方案,其中最合理的是(填寫數字序號)_______。
①將炭與濃硝酸一同放在裝置中加熱;②先加熱濃硝酸,然后將炭投入其中;
③先加熱炭,再加入冷濃硝酸; ④先加熱炭,再將炭投入冷濃硝酸。
(3)請用平衡移動原理解釋B裝置的作用____________________________________。
(4)C裝置中出現的現象是_______________________________________________,經檢測C的溶液中還含有少量氮元素,只以NO3-形式存在,寫出生成該離子的化學方程式___________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中華人民共和國國家標準(G2762011)規定葡萄酒中c最大使用量為0.25g/L.某興趣小組用圖裝置(夾持裝置略)收集某葡萄酒中SO2,并對含量進行測定。
(1)儀器A的名稱是________,水通入A的進口為_______________
(2)B中加入300.0ml葡萄酒和適量鹽酸,加熱使SO2全部逸出與C中H2O2完全反應其化學方程式為_________________________________
(3)除去C中過量的H2O2,然后用0.0900mol/LNaOH標準溶液進行滴定,滴定前排氣泡時,應選擇圖2中的________;若滴定終點時溶液的pH=8.8,則選擇的指示劑為________;若用50mL滴定管進行實驗,當滴定管中的液面在刻度“20”處,則管內液體的體積______(填序號)
(①=20mL,②=30mL,③<20mL,④>30mL).
(4)滴定至終點時,消耗NaOH溶液12.50mL,該葡萄酒中SO2含量為:___g/L
(5)該測定結果比實際值偏高,分析原因并利用現有裝置提出改進措施______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求完成填空
(1)計算25 ℃時下列溶液的pH:
①1 mL pH=2的H2SO4加水稀釋至100 mL,pH=________;
②0.001 mol/L的鹽酸,pH=________;
③0.01 mol/L的NaOH溶液,pH=________;
④0.015 mol/L的硫酸與0.01 mol/L的NaOH等體積混合,混合溶液的pH=________。
(2)H2S溶于水的電離方程式為_______________________________________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E五種元素,已知:
①A原子的最外層電子數是次外層電子數的兩倍,B的陰離子與C的陽離子跟氖原子的電子層結構相同,E原子的最外層上的電子數比最內層多5。
②常溫下B2是氣體,它的相對分子質量是氫氣的16倍。
③C的單質在B2中燃燒,生成淡黃色固體F,F與AB2反應可生成B2。
④D的單質在B2中燃燒,發出藍紫色火焰,生成有刺激性氣味的氣體DB2,D在DB2中的含量為50%。根據以上情況回答:
(1)E位于第___周期___族;
(2)C的離子結構示意圖是_____,F中的化學鍵為______;
(3)AB2的電子式為___; F和AB2反應的化學方程式為_______;
(4)C、D、E三種元素的原子半徑從小到大的順序為___; (用元素符號回答)
(5)常溫下,E的單質與C的最高價氧化物對應水化物的水溶液反應的離子方程式為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面有關晶體的敘述中,不正確的是( )
A.金剛石為網狀結構,由共價鍵形成的碳原子環中,最小的環上有6個碳原子
B.氯化鈉晶體中,每個Na+周圍緊鄰且距離相等的Na+共有6個
C.氯化銫晶體中,每個Cs+周圍緊鄰且距離相等的Cl-有8個
D.干冰晶體中,每個CO2分子周圍緊鄰且距離相等的CO2分子有12個
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵及其化合物在有機化學中應用廣泛,例如有機合成中,常用鐵和鹽酸將硝基(﹣NO2)還原為氨基(﹣NH2);在苯的溴代反應中用溴化鐵作催化劑。
(1)N的原子結構示意圖為_______,Fe基態原子核外電子排布式為_______。
(2)H、N、O 的電負性從小到大的順序是_______。
(3)與NO2+互為等電子體的一種分子為_____(填化學式),氨基(﹣NH2)中氮原子的雜化類型為_____。
(4)1mol苯分子中含有σ鍵的物質的量為______。
(5)Fe 與 N 形成的某化合物晶胞如圖所示,則該晶體的化學式為_______。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應:2NO2(g)![]() 2NO(g) + O2(g),在體積不變的密閉容器中反應,達到平衡狀態的標志是( )
2NO(g) + O2(g),在體積不變的密閉容器中反應,達到平衡狀態的標志是( )
①單位時間內生成n mol O2的同時生成2 n mol NO2
②單位時間內生成n mol O2的同時生成2 n mol NO
③用NO2、NO、O2表示的反應速率數值之比為2∶2∶1的狀態
④混合氣體的顏色不再改變的狀態
A.①④B.②③C.①③④D.①②③④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com